研载生物科技(上海)有限公司
9 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
公司新闻/正文
紧跟前沿步伐!“hiPSC-CMs与EV调控”探索新进展,核心内容全盘揭秘——15+的创新佳作,快快记下!!
482 人阅读发布时间:2024-12-16 16:04
心肌梗死(MI)是世界范围内死亡的主要原因。尽管目前有治疗方案,但心肌梗死后心力衰竭的发病率预计在未来几年将增加。很明显,对促进心脏修复的新方法的需求尚未得到满足。最近有报道称,缺血心脏组织释放的细胞外囊泡(EVs)在急性心肌梗死和慢性缺血重塑后驱动心脏修复。

湾湾今天分享的是发表在【J Extracell Vesicles】(IF:15.5)上题为“Hypoxia and TNF-alpha modulate extracellular vesicle release from human induced pluripotent stem cell-derived cardiomyocytes”的研究,在该研究中,作者旨在了解CM-EV在基础培养条件下的生物发生和分泌的调控机制,并结合已知的心肌梗死后应激源,如营养和氧气剥夺,以及暴露于促炎刺激。为了实现这一目标,生成了表达NanoLuc-tetraspanin报告基因的hiPSC-CMs,这使得直接从条件培养基中研究CM-EV的生物发生成为可能。作者确定了在基础培养条件下使用小分子抑制剂参与tetraspanin阳性CM-EV生物发生的几种途径。此外,作者发现心肌梗死相关条件可调节CM-EV释放,并发现中性鞘磷脂酶2 (nSMase2)在缺氧驱动的EV分泌中的作用,以及NLRP3炎症小体和mTOR信号传导在TNF-α-诱导的EV释放中的潜在作用。
研究结果
1.hiPSC来源的心肌细胞(hiPSC-CMs)分泌细胞外囊泡(sEVs)
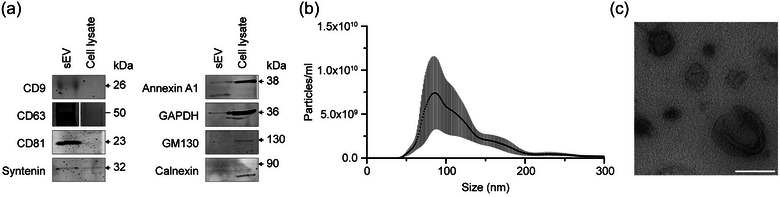
图1a:Western blot分析hiPSC-CMs条件培养基中差异超离心分离的sEVs的蛋白标志物CD9、CD63、CD81、Syntenin、Annexin A1和细胞富集的蛋白标记物GAPDH、GM130、Calnexin的表达。
图1b:纳米粒子跟踪分析(NTA)分析sEVs的颗粒大小和分布。
图1c:透射电镜(TEM)分析sEVs的形态。
以上数据表明,该研究中使用的hiPSC-CMs释放了sEVs。
2.NanoLuc-tetraspanin报告可以直接定量hiPSC-CMs的sEV分泌
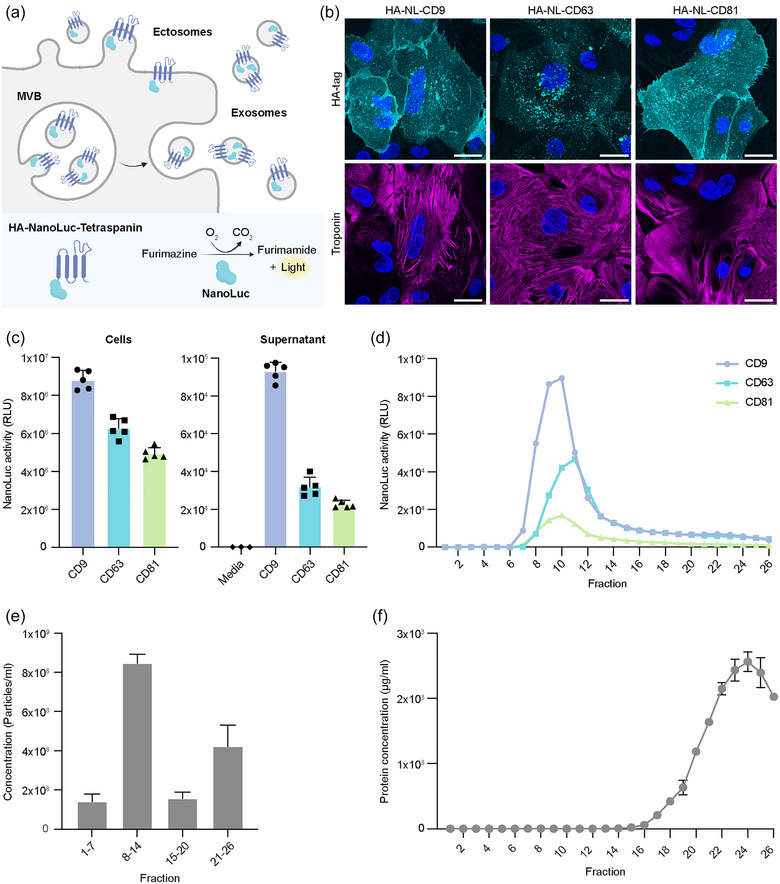
图2a:使用HA-NanoLuc(NL)-tetraspanin报告器定量sEVs的示意图。HA-NL-tetraspanin报告体被分为外泌体和外泌体,通过测量培养上清中NanoLuc生物发光活性,可以量化tetraspanin阳性EV的分泌。
图2b:hiPSC-CMs的代表性免疫荧光图像用HA标记的NL-tetraspanin报告基因转导,并进行HA标记和心肌肌钙蛋白染色。
图2c:表达HA-NL-tetraspanin报告基因的hiPSC-CMs细胞和条件培养上清中NanoLuc活性的代表性测量。
图2d:从表达HA-NL-tetraspanin报告基因的hiPSC-CMs上清液中获得的大小排阻色谱(SEC)组分的代表性发光测量。
图2e:纳米粒子跟踪分析(NTA)分析了混合的SEC组分的粒子数(>50 nm)的代表性图。
图2f:SEC各组分蛋白质浓度的代表性曲线图。
以上数据表明,生成了稳定表达HA-NL-tetraspanin报告基因的hiPSC-CMs。这些细胞可以用来测量相对较少的细胞从条件培养基中直接释放的tetraspanin阳性EV。
3.细胞外囊泡生物发生调节剂对hiPSC-CMs分泌NanoLuc-tetraspanin的影响
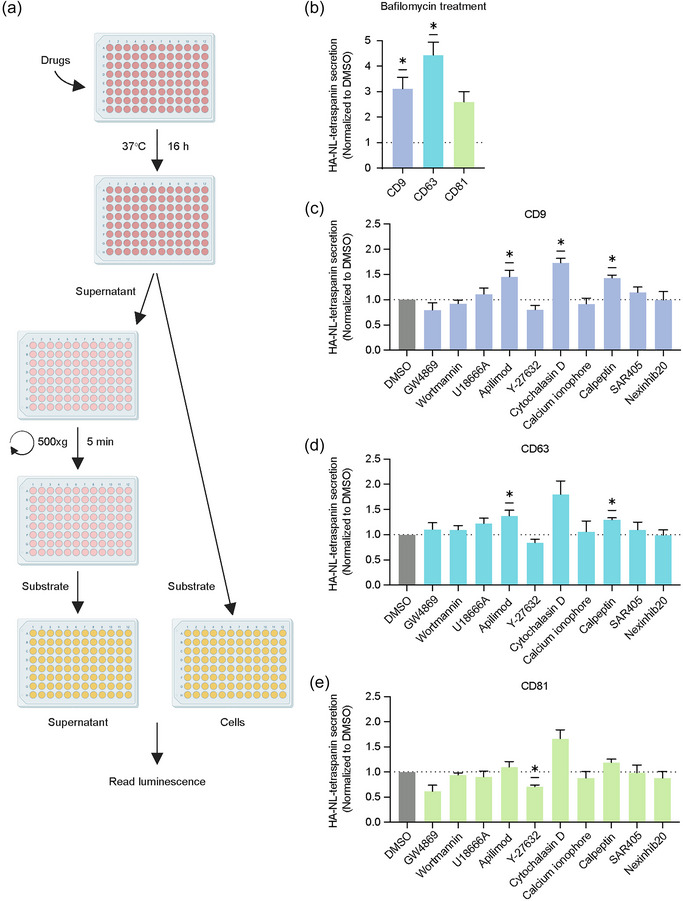
图3a:利用NanoLuc-tetraspanin报告基因在hiPSC-CMs中进行小分子筛选的实验方法示意图。
图3b:巴弗洛霉素(0.1 μM)治疗后的NanoLuc-tetraspanin分泌与DMSO对照归一化。
图3c-e:NanoLuc-tetraspanin分泌CD9、CD63和CD81的分析。
以上数据表明,表达HA-NL-tetraspanins的心肌细胞可用于筛选CM-EVs分泌的调节剂,并提示多种参与者参与了tetraspanins阳性CM-EVs的生物发生。
4.应激条件通过hiPSC-CMs调节tetraspanin阳性EV的分泌
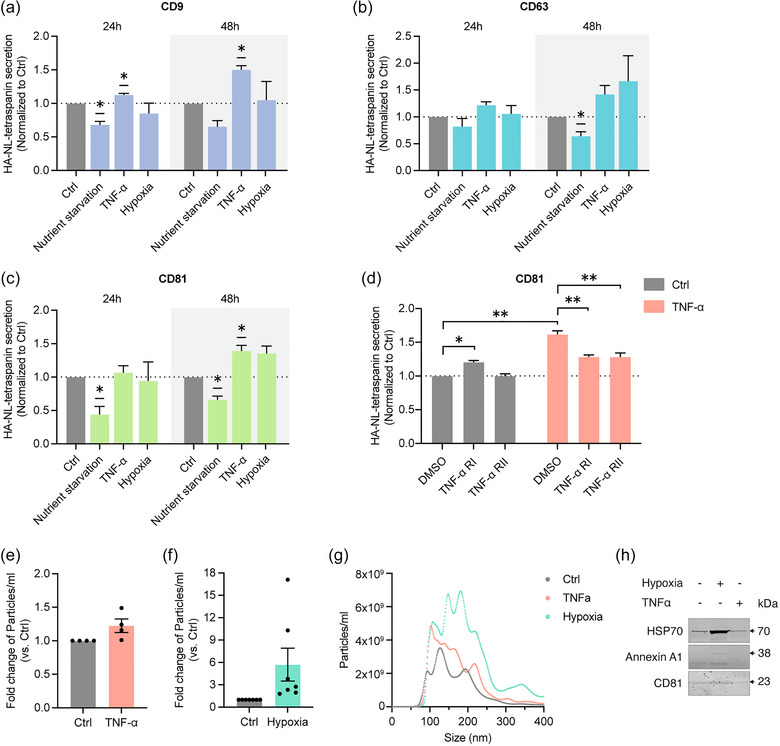
图4a-c:不同应激条件(营养饥饿、10 ng/mL TNF-α和缺氧)对24和48 h后NanoLuc-CD9、NanoLuc-CD63和NanoLuc-CD81分泌的影响。
图4d:在控制(Ctrl)和TNF-α条件下,NanoLuc-CD81分泌与TNF-α受体I(TNF-α RI)或II(TNF-α RII)的中和抗体联合。
图4e-g:纳米颗粒跟踪分析(NTA)分析了控制48 h后释放的sEVs、TNF-α和缺氧的颗粒浓度与对照组相比的倍数变化和代表性尺寸分布曲线。
图4h:在对照组、缺氧和TNF-α条件下48 h后释放的sEVs的两个独立实验中,对EV标志物(HSP70、膜联蛋白A1和CD81)进行代表性的western blot分析。
以上数据表明,hiPSC-CMs释放多个EV和颗粒亚群,并强调MI相关的应激条件影响hiPSC-CMs分泌tetraspanin阳性EV。
5.中性鞘磷脂酶2在缺氧条件下介导四球蛋白阳性EV释放
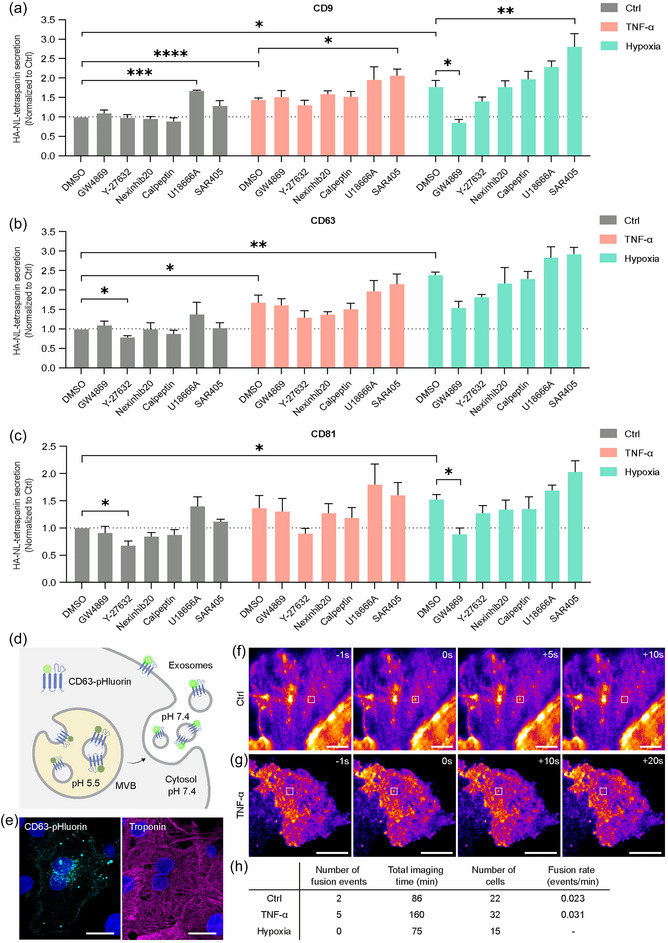
图5a-c:EV生物发生调节剂GW4869 (5 μM)、Y-27632 (5 μM)、nexinhib20 (1 μM)、calpeptin (5 μM)、U18666A (5 μM)和SAR405 (1 μM)对CD9、CD63、CD81 阳性EV培养48 h后在对照(Ctrl)、10 ng/mL TNF-α和缺氧条件下NanoLuc-tetraspanin分泌的影响。
图5d:CD63-pHluorin在MVB -质膜融合成像中的图示。
图5e:CD63-pHluorin在hiPSC-CMs中的定位。
图5f-g:对照和TNF-α-处理的hiPSC-CMs中CD63-pHluorin融合事件的延时TIRF成像。
图5h:CD63-pHluorin hiPSC-CMs在对照、TNF-α和缺氧条件下的MVB -质膜融合率。
6.炎性小体激活和mTOR信号传导有助于TNF-α诱导的HA-NL-CD81分泌
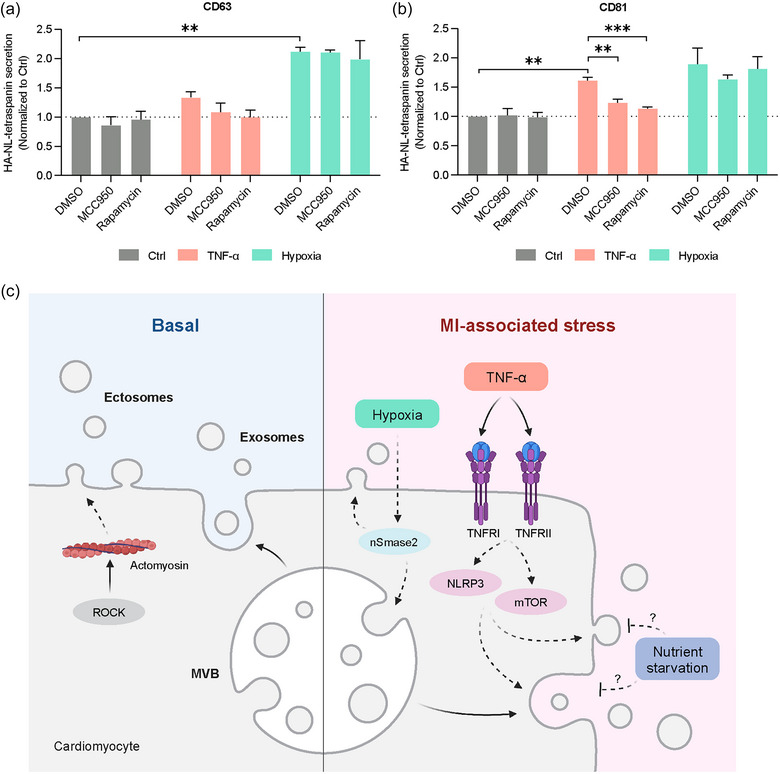
图6a-b:在控制炎症小体抑制剂MCC950或mTOR抑制剂雷帕霉素孵育48小时后,在TNF-α和缺氧条件下,NanoLuc-tetraspanin分泌CD63 (a)和CD81 (b)。
图6c:总结本研究结果的方案。在hiPSC-CMs中,EV的生物发生依赖于环境。在基础培养条件下,hiPSC-CMs可以分泌外泌体和外泌体,其释放部分由ROCK介导。营养饥饿减少CM-EV的分泌,而缺氧则以依赖nsmase2的方式增加CM-EV的产生。TNF-α通过NLRP3炎性体激活和mTOR信号传导增加CM-EV分泌。
以上数据结果表明,炎症小体激活和mTOR信号在TNF-α-诱导的CM-EV分泌中起作用。
总结
综上,作者生成了表达HA - NL -tetraspanin的hiPSC-CMs,可以从少量细胞(70K)中定量CM-EV分泌,而无需繁琐且耗时的EV分离技术。利用这些细胞鉴定了在基础和心肌梗死相关应激条件下tetraspanin阳性CM-EV生物发生的调节因子,证明了这种多报告者方法的力量。作者观察到在基础培养条件下,hiPSC-CMs能分泌外泌体,外泌体作为CM-EV释放的一部分是由ROCK介导的。此外,证明了EV在hiPSC-CMs中的生物发生依赖于环境。营养饥饿降低HA-NL-tetraspanin分泌,而缺氧以nsmase2依赖的方式增加了tetraspanin阳性EV的产生。此外,TNF-α通过NLRP3炎性体激活和mTOR信号传导的过程增加了tetraspanin阳性EV的分泌。这项工作为更大的筛选铺平了道路,这将提高对体内平衡和疾病中CM-EV生物发生的分子机制的理解,这将有助于开发新的心肌梗死药理策略。






