研载生物科技(上海)有限公司
9 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
公司新闻/正文
J Adv Res 13|天然益生菌外泌体负载黑色素纳米颗粒,抗氧化+菌群调节双效协同,UC可视化治疗迈向临床!
75 人阅读发布时间:2026-03-27 11:10
外泌体作为天然纳米级细胞间通讯载体,凭借其低免疫原性、良好生物相容性及可工程化改造潜力,已成为药物递送系统和无细胞治疗平台的研究热点。近年来,外泌体研究正从传统的哺乳动物细胞来源拓展至更广泛的生物来源,其中益生菌来源外泌体因其天然的安全性、抗炎活性及菌群调节功能,在肠道炎症性疾病治疗中展现出独特优势。

今天分享的是一篇发表在【J Adv Res.】(IF:13)上题为“Melanin nanoparticles-loaded lactobacillus fermentum exosomes for targeted and visualized treatment of ulcerative colitis”的研究,该研究构建了黑色素纳米颗粒负载发酵乳杆菌外泌体(MNPs-Lf-EVs),通过超声破碎法将黑色素纳米颗粒(MNPs)封装于发酵乳杆菌来源外泌体(Lf-EVs)中,旨在利用Lf-EVs的肠道靶向性和菌群调节作用,结合MNPs的抗氧化与光声成像功能,精准靶向溃疡性结肠炎(UC)肠道炎症部位,通过清除ROS、缓解炎症、修复肠道屏障及调节肠道菌群发挥治疗作用,为UC提供靶向可视化的新型治疗策略。
研究成果
1. MNPs-Lf-EVs的制备及基本表征
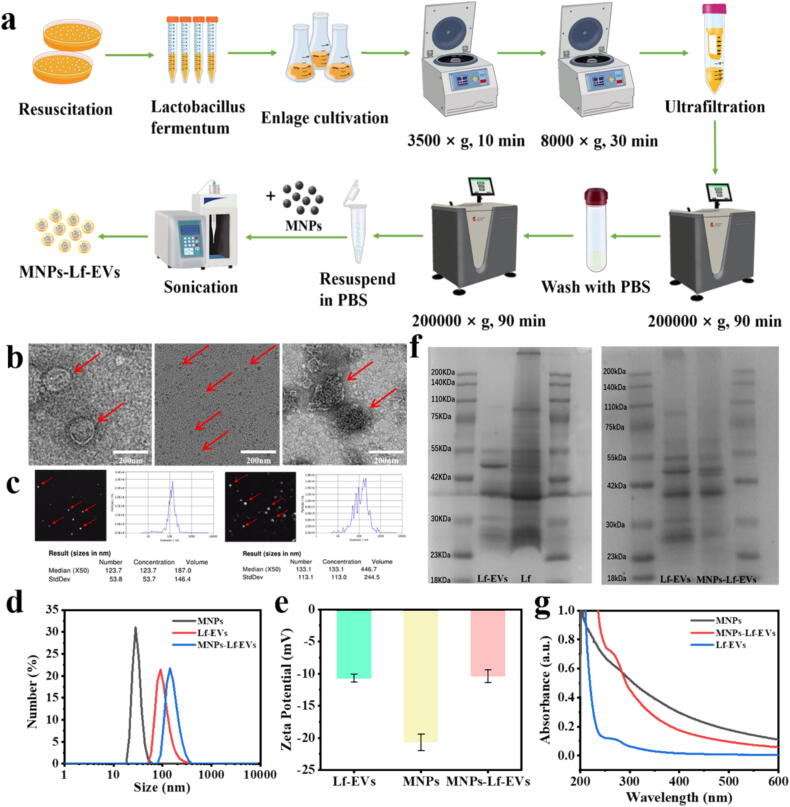
图1A:制备流程示意图。
图1B:透射电镜(TEM)检测。结果显示,Lf-EVs呈典型双凹圆盘状,直径约150 nm;MNPs粒径均一且尺寸较小;MNPs-Lf-EVs保留外泌体膜结构,MNPs成功封装于其中。
图1C:纳米颗粒追踪分析(NTA)。结果显示,Lf-EVs平均粒径约123 nm,MNPs-Lf-EVs平均粒径略增至133 nm。
图1D:动态光散射(DLS)检测。结果显示,Lf-EVs、MNPs、MNPs-Lf-EVs的水合粒径分别约为155 nm、40 nm、210 nm,与TEM和NTA结果趋势一致。
图1E:Zeta电位检测。结果显示,Lf-EVs电位为-10.7±0.7 mV,MNPs为-20.7±1.3 mV,MNPs-Lf-EVs电位为-10.3±1.0 mV,与Lf-EVs电位接近。
图1F:SDS-PAGE电泳。结果显示,Lf-EVs的蛋白条带主要分布在23-55 kDa之间,少量分布于75-110 kDa,与Lf细胞膜蛋白条带分布基本一致;装载MNPs后,大部分蛋白条带保留,表明超声破碎法未破坏Lf-EVs的主要蛋白成分。
图1G:紫外-可见吸收光谱。结果显示,Lf-EVs在280 nm处有微弱吸收峰;MNPs在200-600 nm范围内有宽吸收峰,且随波长接近200 nm逐渐升高;MNPs-Lf-EVs同时具备两者的吸收特征,证实MNPs成功装载。
这些结果表明,通过超声破碎法成功制备了MNPs-Lf-EVs,该载体保留了Lf-EVs的基本结构和蛋白成分,MNPs装载后粒径和电位符合纳米载体的特性要求。
2. MNPs-Lf-EVs的光声性能、抗氧化活性、稳定性及释放特性
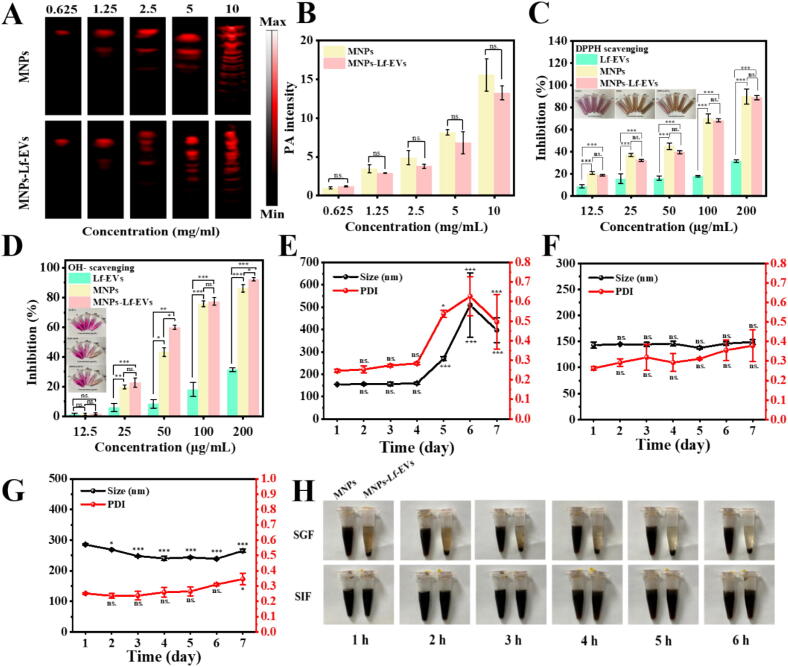
图2A:体外光声(PA)成像。结果显示,MNPs和MNPs-Lf-EVs的PA信号强度均随浓度升高而增强,呈浓度依赖性。
图2B:PA信号半定量分析。结果显示,相同浓度下MNPs与MNPs-Lf-EVs的PA信号强度无显著差异,表明MNPs装载后仍保留良好的光声成像性能。
图2C:DPPH自由基清除实验。结果显示,Lf-EVs无明显自由基清除能力;200 μg/mL时,MNPs-Lf-EVs的DPPH清除率达88.82±1.9%,与MNPs清除能力相当。
图2D:羟基自由基(OH⁻)清除实验。结果显示,200 μg/mL时,MNPs-Lf-EVs的OH⁻清除率达92.23±1.1%,与MNPs清除能力相近,表明MNPs-Lf-EVs保留了优异的抗氧化活性。
图2E:Lf-EVs在4°C下的稳定性检测。结果显示,Lf-EVs在4℃储存时,从第5天起粒径和PDI显著升高,最大粒径达509.1±143.4 nm,PDI达0.62±0.1,稳定性较差。
图2F:Lf-EVs在−20°C下的稳定性检测。结果显示,Lf-EVs在-20℃储存时,粒径和PDI保持稳定,表明低温可维持其结构完整性。
图2G:MNPs-Lf-EVs在4°C下的稳定性检测。结果显示,MNPs-Lf-EVs在4℃储存1周内,粒径、PDI、Zeta电位及形态基本无变化,封装效率从35%降至28%,稳定性优于Lf-EVs。
图2H:模拟胃肠道环境稳定性实验。结果显示,MNPs在模拟胃液(SGF)中易聚集沉淀,而MNPs-Lf-EVs在SGF中保持稳定分散;在模拟肠液(SIF)中,两者均均匀分散,MNPs-Lf-EVs可实现MNPs的肠道靶向释放。
这些结果表明,MNPs-Lf-EVs保留了MNPs的光声成像性能和抗氧化活性,具有良好的储存稳定性和胃肠道环境耐受性,可在肠道内定向释放MNPs。
3. MNPs-Lf-EVs的体外细胞毒性、细胞摄取及划痕修复实验
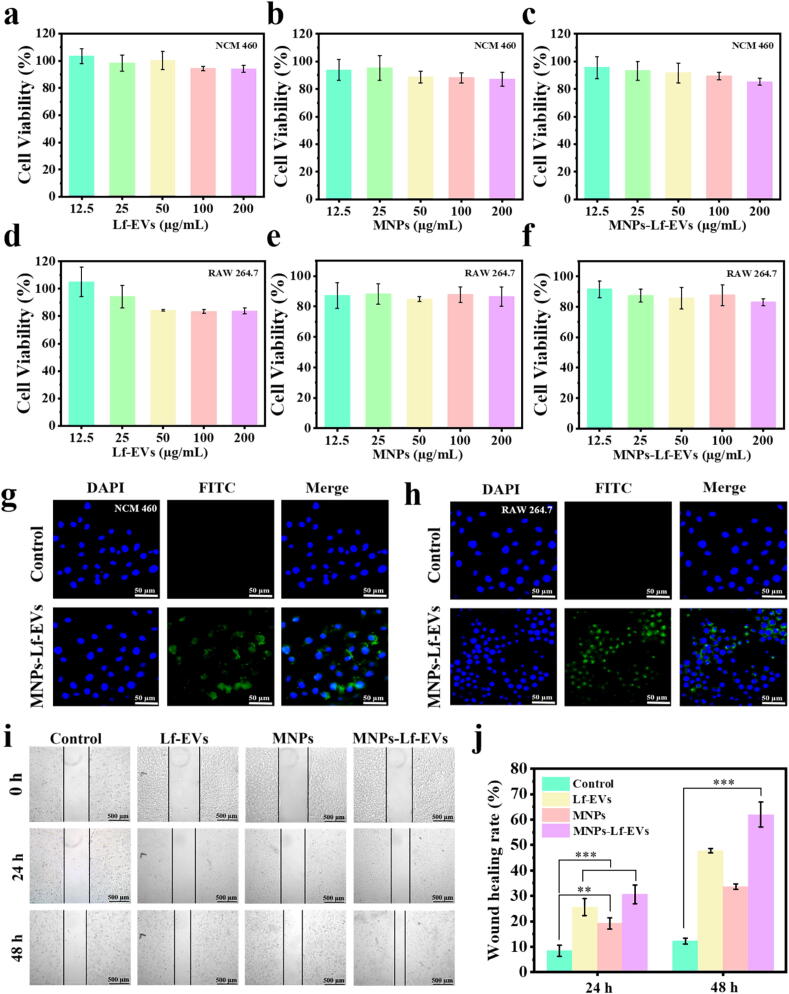
图3A-F:CCK-8实验。结果显示,当Lf-EVs、MNPs、MNPs-Lf-EVs浓度高达200 μg/mL时,对人正常结肠上皮细胞(NCM460)和小鼠腹腔巨噬细胞(RAW264.7)的存活率均无显著影响,表明三种载体均具有良好的生物相容性。
图3G:荧光显微镜观察。结果显示,FITC标记的MNPs-Lf-EVs与NCM460细胞共培养6h后,细胞内出现明显绿色荧光,证实NCM460细胞可成功摄取MNPs-Lf-EVs。
图3H:荧光显微镜观察。结果显示,RAW264.7细胞可有效摄取FITC标记的MNPs-Lf-EVs,细胞内可见绿色荧光分布。
图3I:NCM460细胞划痕实验。结果显示,与对照组相比,Lf-EVs、MNPs、MNPs-Lf-EVs处理组的划痕距离随时间逐渐缩短,MNPs-Lf-EVs组划痕愈合速度最快。
图3J:划痕愈合率定量。结果显示,48h时MNPs-Lf-EVs组细胞迁移率达62%,较对照组提升约49.8%,显著高于Lf-EVs组和MNPs组。
这些结果表明,MNPs-Lf-EVs无明显细胞毒性,可被肠道上皮细胞和巨噬细胞高效摄取,且能显著促进肠道上皮细胞迁移,增强损伤修复能力。
4. MNPs-Lf-EVs对LPS刺激后细胞的保护作用
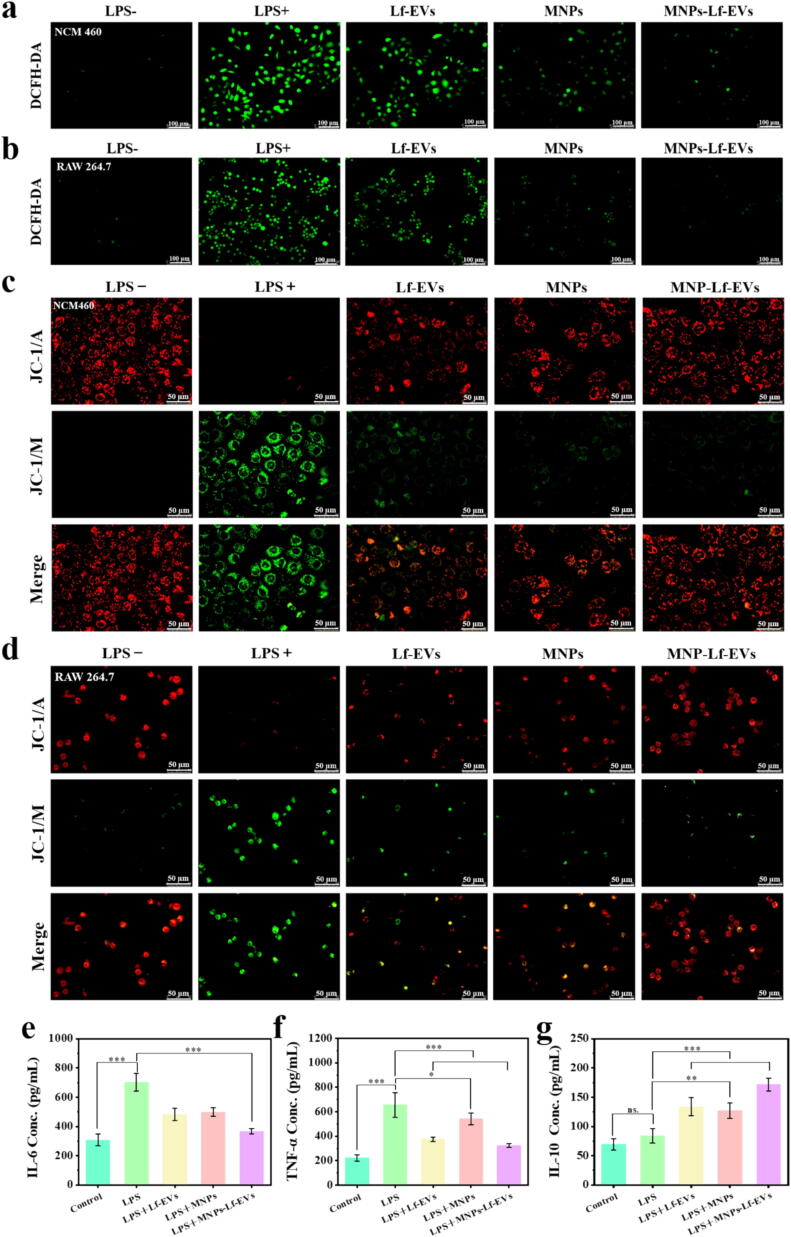
图4A:NCM 460内活性氧的荧光显微镜图像。结果显示,LPS刺激后NCM460细胞内ROS水平显著升高;经Lf-EVs、MNPs、MNPs-Lf-EVs处理后,绿色荧光强度依次减弱,MNPs-Lf-EVs组ROS清除效果最显著。
图4B:RAW 264.7内活性氧的荧光显微镜图像。结果显示,RAW264.7细胞经LPS刺激后ROS大量产生;MNPs-Lf-EVs处理后绿色荧光最弱,ROS清除能力最优。
图4C:NCM 460的JC-1荧光显微镜图像。结果显示,LPS刺激后NCM460细胞线粒体膜电位(MMP)下降,绿色荧光强;处理组红色荧光逐渐增强、绿色荧光减弱,MNPs-Lf-EVs组线粒体功能恢复最明显。
图4D:RAW264.7的JC-1荧光显微镜图像。结果显示,RAW264.7细胞经LPS刺激后MMP降低;MNPs-Lf-EVs处理后红色荧光占比最高,可有效抑制线粒体功能紊乱。
图4E:ELISA检测促炎因子IL-6水平。结果显示,LPS刺激后RAW264.7细胞分泌的促炎因子IL-6水平显著升高;处理组IL-6水平显著降低,MNPs-Lf-EVs组抑制效果最显著。
图4F:ELISA检测促炎因子TNF-α水平。结果显示,LPS刺激后RAW264.7细胞分泌的促炎因子TNF-α水平大幅升高;MNPs-Lf-EVs组TNF-α水平显著低于其他处理组,抗炎效果最优。
图4G:ELISA检测抗炎因子IL-10水平。结果显示,LPS刺激后RAW264.7细胞分泌的抗炎因子IL-10水平降低;MNPs-Lf-EVs组IL-10水平显著升高,可有效调节细胞因子平衡。
这些结果表明,MNPs-Lf-EVs可通过清除细胞内ROS、维持线粒体膜电位、抑制促炎因子分泌、上调抗炎因子表达,对LPS诱导的损伤细胞发挥显著保护作用。
5. MNPs-Lf-EVs在体内的荧光成像及靶向分布
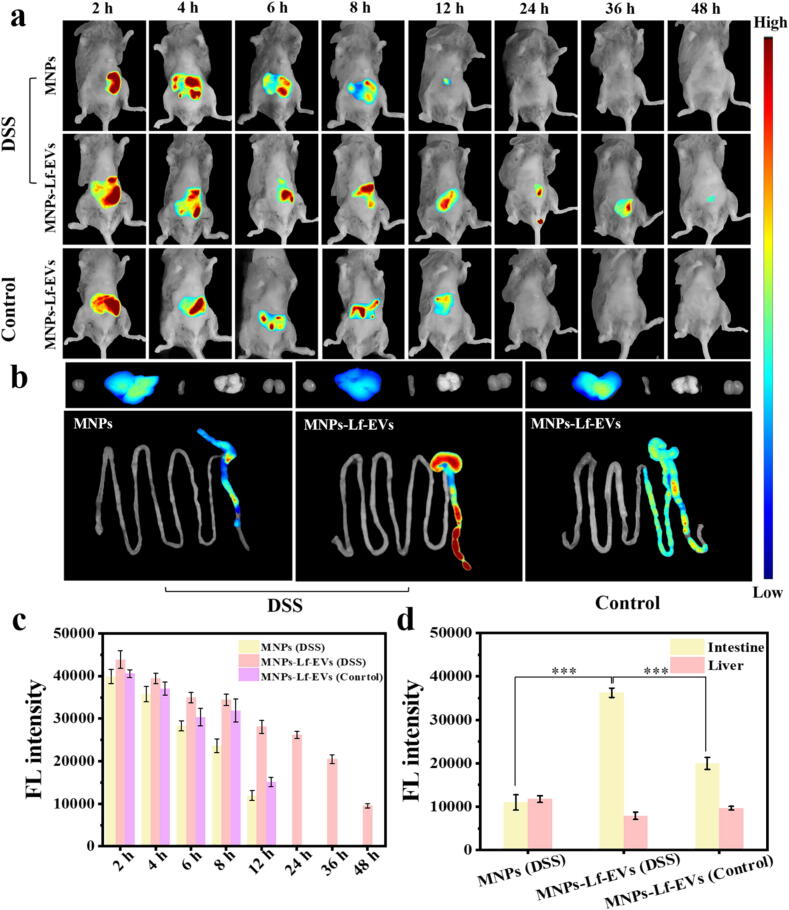
图5A:体内NIR-II荧光成像。结果显示,健康小鼠和UC模型小鼠口服ICG标记的MNPs和MNPs-Lf-EVs后,模型组中MNPs-Lf-EVs的肠道荧光信号在12h内持续维持较高强度,且持续时间长达36h;而MNPs组肠道荧光信号在24h时基本消失,表明MNPs-Lf-EVs具有更强的炎症靶向滞留能力。
图5B:离体器官荧光成像。结果显示,12h时模型组小鼠结肠组织中MNPs-Lf-EVs的荧光信号最强,而MNPs组和健康小鼠MNPs-Lf-EVs组的结肠荧光信号较弱;肝脏中MNPs组和健康小鼠MNPs-Lf-EVs组荧光信号更强,提示其被肝脏代谢清除。
图5C:体内荧光强度半定量。结果显示,模型组MNPs-Lf-EVs在肠道的荧光信号强度显著高于其他组,且在各时间点均保持较高水平。
图5D:离体器官荧光强度半定量。结果显示,模型组MNPs-Lf-EVs在结肠组织的荧光强度显著高于其他组,证实其对肠道炎症部位的靶向聚集能力。
这些结果表明,MNPs-Lf-EVs口服后可抵抗胃肠道环境,靶向聚集于UC模型小鼠的结肠炎症部位,且滞留时间长,具备良好的炎症靶向性。
6. MNPs-Lf-EVs在体内的光声成像监测
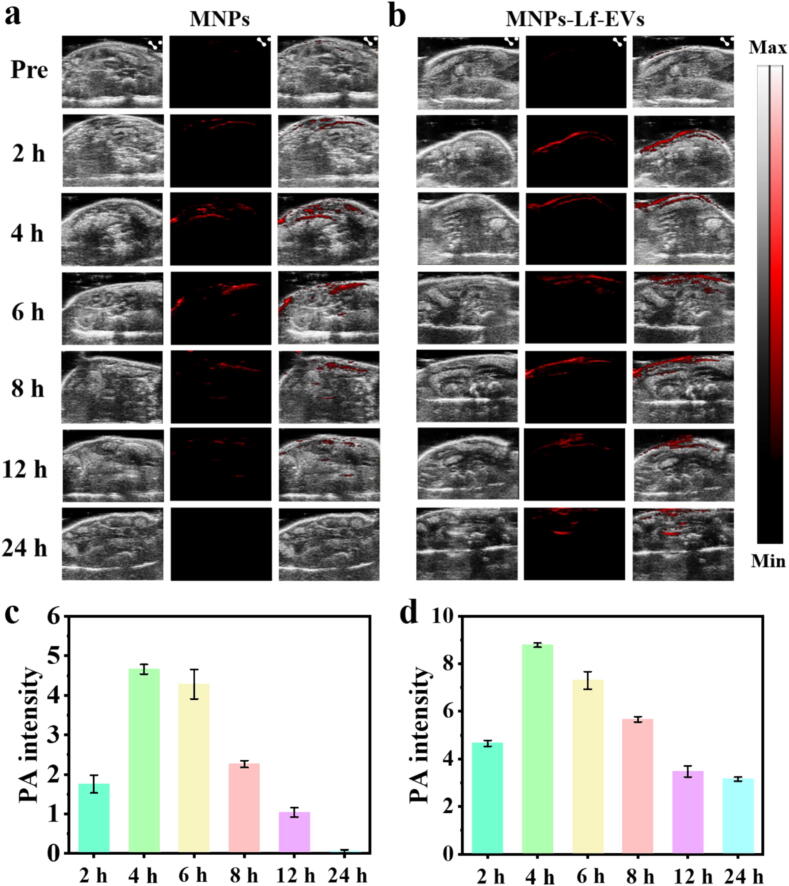
图6A:UC小鼠不同时间点MNPs的PA图像。结果显示,UC模型小鼠注射MNPs后,肠道光声信号随时间逐渐增强,4h达峰值后开始减弱,24h时信号基本消失。
图6B:UC小鼠不同时间点MNPs-Lf-EVs的PA图像。结果显示,UC模型小鼠注射MNPs-Lf-EVs后,肠道光声信号在4h达峰值,且在各时间点的信号强度均高于MNPs组,24h时仍维持较强信号。
图6C:UC小鼠不同时间点MNPs PA图像信号强度的半定量数据。结果显示,MNPs组信号峰值出现于4h,随后快速下降,24h信号强度接近基线。
图6D:UC小鼠不同时间点MNPs-Lf-EVs PA图像信号强度的半定量数据。结果显示,MNPs-Lf-EVs组信号峰值同样出现于4h,且峰值强度更高,24h时仍保持较高信号水平,与荧光成像结果一致。
这些结果表明,MNPs-Lf-EVs可通过光声成像实时监测其在肠道炎症部位的动态分布,为UC的可视化治疗提供技术支持。
7. MNPs-Lf-EVs对DSS诱导UC小鼠的治疗效果
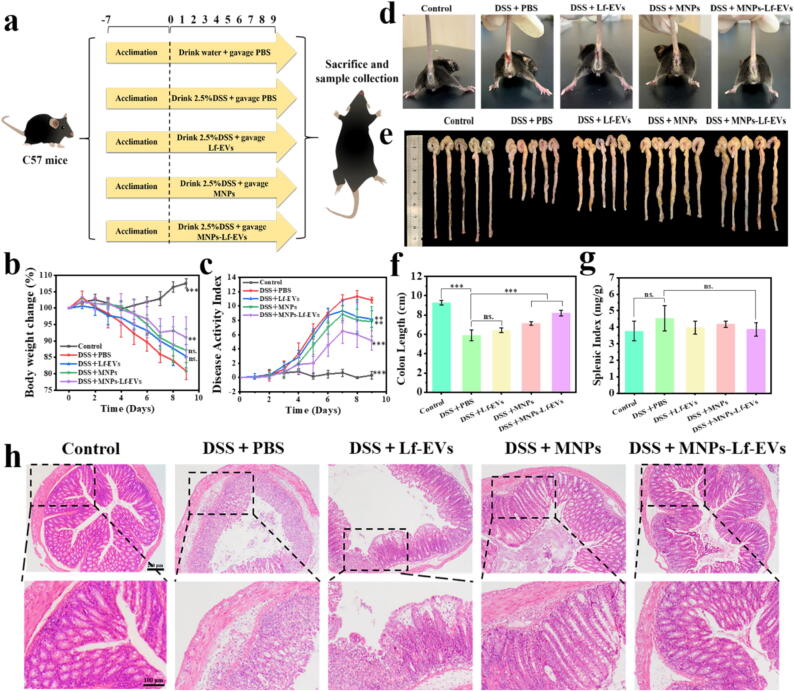
图7A:动物实验流程示意图。
图7B:体重变化曲线。结果显示,DSS模型组小鼠体重逐渐下降,第10天体重降幅达20%;Lf-EVs组、MNPs组、MNPs-Lf-EVs组体重降幅分别为14.7%、12.8%、8.9%,MNPs-Lf-EVs组体重维持效果最优。
图7C:疾病活动指数(DAI)评分。结果显示,DSS模型组DAI评分持续升高;MNPs-Lf-EVs组DAI评分显著低于其他处理组,症状改善最明显。
图7D:便血情况观察。结果显示,DSS模型组第5天出现严重便血;各处理组便血出现时间延迟(6-8天),且严重程度显著轻于模型组,MNPs-Lf-EVs组便血症状最轻。
图7E:结肠实物图。结果显示,DSS模型组结肠明显缩短、充血水肿;各处理组结肠形态改善,MNPs-Lf-EVs组结肠长度最接近正常组。
图7F:结肠长度统计。结果显示,正常组结肠长度为9.28±0.3 cm,DSS模型组缩短至5.9±0.5 cm;MNPs-Lf-EVs组结肠长度增至8.2±0.3 cm,显著长于其他处理组。
图7G:脾脏指数检测。结果显示,DSS模型组脾脏指数显著升高;MNPs-Lf-EVs组脾脏指数显著降低,最接近正常组,表明其可调节小鼠免疫功能。
图7H:HE染色。结果显示,DSS模型组结肠黏膜上皮坏死、隐窝结构丢失、炎性细胞大量浸润;MNPs-Lf-EVs组结肠黏膜结构基本恢复,隐窝完整,炎性细胞浸润显著减少。
这些结果表明,MNPs-Lf-EVs可显著改善UC小鼠的体重下降、便血、结肠缩短等症状,减轻结肠组织病理损伤,治疗效果优于单独使用Lf-EVs或MNPs。
8. MNPs-Lf-EVs治疗UC的体内机制验证
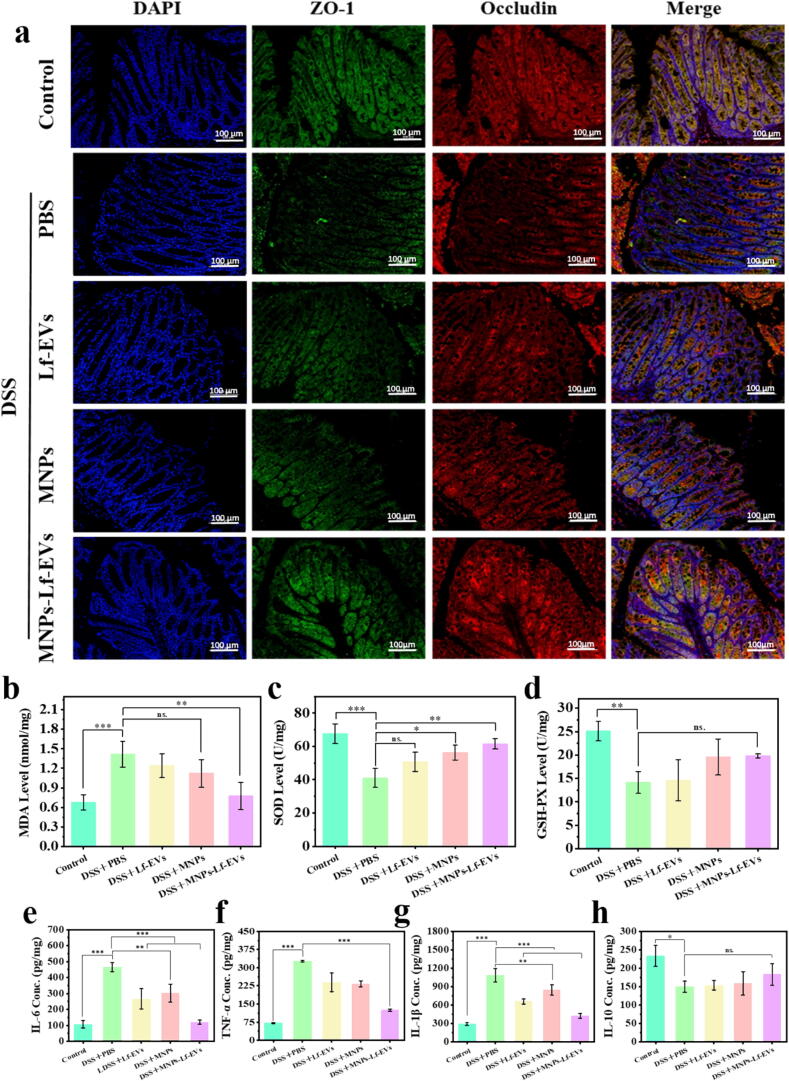
图8A:各组小鼠结肠中ZO-1和Occludin免疫荧光染色的代表性图像。结果显示,DSS模型组结肠组织中紧密连接蛋白ZO-1和Occludin表达显著降低;MNPs-Lf-EVs组ZO-1和Occludin荧光信号最强,表达水平最接近正常组,表明其可有效修复受损的肠道屏障。
图8B:各组小鼠结肠组织中的MDA含量。结果显示,DSS模型组丙二醛(MDA)含量显著升高;MNPs-Lf-EVs组MDA含量显著降低,抗氧化效果最优。
图8C:各组小鼠结肠组织中的SOD含量。结果显示,DSS模型组超氧化物歧化酶(SOD)活性显著降低;MNPs-Lf-EVs组SOD活性显著升高,可有效增强机体抗氧化能力。
图8D:各组小鼠结肠组织中的GSH-PX含量。结果显示,DSS模型组谷胱甘肽过氧化物酶(GSH-PX)活性显著降低;MNPs-Lf-EVs组GSH-PX活性显著升高,氧化应激状态明显改善。
图8E:ELISA检测各组小鼠结肠组织中的IL-6含量。结果显示,DSS模型组结肠组织中促炎因子IL-6水平显著升高;MNPs-Lf-EVs组IL-6水平显著降低,抗炎效果显著。
图8F:ELISA检测各组小鼠结肠组织中的TNF-α含量。结果显示,DSS模型组结肠组织中促炎因子TNF-α水平大幅升高;MNPs-Lf-EVs组TNF-α水平显著低于其他处理组,可有效抑制炎症反应。
图8G:ELISA检测各组小鼠结肠组织中的IL-1β含量。结果显示,DSS模型组结肠组织中促炎因子IL-1β水平显著升高;MNPs-Lf-EVs组IL-1β水平显著降低,炎症抑制效果最优。
图8H:ELISA检测各组小鼠结肠组织中的IL-10含量。结果显示,DSS模型组结肠组织中抗炎因子IL-10水平显著降低;MNPs-Lf-EVs组IL-10水平显著升高,可有效恢复细胞因子平衡。
这些结果表明,MNPs-Lf-EVs可通过修复肠道屏障、减轻氧化应激、抑制促炎因子分泌、上调抗炎因子表达,多维度发挥抗UC作用。
9. MNPs-Lf-EVs对UC小鼠肠道菌群的调节作用
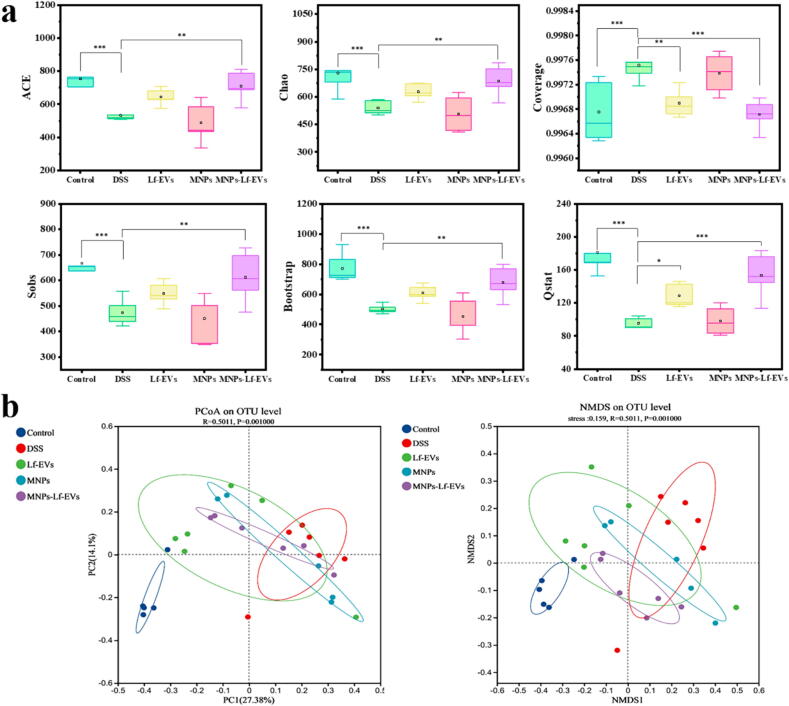
图9A:α多样性分析(ACE、Chao、Coverage等6种指数)。结果显示,DSS模型组肠道菌群多样性和丰富度显著降低;各处理组菌群多样性和丰富度均有提升,MNPs-Lf-EVs组改善最显著,接近正常组。
图9B:β多样性分析(PCoA和NMDS)。结果显示,各组间菌群结构存在显著差异;MNPs-Lf-EVs组菌群结构介于正常组和模型组之间,且更接近正常组,表明其可有效重塑肠道菌群结构。
这些结果表明,MNPs-Lf-EVs能显著提升UC小鼠肠道菌群的多样性和丰富度,重塑肠道菌群平衡。
10. MNPs-Lf-EVs对肠道菌群组成的影响
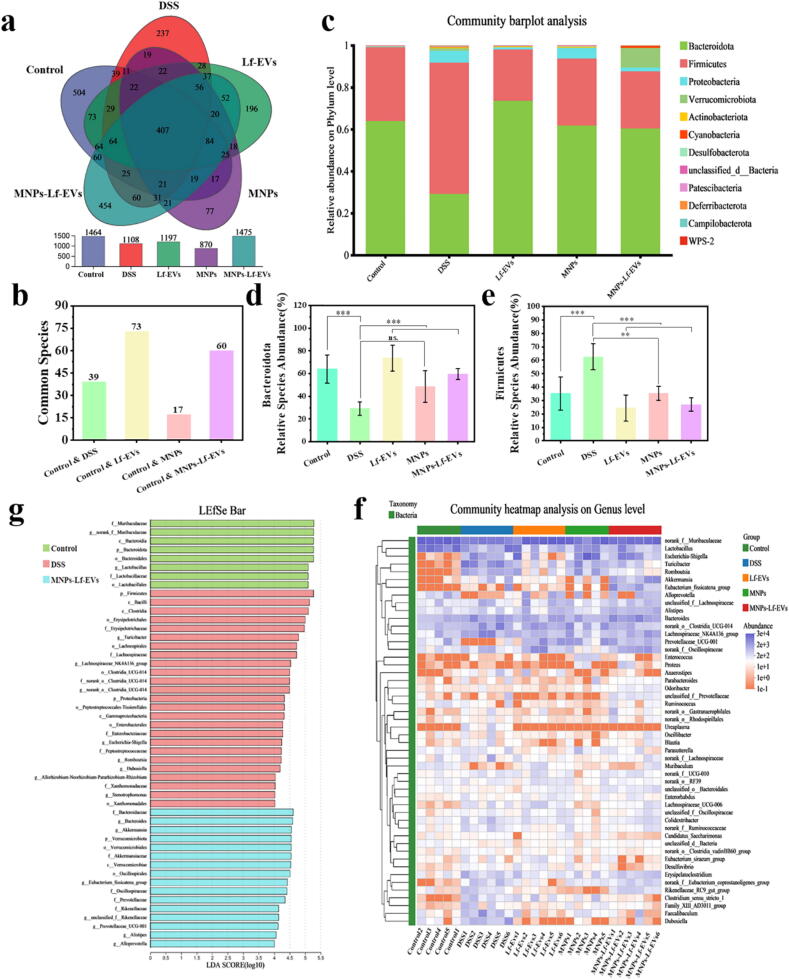
图10A:Venn图分析。结果显示,DSS模型组肠道菌群的OTU数量显著少于正常组;MNPs-Lf-EVs组OTU数量明显增加,与正常组共有物种更多。
图10B:物种共有性统计。结果显示,Lf-EVs组、MNPs-Lf-EVs组与正常组的共有物种数量分别为73、60,显著多于DSS模型组,表明其可恢复肠道有益菌群。
图10C:门水平菌群组成分析。结果显示,DSS模型组拟杆菌门(Bacteroideta)相对丰度显著降低,厚壁菌门(Firmicutes)和变形菌门(Proteobacteria)相对丰度升高;MNPs-Lf-EVs组可逆转该趋势,且疣微菌门(Verrucomicrobiota)相对丰度升高。
图10D:拟杆菌门相对丰度统计。结果显示,MNPs-Lf-EVs组拟杆菌门相对丰度显著高于DSS模型组,接近正常组。
图10E:厚壁菌门相对丰度统计。结果显示,MNPs-Lf-EVs组厚壁菌门相对丰度显著低于DSS模型组,菌群结构更接近正常组。
图10F:属水平菌群热图。结果显示,与DSS模型组相比,MNPs-Lf-EVs组脲原体属(Ureaplasma)相对丰度降低,普雷沃氏菌科(Prevotellaceae)相对丰度升高。
图10G:LEfSe分析。结果显示,MNPs-Lf-EVs组的优势菌群包括拟杆菌属(Bacteroides)、阿里斯特pu氏菌属(Alistipes)、颤螺菌目(Oscillospirales)、普雷沃氏菌科、疣微菌门、阿克曼菌属(Akkermansia)等有益菌群。
这些结果表明,MNPs-Lf-EVs可通过上调有益菌群(如拟杆菌属、阿克曼菌属)相对丰度、下调有害菌群相对丰度,有效调节UC小鼠肠道菌群组成。
11. MNPs-Lf-EVs的体内生物安全性评估
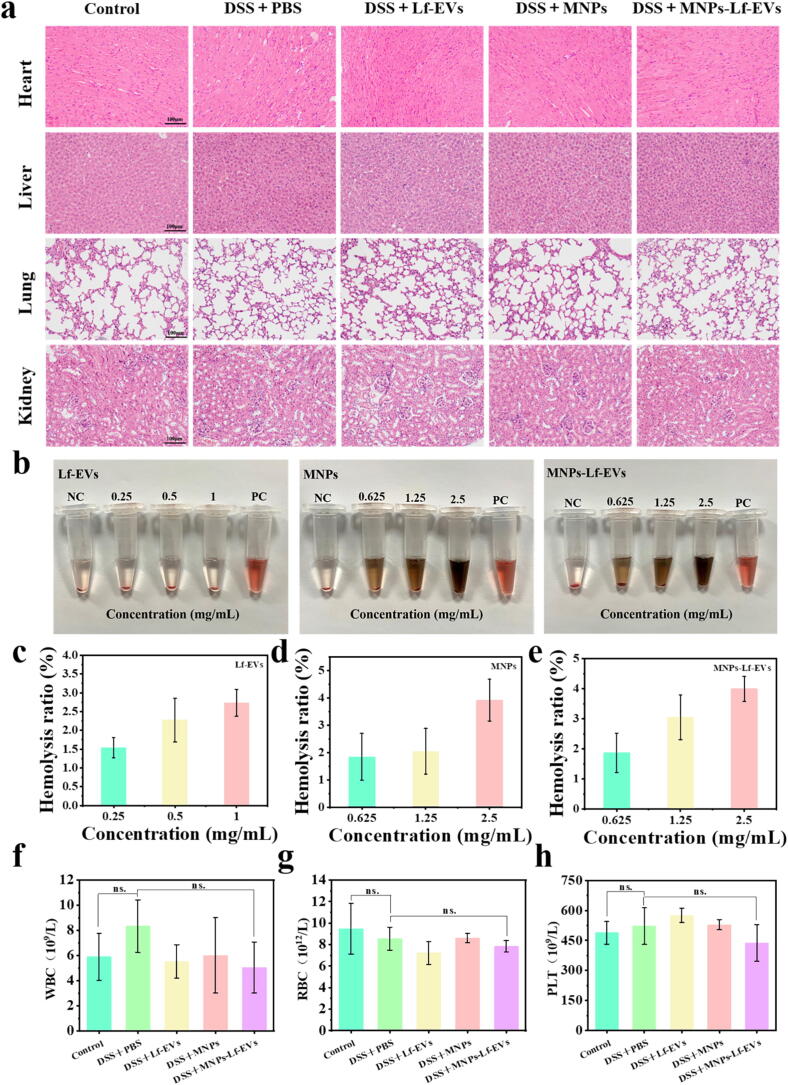
图11A:主要器官HE染色。结果显示,Lf-EVs组、MNPs组、MNPs-Lf-EVs组小鼠的心、肝、脾、肺、肾组织形态正常,无炎性细胞浸润、细胞坏死等病理损伤,与正常组无显著差异。
图11B-E:溶血实验。结果显示,不同浓度的Lf-EVs、MNPs、MNPs-Lf-EVs与红细胞孵育后,红细胞沉淀清晰可见,溶血率均低于5%,表明其无明显溶血毒性。
图11F-H:血常规检测。结果显示,各处理组小鼠的白细胞(WBC)、红细胞(RBC)、血小板(PLT)计数与正常组无显著差异;DSS模型组WBC计数略有升高(与炎症发生相关)。
这些结果表明,MNPs-Lf-EVs在有效治疗剂量下无明显体内毒性,生物相容性良好。
结论
本研究通过超声破碎法成功构建了黑色素纳米颗粒负载发酵乳杆菌外泌体(MNPs-Lf-EVs),该载体整合了Lf-EVs和MNPs的优势:保留了MNPs的优异抗氧化活性和光声成像性能,可通过光声成像实时监测其在体内的动态分布,为治疗方案制定提供指导;Lf-EVs作为载体,不仅保护MNPs免受胃肠道环境破坏、避免其快速代谢清除,还能实现肠道炎症部位的靶向聚集和长效滞留,同时发挥调节肠道菌群的作用。






