研载生物科技(上海)有限公司
9 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
公司新闻/正文
Bioact Mater|告别单一靶点!双外泌体+微流控递送+三重miRNA通路,协同抗炎修复,OA多靶点干预太顶了!
238 人阅读发布时间:2026-03-27 11:53
骨关节炎(OA)是一种慢性退行性关节疾病,以疼痛、活动受限和关节畸形为主要特征,严重影响患者生活质量,全球受累人群超6.5亿,我国约有1.32亿患者。OA病理机制复杂,涉及慢性炎症、合成代谢抑制、软骨退变等多重微环境紊乱,单一治疗手段难以实现全面的软骨保护功能。近年来,生物治疗在OA领域备受关注,但现有研究多聚焦于单一靶点,疗效不尽如人意。骨髓间充质基质细胞(BMSCs)和软骨祖细胞(CPCs)作为两种具有修复潜力的细胞,分别在抗炎调节和软骨生成方面展现出独特优势,其分泌的外泌体(Exo)继承了亲本细胞的核心生物学功能,且无直接细胞移植的免疫原性和致瘤性风险。

今天分享的是发表在【Bioact Mater】(IF:20.3)上题为“Harnessing bi-exosome combination alleviates osteoarthritis progression”的研究。该研究基于两种外泌体的功能差异,提出“双外泌体组合”策略,将抗炎导向的BMSC来源外泌体(B-Exo)与抗分解代谢导向的CPC来源外泌体(C-Exo)联合,通过透明质酸甲基丙烯酰微球递送至关节腔,同时调控巨噬细胞极化和软骨细胞表型,为OA治疗提供新型多靶点干预方案。
研究思路
首先通过RNA测序鉴定B-Exo和C-Exo的miRNA富集特征,明确二者分别侧重巨噬细胞调控和软骨细胞调节的功能差异;随后在体外验证两种外泌体单独及联合使用对软骨细胞(CCs)和骨髓来源巨噬细胞(BMDMs)的作用,优化组合比例;接着利用微流控技术构建负载双外泌体(BC-Exo)的透明质酸甲基丙烯酰(HAMA)微球,表征其理化性质、缓释效果及生物安全性;在OA大鼠模型中评估该递送系统的体内治疗效果,包括疼痛缓解、关节功能改善、软骨保护及炎症抑制;最后通过转录组分析结合miRNA靶点验证,揭示双外泌体组合缓解OA进展的核心分子通路,为其临床应用提供理论支撑。
研究结果
1、B-Exo与C-Exo的miRNA富集特征对比
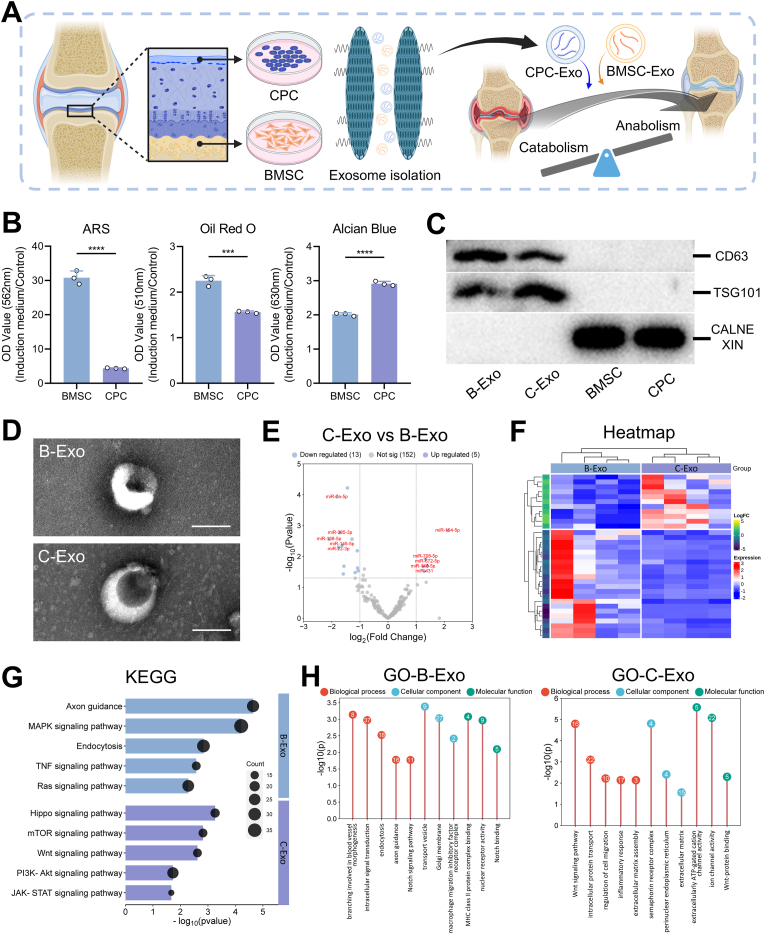
图1A:研究假设示意图,提出B-Exo(抗炎)与C-Exo(抗分解代谢)联合通过多靶点调控缓解OA进展。
图1B:BMSCs和CPCs的成骨、成脂、成软骨分化定量分析,BMSCs成骨和成脂能力分别为CPCs的7.04倍和1.44倍,CPCs成软骨能力为BMSCs的1.45倍。
图1C:Western blot检测显示,B-Exo和C-Exo均高表达外泌体标志物CD63、TSG101,不表达钙连蛋白CALNEXIN(细胞杂质标志物)。
图1D:透射电镜(TEM)显示,B-Exo和C-Exo均呈典型结构。
图1E:火山图显示,与B-Exo相比,C-Exo中有18个miRNA差异表达,其中5个上调、13个下调。
图1F:热图展示B-Exo与C-Exo中差异表达miRNA的具体分布特征。
图1G:KEGG通路分析显示,B-Exo富集miRNA的靶基因主要涉及MAPK、TNF等炎症相关通路,C-Exo富集miRNA的靶基因则关联Hippo、mTOR等软骨代谢相关通路。
图1H:GO富集分析显示,B-Exo相关miRNA参与巨噬细胞迁移抑制、MHCⅡ类蛋白复合物结合等功能,C-Exo相关miRNA涉及细胞外基质(ECM)组织、炎症反应调控等过程。
这些结果表明,B-Exo和C-Exo具有不同的miRNA富集特征,分别倾向于调控炎症反应和软骨细胞代谢,为二者联合应用提供了分子基础。
2、B-Exo与C-Exo对体外培养CCs和BMDMs的作用分析
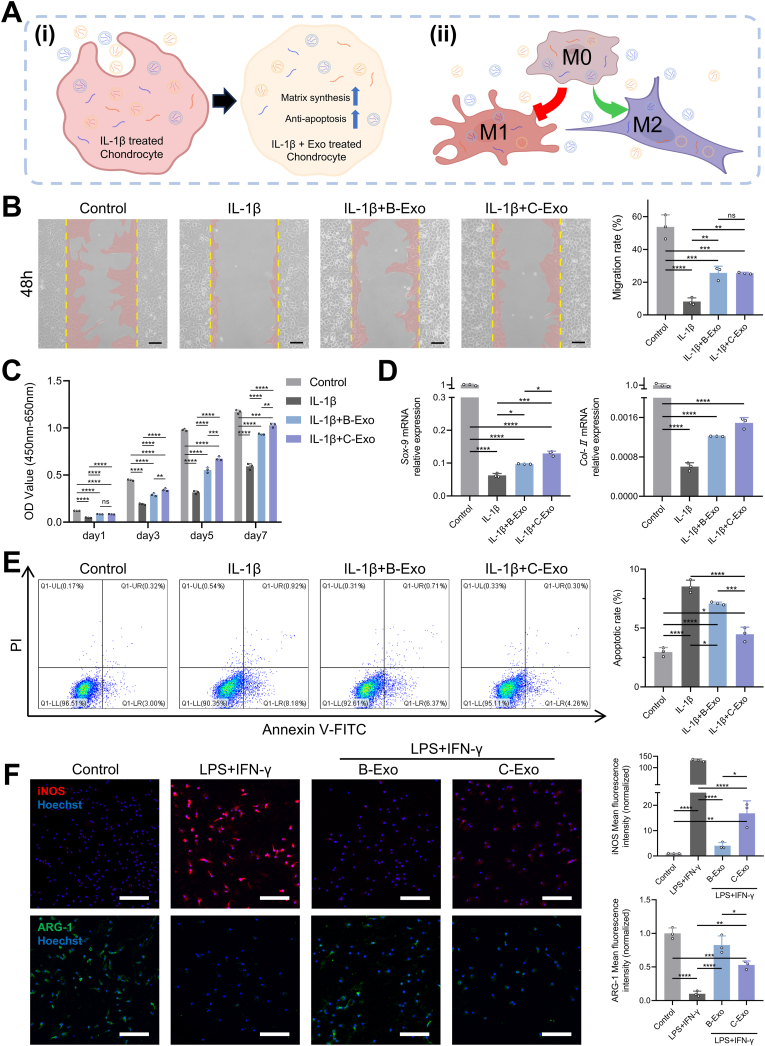
图2A:实验示意图,分别用促炎因子联合外泌体处理CCs(i)和BMDMs(ii)。
图2B:细胞迁移实验显示,IL-1β诱导后CCs迁移能力下降,B-Exo和C-Exo处理均能显著提升迁移率。
图2C:CCK-8实验显示,C-Exo处理组CCs增殖活性在培养3-7天均显著高于B-Exo组。
图2D:qRT-PCR显示,IL-1β诱导后CCs中Sox-9和Col-Ⅱ基因表达降低,C-Exo处理后二者转录水平分别比B-Exo组高33.31%和22.21%。
图2E:流式细胞术显示,IL-1β诱导CCs凋亡率从2.97%升至8.53%,C-Exo组凋亡率(4.47%)显著低于B-Exo组(7.09%)。
图2F:免疫荧光染色显示,LPS+IFN-γ诱导后,B-Exo组iNOS⁺(M1标志物)巨噬细胞数量显著减少,ARG-1⁺(M2标志物)巨噬细胞数量显著增加,效果优于C-Exo组。
这些结果表明,C-Exo在促进软骨细胞增殖、ECM合成及抑制凋亡方面更具优势,而B-Exo在调控巨噬细胞向抗炎M2表型极化方面效果更显著。
3、双外泌体组合(BC-Exo)在体外对CCs保护及BMDMs极化的调控作用
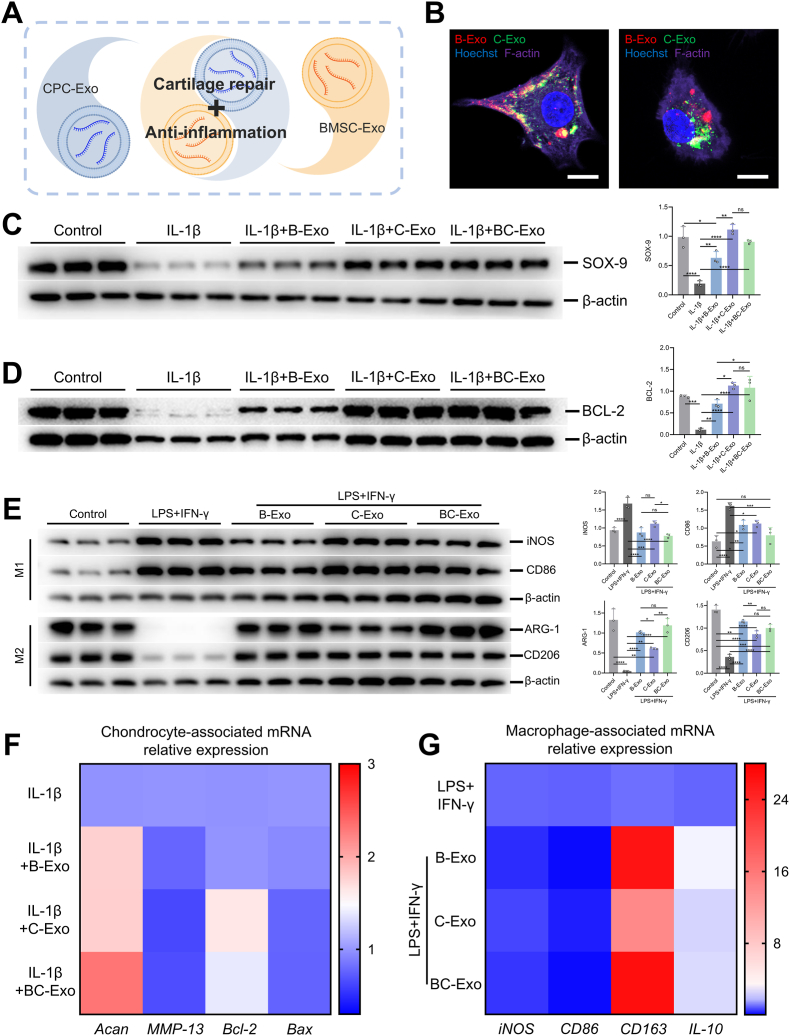
图3A:BC-Exo组合效应示意图,展示其整合B-Exo抗炎功能与C-Exo软骨保护功能的协同作用。
图3B:共聚焦成像显示,DiI标记的B-Exo(红色)和DiO标记的C-Exo(绿色)均能被CCs和BMDMs有效摄取。
图3C:Western blot显示,IL-1β诱导后CCs中SOX-9蛋白表达降低,BC-Exo处理组SOX-9水平显著高于B-Exo组,仅低于C-Exo组。
图3D:Western blot显示,C-Exo和BC-Exo处理组CCs中抗凋亡蛋白BCL-2表达显著上调,分别比B-Exo组高58.58%和51.5%。
图3E:Western blot显示,LPS+IFN-γ诱导后,B-Exo和BC-Exo组巨噬细胞中iNOS、CD86(M1标志物)蛋白表达显著降低,ARG-1、CD206(M2标志物)蛋白表达显著升高,效果优于C-Exo组。
图3F:qRT-PCR显示,BC-Exo组CCs中Acan基因表达分别为B-Exo组的1.31倍和C-Exo组的1.29倍,MMP-13(分解代谢标志物)基因表达显著降低。
图3G:qRT-PCR显示,BC-Exo组巨噬细胞中CD86基因表达显著降低,CD163、IL-10(M2相关细胞因子)基因表达显著升高,与B-Exo组效果相当。
这些结果表明,BC-Exo整合了B-Exo的抗炎优势和C-Exo的软骨保护功能,在体外炎症微环境中对CCs和BMDMs的调控效果优于单一外泌体。
4、外泌体负载HAMA微球(Exo-MS)的制备及体内抗OA效果评估
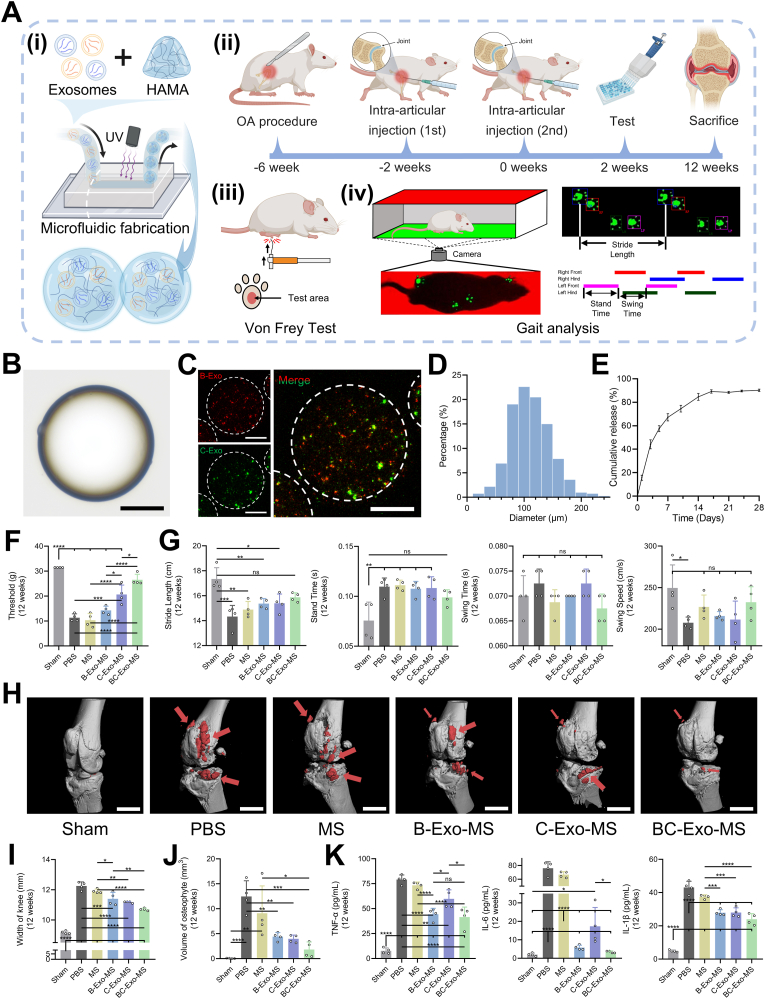
图4A:实验流程示意图,包括Exo-MS制备(i)、OA大鼠模型建立与给药方案(ii)、机械痛阈测试(iii)和步态分析(iv)。
图4B:明场显微镜显示,Exo-MS在油相中的形态完整。
图4C:共聚焦成像显示,DiI标记的B-Exo和DiO标记的C-Exo在微球内均匀分布,白色虚线为微球边界。
图4D:尺寸分布分析显示,Exo-MS平均直径为111±35μm。
图4E:体外释放曲线显示,Exo-MS呈现双相释放特征,前5天为快速释放期(释放超50%),随后进入缓慢缓释期,14天释放趋于平稳。
图4F:Von Frey测试显示,12周时BC-Exo-MS组大鼠后爪机械痛阈(26.54g)显著高于B-Exo-MS(14.27g)和C-Exo-MS(20.66g)组。
图4G:步态分析显示,BC-Exo-MS组大鼠步长更长、站立时间更短,关节活动功能改善更显著。
图4H:μCT成像显示,BC-Exo-MS组大鼠膝关节骨赘形成显著少于其他处理组。
图4I:膝关节宽度测量显示,BC-Exo-MS组关节肿胀程度显著轻于B-Exo-MS、C-Exo-MS组及对照组。
图4J:骨赘体积定量分析显示,BC-Exo-MS组骨赘体积显著小于B-Exo-MS和C-Exo-MS组。
图4K:ELISA显示,BC-Exo-MS组大鼠关节滑液中TNF-α、IL-6、IL-1β水平显著低于C-Exo-MS组,与B-Exo-MS组相当。
这些结果表明,Exo-MS具有良好的形态特征和缓释性能,BC-Exo-MS在体内能显著缓解OA大鼠的疼痛、改善关节功能、抑制骨赘形成和炎症反应。
5、关节组织学变化分析
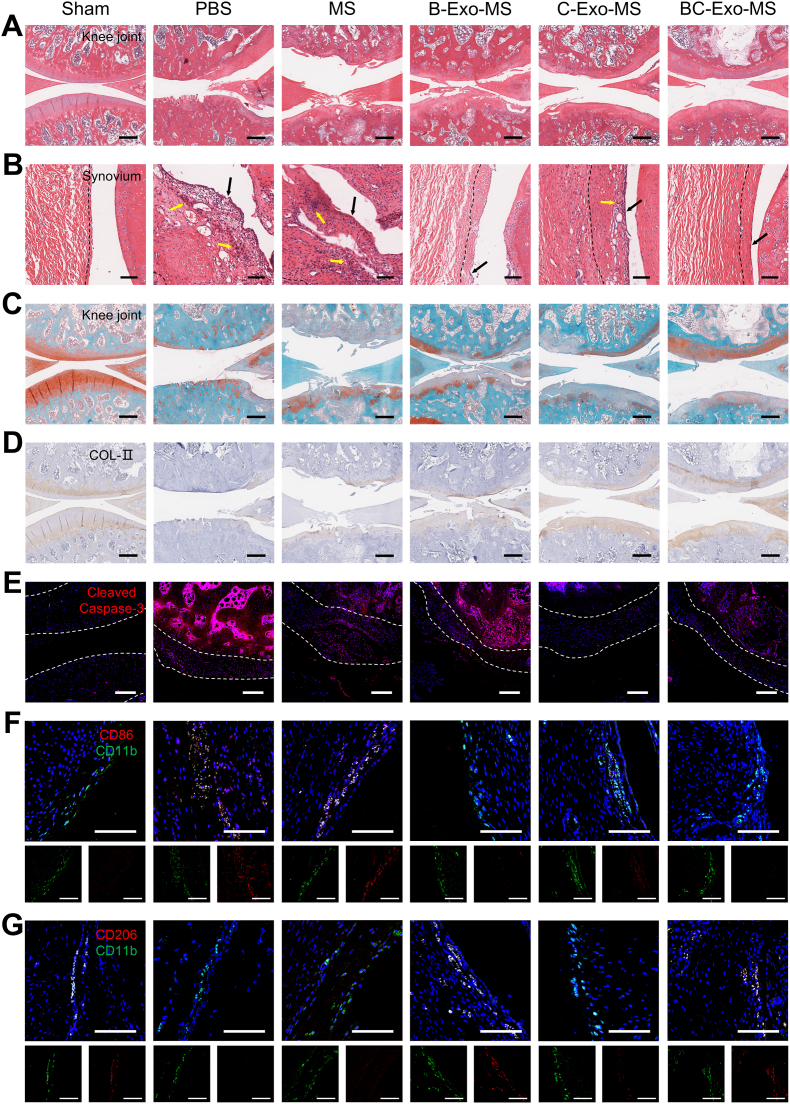
图5A:HE染色显示,BC-Exo-MS组关节软骨表面相对光滑、结构完整,损伤程度显著轻于其他处理组。
图5B:HE染色显示,PBS和MS组滑膜衬里层增厚、细胞密度增加,B-Exo-MS和BC-Exo-MS组滑膜炎症显著缓解。
图5C:番红O-固绿染色显示,BC-Exo-MS组软骨基质染色强度较高,OARSI评分显著低于其他处理组。
图5D:IHC染色显示,BC-Exo-MS组软骨组织中COL-Ⅱ表达强度显著高于B-Exo-MS组。
图5E:免疫荧光染色显示,BC-Exo-MS组软骨细胞中凋亡标志物Cleaved Caspase-3荧光强度显著低于B-Exo-MS组。
图5F:免疫荧光染色显示,BC-Exo-MS组滑膜中CD11b⁺CD86⁺(M1型)巨噬细胞数量显著减少。
图5G:免疫荧光染色显示,BC-Exo-MS组滑膜中CD11b⁺CD206⁺(M2型)巨噬细胞数量显著增加。
这些结果表明,BC-Exo-MS能有效减轻OA大鼠的滑膜炎症、保护软骨基质完整性、抑制软骨细胞凋亡,组织学改善效果优于单一外泌体处理。
6、BC-Exo缓解OA进展的分子机制探究
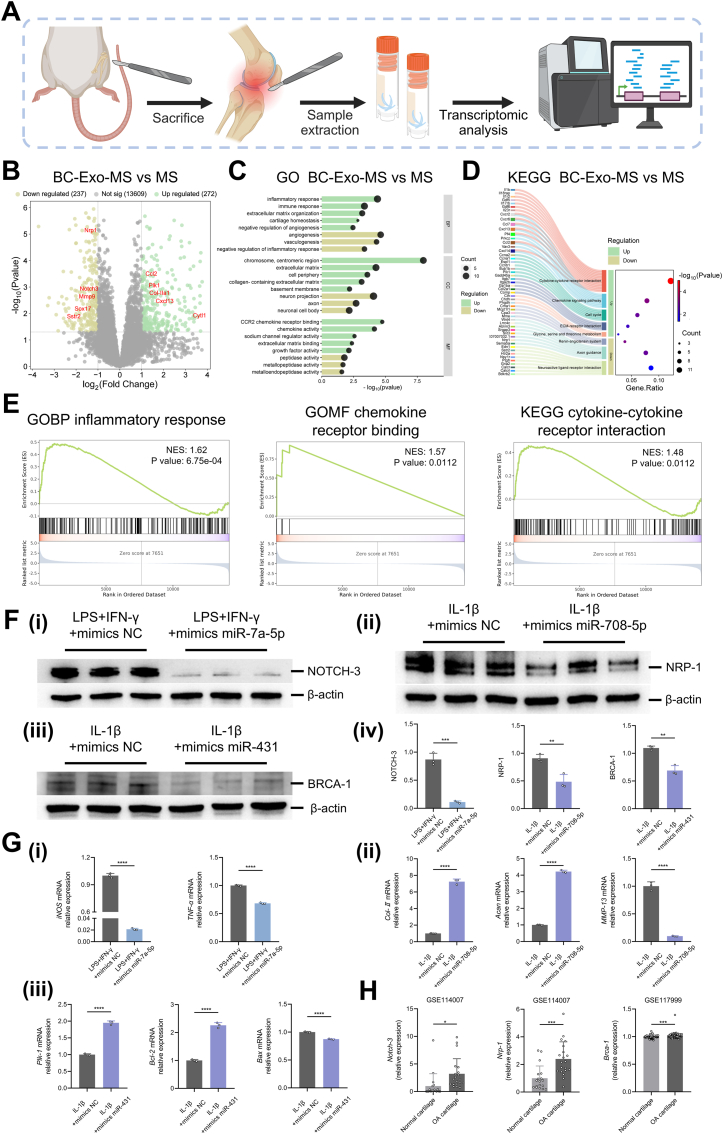
图6A:大鼠膝关节软骨区域组织转录组分析流程示意图。
图6B:火山图显示,BC-Exo-MS组与MS组相比,共有272个基因上调、237个基因下调,涉及炎症调控和软骨修复相关基因。
图6C:GO富集分析显示,上调基因主要参与ECM合成、软骨稳态调控等过程,下调基因涉及金属肽酶表达、病理性血管生成等功能。
图6D:KEGG通路分析显示,BC-Exo-MS组富集了细胞因子-受体相互作用、ECM-受体相互作用等通路。
图6E:GSEA分析显示,BC-Exo-MS组在炎症反应、趋化因子受体结合等过程中显著富集。
图6F:Western blot显示,转染miR-7a-5p mimic后,BMDMs中NOTCH-3蛋白表达降低87.18%(i)。转染miR-708-5p mimic后,CCs中NRP-1蛋白表达降低46.57%(ii)。转染miR-431 mimic后,CCs中BRCA-1蛋白表达降低1.59倍(iii)。内参蛋白β-actin表达水平(iv)。
图6G:qRT-PCR显示,miR-7a-5p mimic转染后,BMDMs中iNOS和TNF-α基因表达分别降低97.87%和31.69%(i)。miR-708-5p mimic转染后,CCs中Col-Ⅱ和Acan基因表达升高超4倍,MMP-13基因表达降低超10倍(ii)。miR-431 mimic转染后,CCs中Plk-1和Bcl-2基因表达分别升高1.95倍和显著上调,Bax基因表达降低(iii)。
图6H:公共数据集(GSE114007、GSE117999)分析显示,人OA软骨中Notch-3、Nrp-1、Brca-1基因表达均显著高于正常软骨。
这些结果表明,BC-Exo通过B-Exo中的miR-7a-5p/NOTCH-3通路抑制炎症,通过C-Exo中的miR-708-5p/NRP-1通路促进软骨修复、miR-431/BRCA-1/PLK-1通路抑制软骨细胞凋亡,共同发挥抗OA作用。
结论
本研究明确了B-Exo和C-Exo在miRNA富集特征和生物学功能上的差异,提出并验证了双外泌体组合(BC-Exo)的协同治疗价值。通过微流控技术构建的BC-Exo负载HAMA微球,实现了外泌体的缓释递送和关节内长效滞留,且生物安全性良好。体内外实验证实,BC-Exo能整合B-Exo的抗炎优势(调控巨噬细胞M2极化)和C-Exo的软骨保护功能(促进ECM合成、抑制软骨细胞凋亡),通过miR-7a-5p/NOTCH-3、miR-708-5p/NRP-1及miR-431/BRCA-1/PLK-1三条核心通路,多靶点改善OA关节的炎症微环境和软骨退变,显著缓解疼痛、改善关节功能。该研究为OA的多靶点治疗提供了创新策略,也为外泌体组合疗法的临床转化奠定了基础。






