研载生物科技(上海)有限公司
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
IRE1A刺激肝细胞来源的细胞外囊泡,促进脂肪性肝炎的小鼠炎症
1026 人阅读发布时间:2021-05-31 09:56
【关键词】内质网应激、外泌体、脂质毒性、巨噬细胞

【摘要】内质网至细胞核信号传导1(IRE1A)蛋白在非酒精性脂肪性肝炎(NASH)患者的肝脏中被激活,IRE1A激活后,干细胞释放富含神经酰胺的炎性细胞外囊泡(EVs),因此本文研究抑制IRE1A对饮食诱发的脂肪性肝炎小鼠炎性EVs释放的影响。构建模型鼠后,富强内注射IRE1A抑制剂或腺病毒转染小鼠肝脏和原代干细胞,收集后分离EVs进行检测。肝细胞中Ire1a破坏后EVs释放减少,肝损伤、炎症、巨噬细胞局部积累减少。IRE1A靶向编码神经酰胺合成限速酶,导致神经酰胺的生物合成和释放,从而影响EVs的分泌,导致脂肪性肝炎的小鼠肝脏受损。
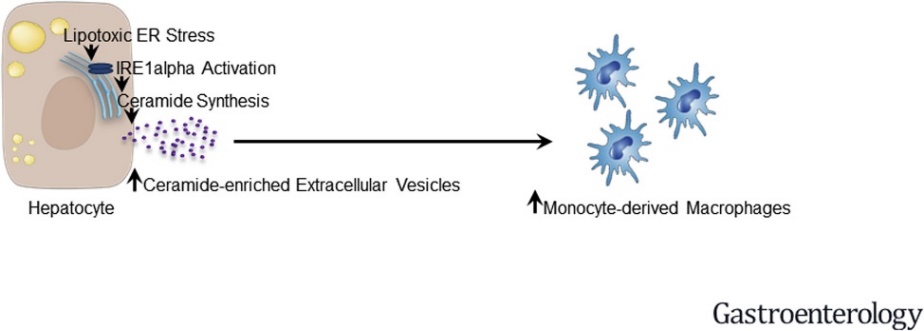
【前言】非酒精性脂肪肝疾病(NAFLD)特征是肝细胞损伤,被认为是气球样变形和炎症,伴有纤维化,目前缺乏有效的治疗药物。NASH是众多信号通路之间相互作用的结果,包括遗传易感性、肠道营养不良、饮食摄入和脂质代谢异常,进而导致脂质毒性和炎症反应。内质网应激是脂毒性亚致死应激的重要表现,多项研究表明IRE1A-XBP1信号传导与NAFLD的胰岛素抵抗,血脂异常,肝脂肪变性,炎症相关。先前研究中,IRE1A对于从细胞中释放EVs是必须的,而EVs作为介导细胞间相互作用是必须的。目前IRE1A刺激的EVs在NASH中的作用仍然有待研究。
【结果】
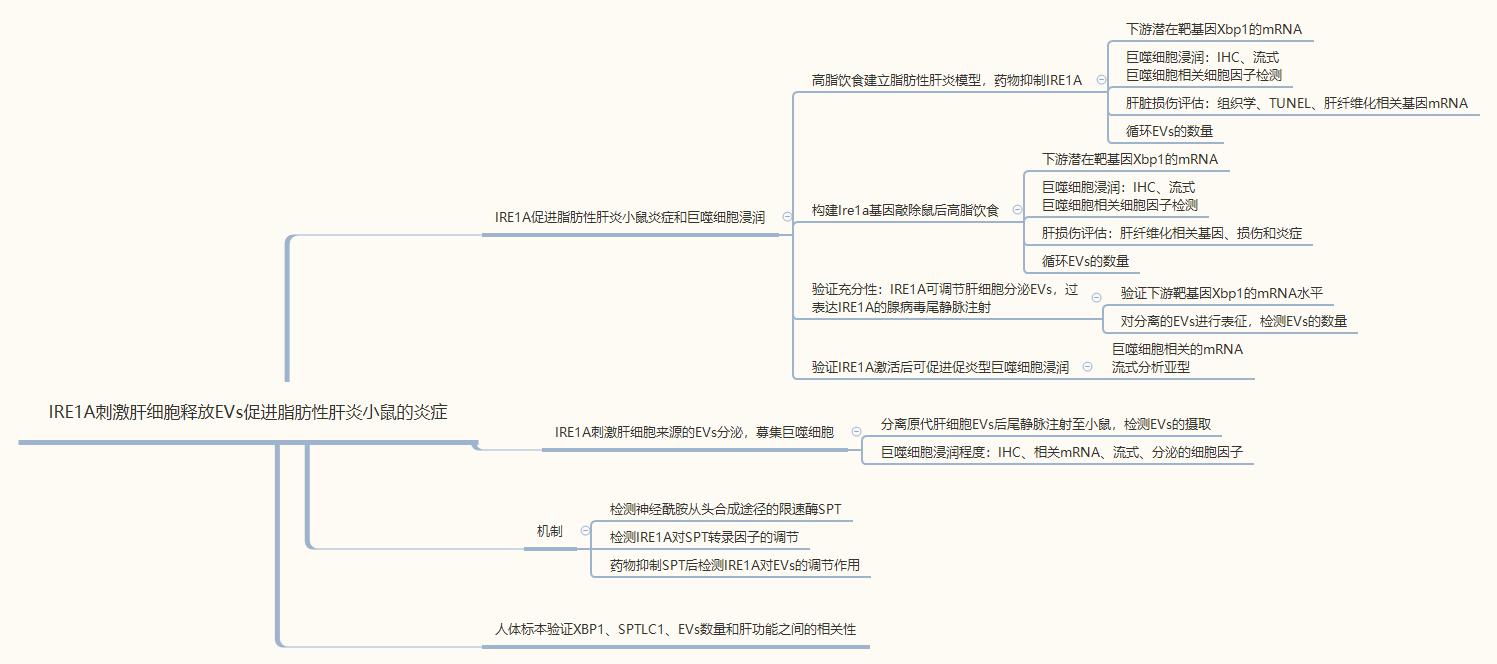
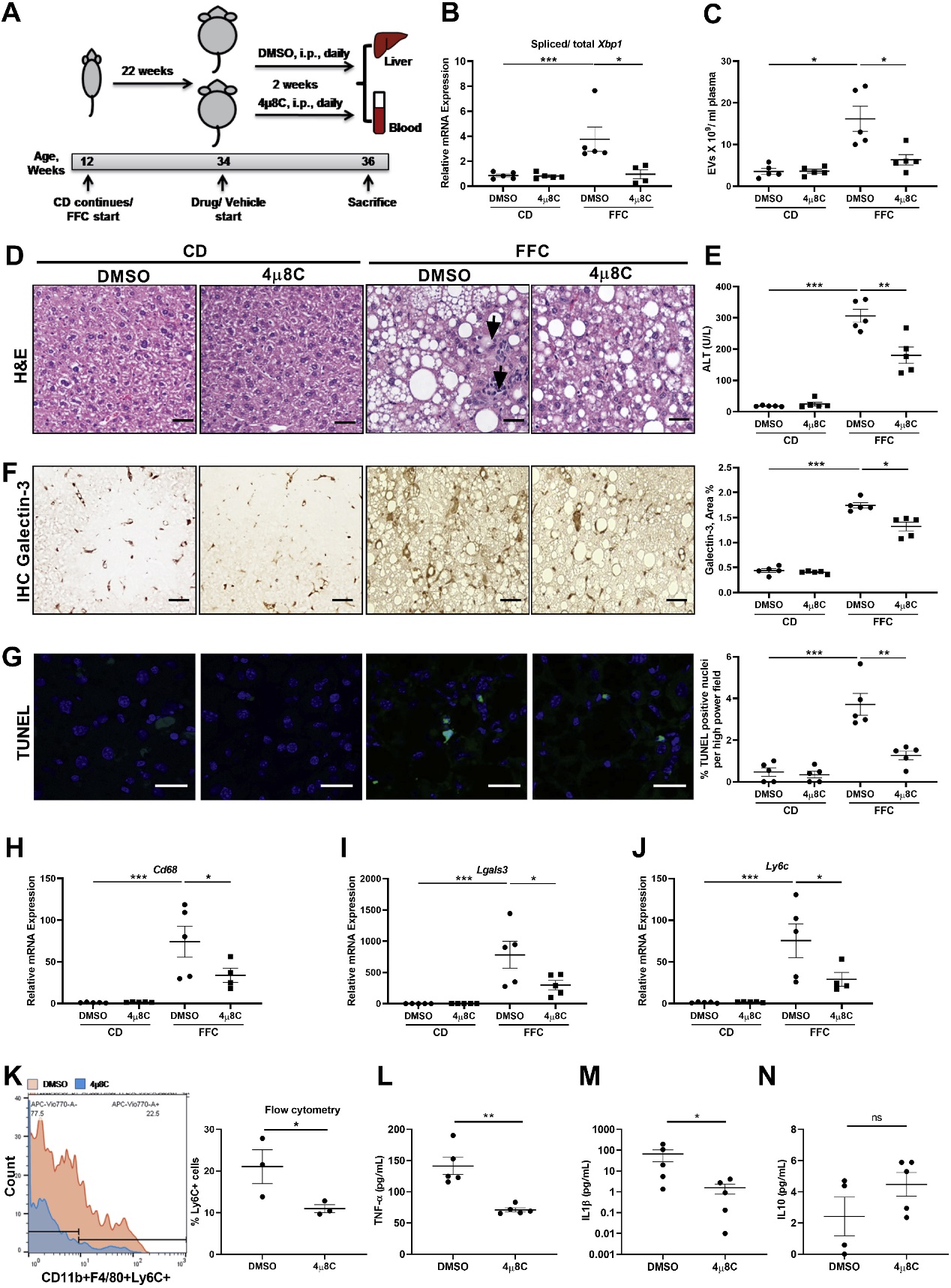
NASH中存在脂毒性ER应激反应的激活。构建NASH小鼠模型,用IRE1A抑制剂处理模型鼠后检测Xbp1表达,组织学评估肝脏损伤,IHC和流式检测巨噬细胞浸润,检测巨噬细胞相关mRNA以及释放的因子,TUNEL检测肝细胞凋亡,检测肝脏纤维化相关指标。结果表明:IRE1A抑制剂可减少巨噬细胞浸润,减少肝脏损伤。
构建Ire1a基因敲除鼠,重复上述步骤,检测Xbp1的mRNA,EVs数量,肝功能,巨噬细胞浸润,肝脏纤维化等指标。
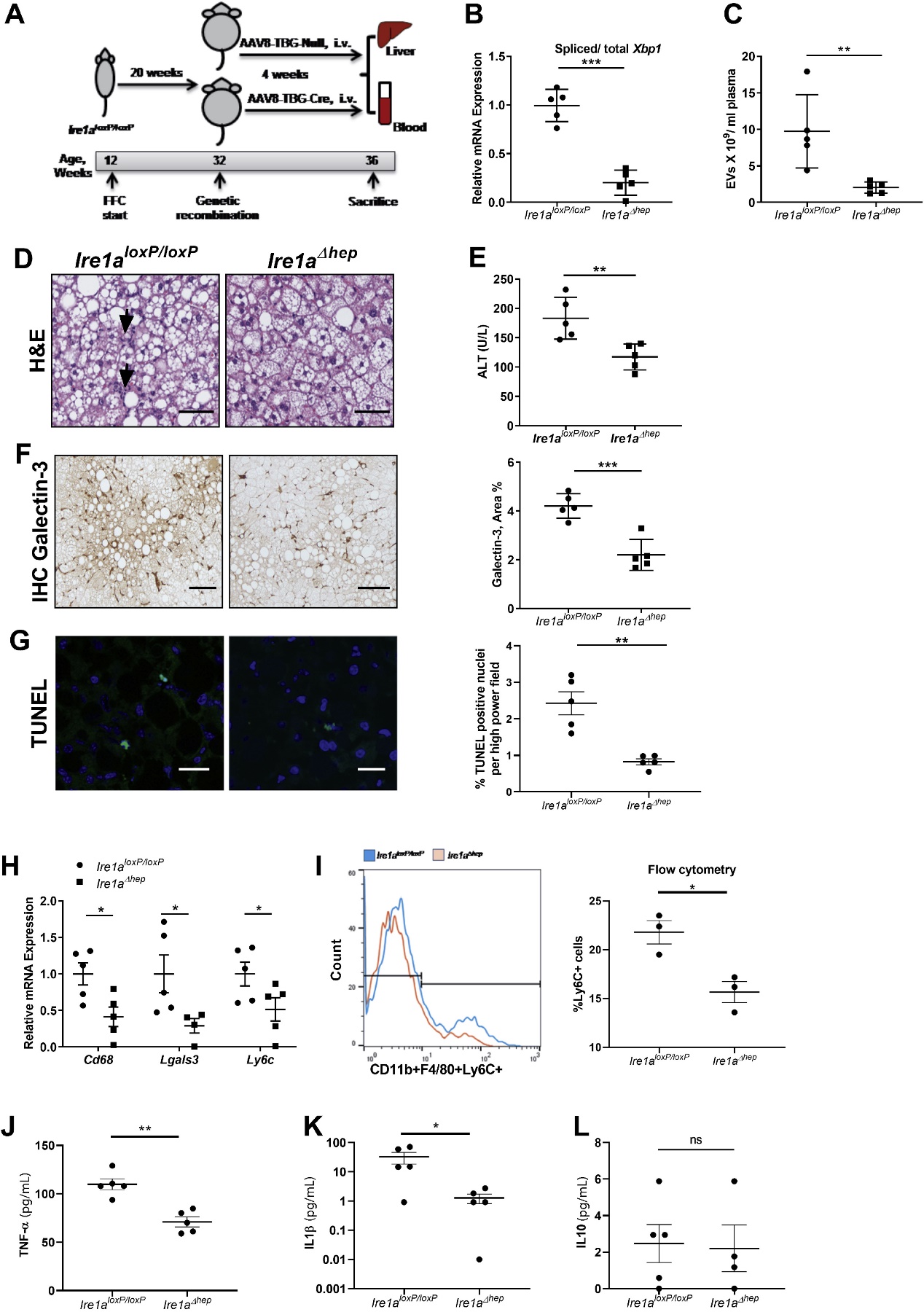
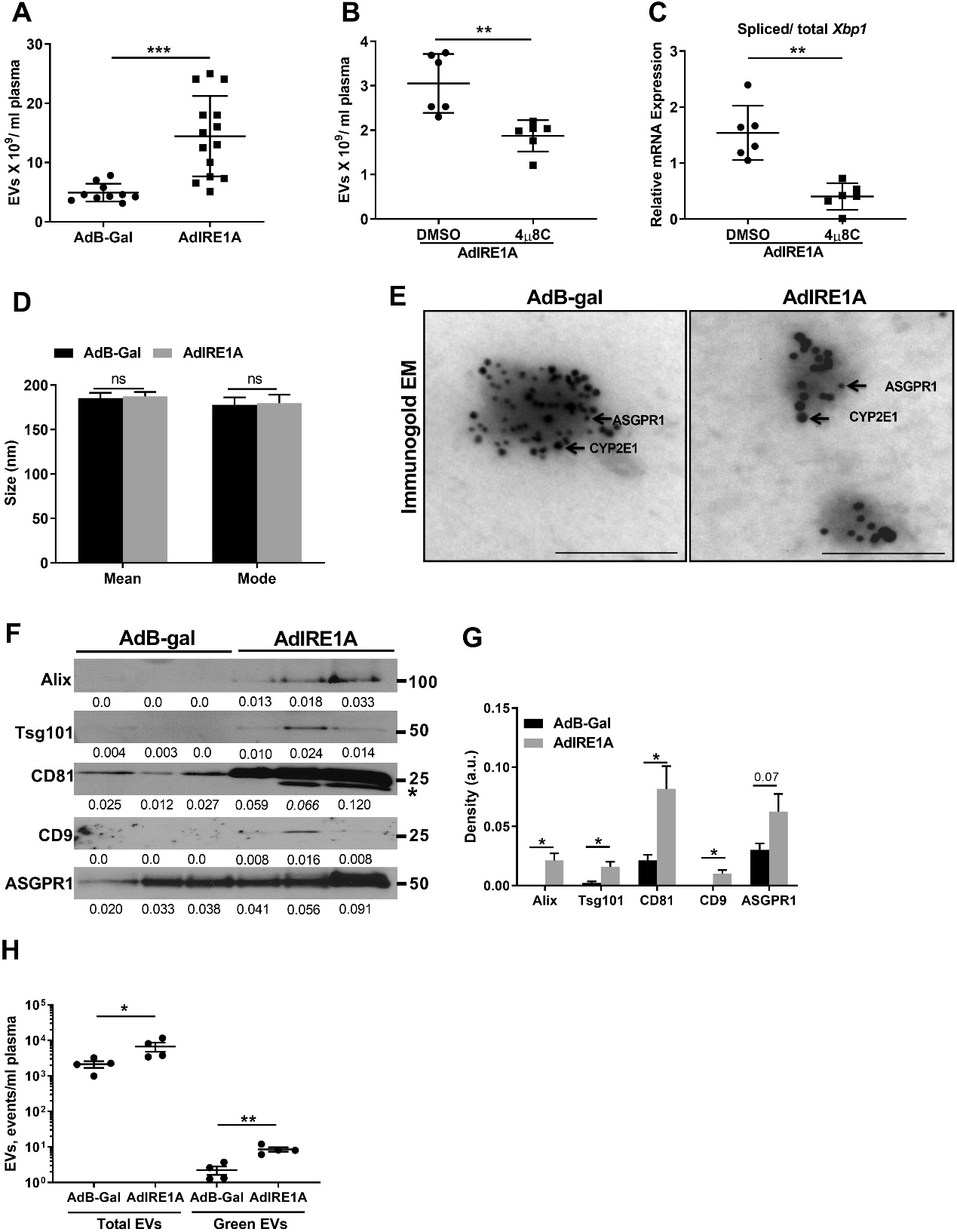
IRE1A抑制后循环EVs的数量也相应减少,表明IRE1A可调控肝细胞释放EVs。小鼠注射过表达IRE1A的腺病毒,检测EVs的数量和Xbp1的mRNA表达量,IRE1A抑制剂、IRE1A的RNase做rescue实验验证。对EVs进行表征,检测不同处理状态下的数量。
IRE1A可促进巨噬细胞的募集,诱导肝损伤。腺病毒转染的过表达IRE1A小鼠中IHC和流式分别检测巨噬细胞浸润,检测巨噬细胞相关mRNA和细胞因子表达,进一步流式检测分析髓样细胞来源的巨噬细胞亚型。结果表明:IRE1A可促进促炎型巨噬细胞浸润至肝脏。
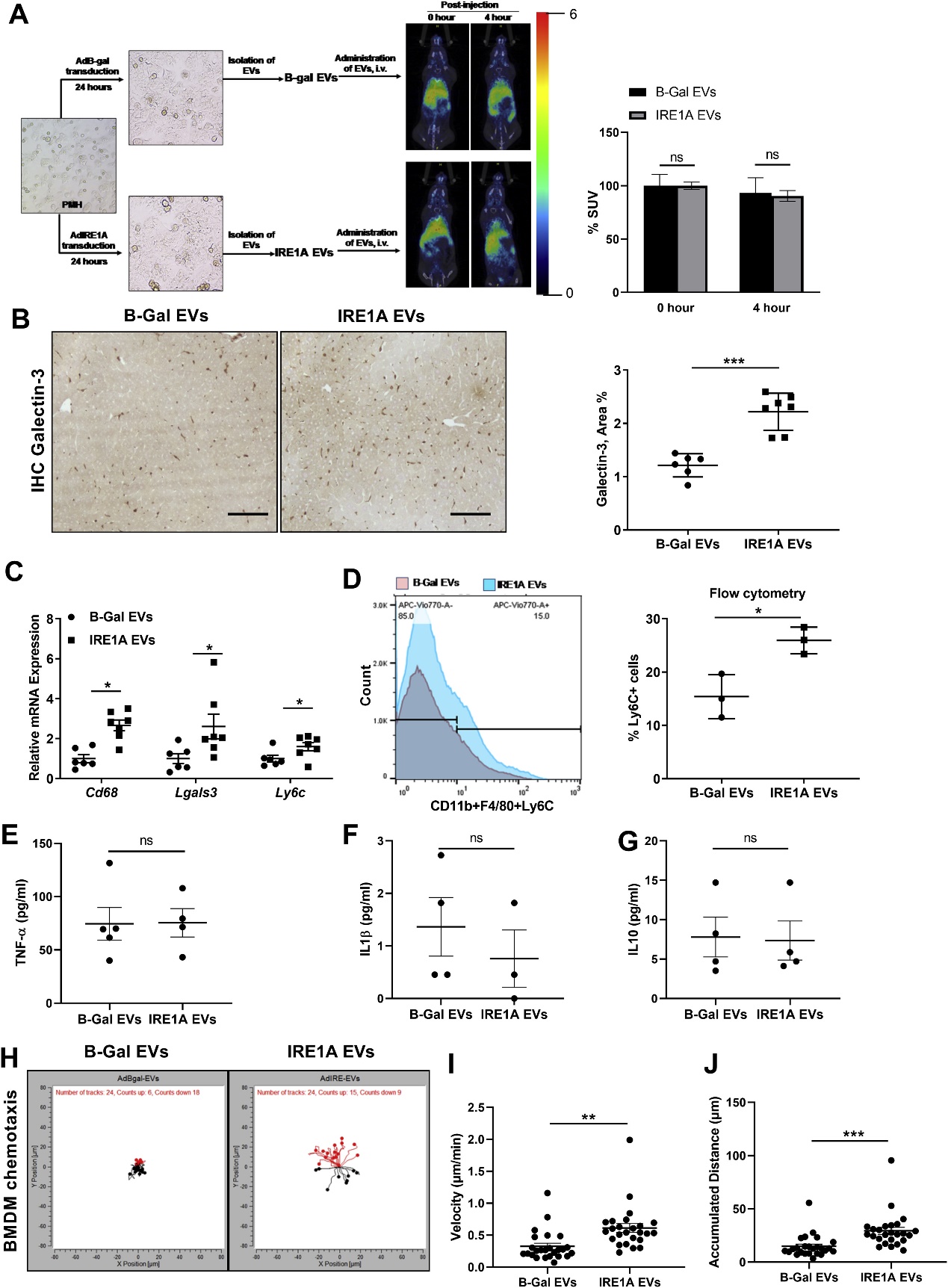
IRE1A刺激原代小鼠肝细胞并分离EVs后尾静脉注射进小鼠体内,检测EVs的数量和肝脏对EVs的摄取情况,巨噬细胞浸润情况。结果表明:IRE1A肝细胞来源的EVs可促进巨噬细胞浸润至肝脏,并且展现出促炎表型。
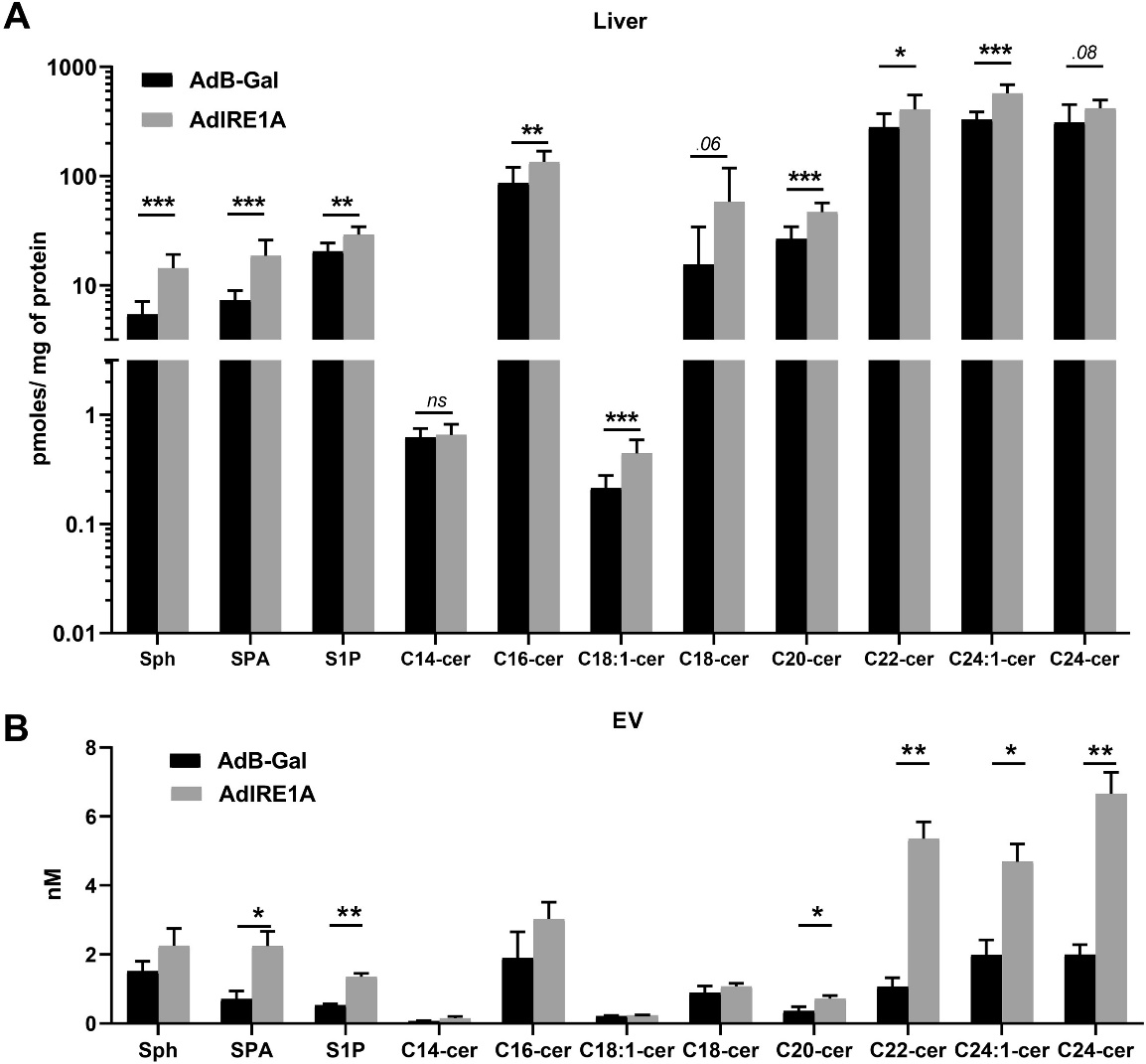
探究IRE1A对EVs释放的调控机制。之前的研究中,脂毒性EVs的释放取决于神经酰胺的从头合成,因此研究IRE1A对神经酰胺从头合成途径的影响。
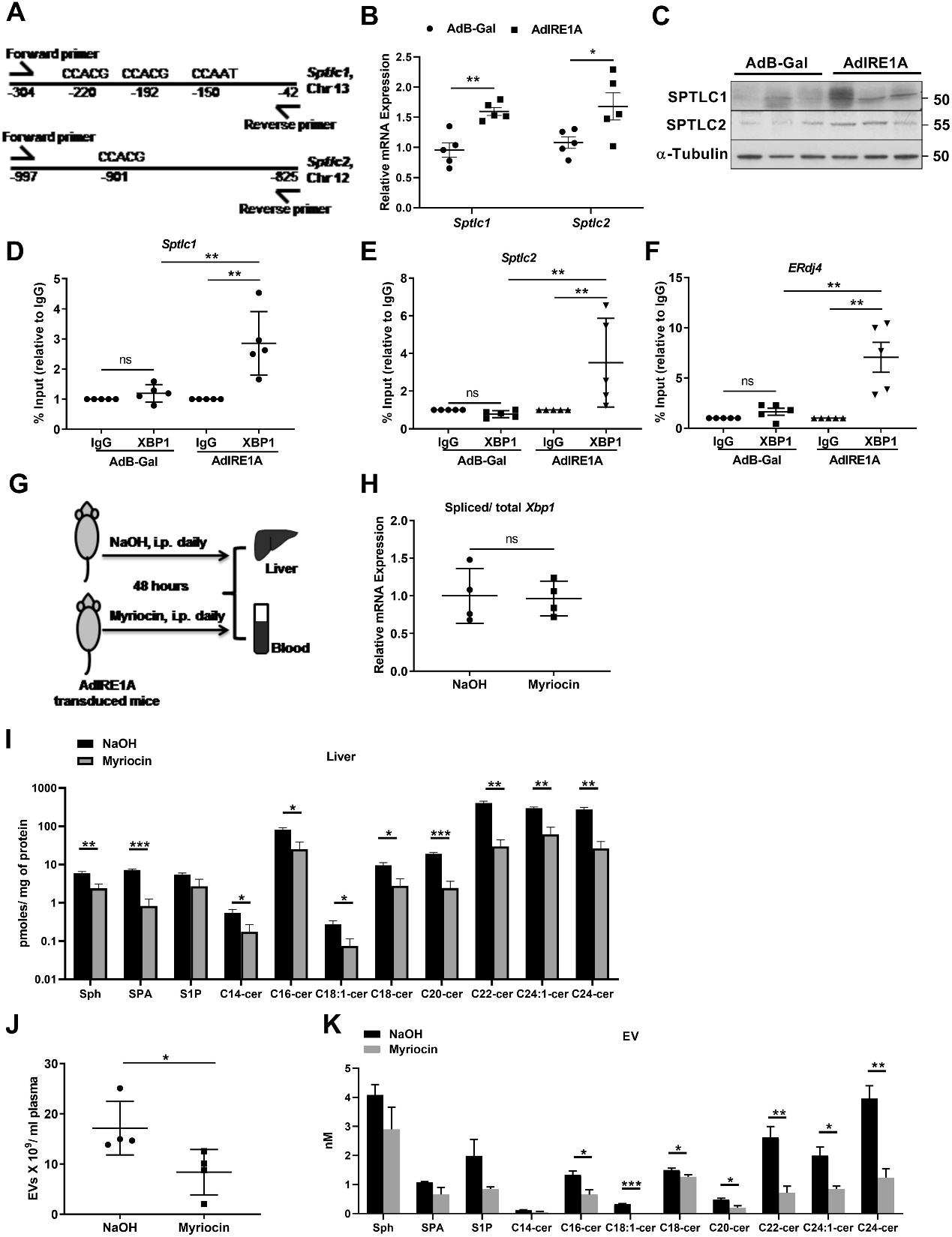
SPT催化神经酰胺合成的限速酶,因此ChIP实验从转录水平研究IRE1A对SPT的调节。SPT抑制剂抑制神经酰胺合成后检测EVs的数量进一步验证:神经酰胺合成途径对于EVs释放是重要的,而IRE1A可调节神经酰胺合成来调节EVs的合成。
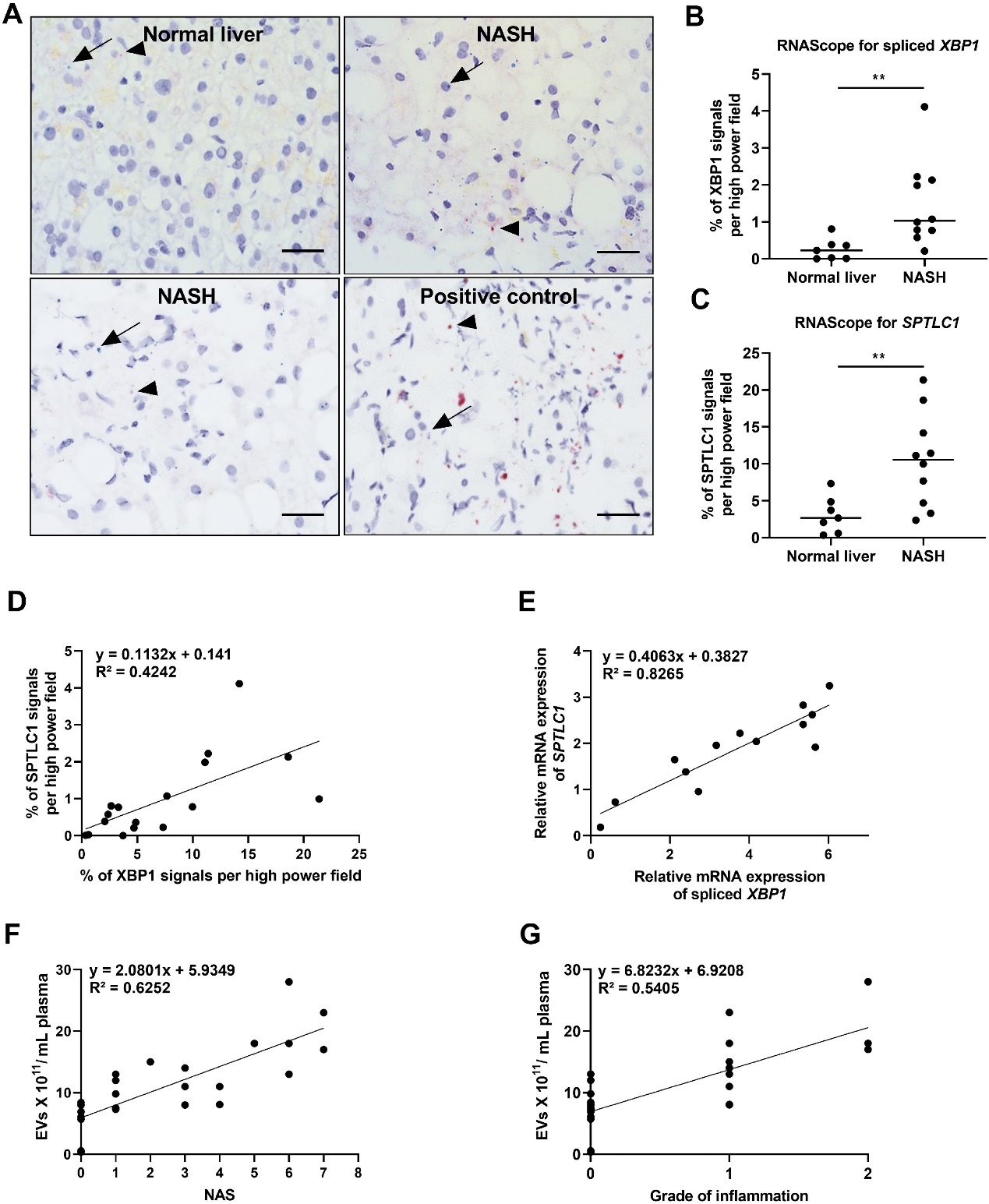
在人类肝脏样本中验证XBP1和SPTLC1与炎症、EVs的数量之间的相关性。

【摘要】内质网至细胞核信号传导1(IRE1A)蛋白在非酒精性脂肪性肝炎(NASH)患者的肝脏中被激活,IRE1A激活后,干细胞释放富含神经酰胺的炎性细胞外囊泡(EVs),因此本文研究抑制IRE1A对饮食诱发的脂肪性肝炎小鼠炎性EVs释放的影响。构建模型鼠后,富强内注射IRE1A抑制剂或腺病毒转染小鼠肝脏和原代干细胞,收集后分离EVs进行检测。肝细胞中Ire1a破坏后EVs释放减少,肝损伤、炎症、巨噬细胞局部积累减少。IRE1A靶向编码神经酰胺合成限速酶,导致神经酰胺的生物合成和释放,从而影响EVs的分泌,导致脂肪性肝炎的小鼠肝脏受损。


【前言】非酒精性脂肪肝疾病(NAFLD)特征是肝细胞损伤,被认为是气球样变形和炎症,伴有纤维化,目前缺乏有效的治疗药物。NASH是众多信号通路之间相互作用的结果,包括遗传易感性、肠道营养不良、饮食摄入和脂质代谢异常,进而导致脂质毒性和炎症反应。内质网应激是脂毒性亚致死应激的重要表现,多项研究表明IRE1A-XBP1信号传导与NAFLD的胰岛素抵抗,血脂异常,肝脂肪变性,炎症相关。先前研究中,IRE1A对于从细胞中释放EVs是必须的,而EVs作为介导细胞间相互作用是必须的。目前IRE1A刺激的EVs在NASH中的作用仍然有待研究。
【结果】
NASH中存在脂毒性ER应激反应的激活。构建NASH小鼠模型,用IRE1A抑制剂处理模型鼠后检测Xbp1表达,组织学评估肝脏损伤,IHC和流式检测巨噬细胞浸润,检测巨噬细胞相关mRNA以及释放的因子,TUNEL检测肝细胞凋亡,检测肝脏纤维化相关指标。结果表明:IRE1A抑制剂可减少巨噬细胞浸润,减少肝脏损伤。

构建Ire1a基因敲除鼠,重复上述步骤,检测Xbp1的mRNA,EVs数量,肝功能,巨噬细胞浸润,肝脏纤维化等指标。

IRE1A抑制后循环EVs的数量也相应减少,表明IRE1A可调控肝细胞释放EVs。小鼠注射过表达IRE1A的腺病毒,检测EVs的数量和Xbp1的mRNA表达量,IRE1A抑制剂、IRE1A的RNase做rescue实验验证。对EVs进行表征,检测不同处理状态下的数量。
IRE1A可促进巨噬细胞的募集,诱导肝损伤。腺病毒转染的过表达IRE1A小鼠中IHC和流式分别检测巨噬细胞浸润,检测巨噬细胞相关mRNA和细胞因子表达,进一步流式检测分析髓样细胞来源的巨噬细胞亚型。结果表明:IRE1A可促进促炎型巨噬细胞浸润至肝脏。

IRE1A刺激原代小鼠肝细胞并分离EVs后尾静脉注射进小鼠体内,检测EVs的数量和肝脏对EVs的摄取情况,巨噬细胞浸润情况。结果表明:IRE1A肝细胞来源的EVs可促进巨噬细胞浸润至肝脏,并且展现出促炎表型。

探究IRE1A对EVs释放的调控机制。之前的研究中,脂毒性EVs的释放取决于神经酰胺的从头合成,因此研究IRE1A对神经酰胺从头合成途径的影响。

SPT催化神经酰胺合成的限速酶,因此ChIP实验从转录水平研究IRE1A对SPT的调节。SPT抑制剂抑制神经酰胺合成后检测EVs的数量进一步验证:神经酰胺合成途径对于EVs释放是重要的,而IRE1A可调节神经酰胺合成来调节EVs的合成。

在人类肝脏样本中验证XBP1和SPTLC1与炎症、EVs的数量之间的相关性。







