研载生物科技(上海)有限公司
9 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
文献支持
细胞增殖实验/CCK8
¥1200
公司新闻/正文
携带在细胞囊泡上的EPHB2通过激活ephrin信号通路诱导肿瘤血管形成
1815 人阅读发布时间:2020-02-18 12:02
头颈鳞状细胞癌(HNSCC)作为一种侵袭性癌症,易转移到淋巴结或远端器官上,造成较高死亡率;而血管生成是保证肿瘤吸收营养,促进其生长代谢的途径。现有大量报道显示细胞外囊泡(EVs)通过携带一些RNA和蛋白质发挥促血管生成的作用,但是否HNSCC分泌的EVs亦有此功能呢?2019年12月由美国范德比尔特大学医学院Shinya Sato发表在JCI insight杂志上的一篇文章,研究了HNSCC分泌的EVs能通过携带EPHB2,激活ephrin信号通路,促进血管形成。
文章链接:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6962030/

技术路线:
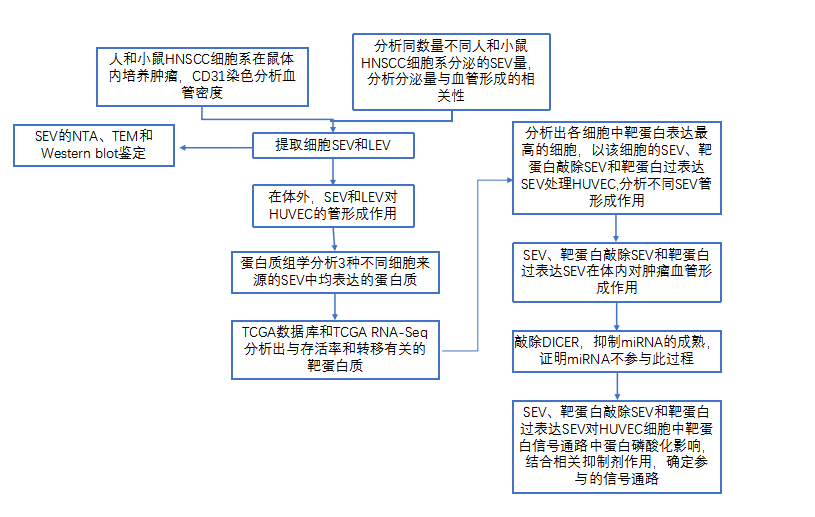
研究结果:
1.细胞分泌的SEV与HNSCC诱导的血管形成有关
将人(SCC61,OSC19, Detroit 562)和小鼠(MOC1, MOC2)的HNSCC细胞注射到裸鼠舌头来诱导肿瘤,对肿瘤中内皮细胞标志物CD31进行免疫染色,从Figure 1B,C可以看出Detroit 562和MOC2肿瘤的血管密度要高于其他组,同时Figure 1D也显示出这两个细胞具高分泌SEV能力。表明了血管密度与SEV分泌率有关(Figure1E)。
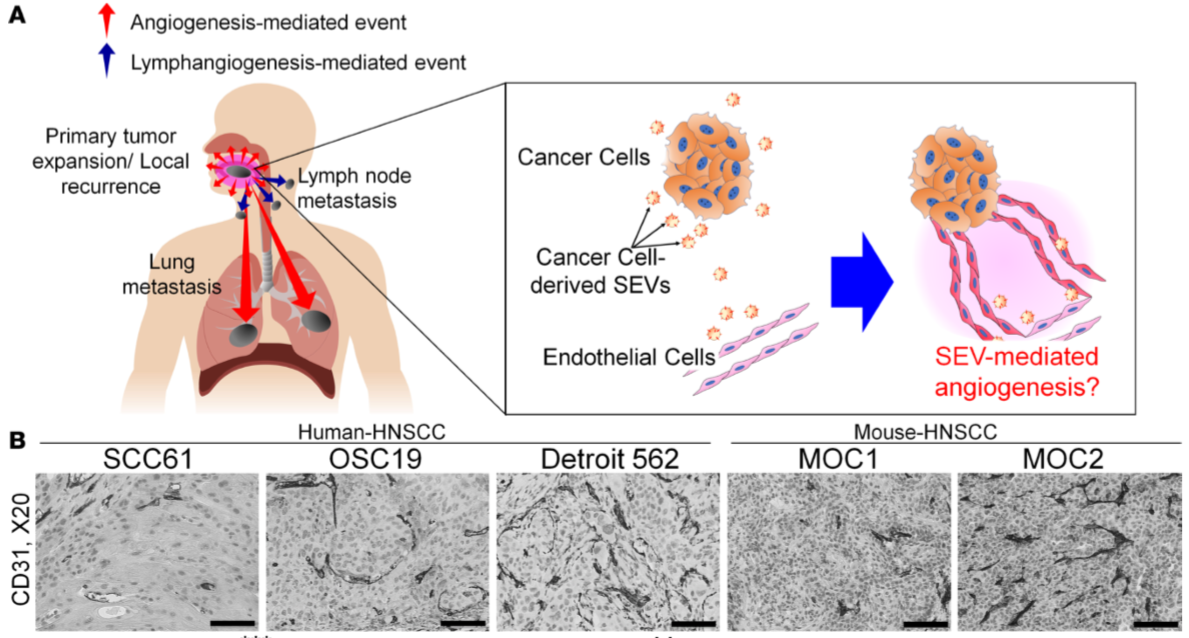
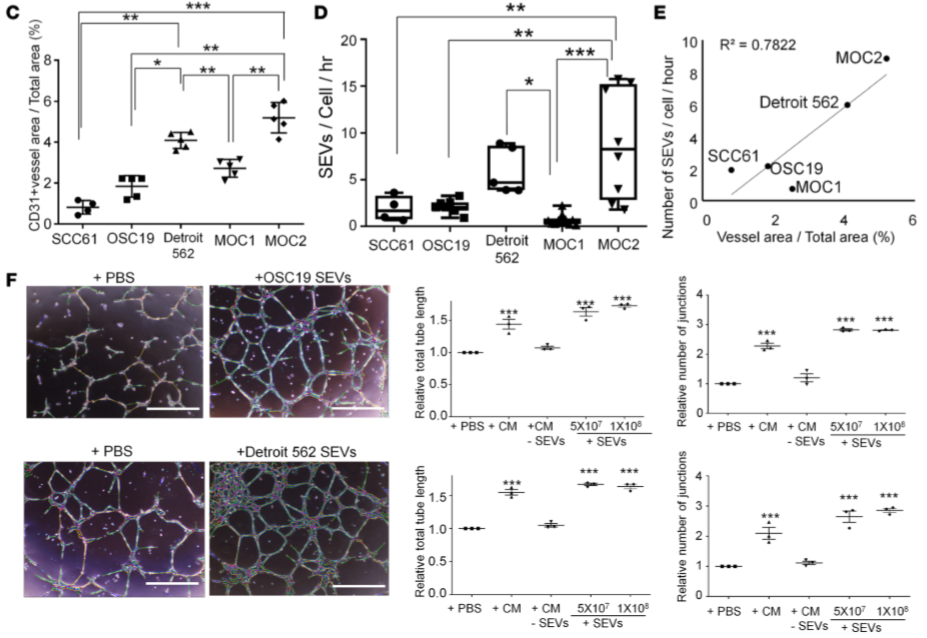
Figure 1 源自HNSCC细胞的SEV可促进血管形成
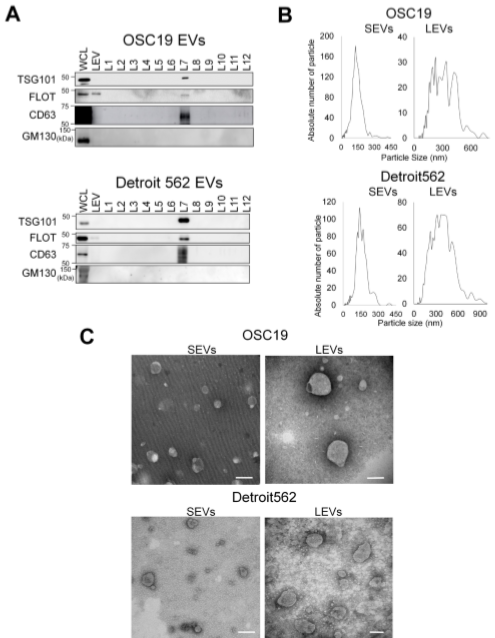
Supplemental Figure 1 外泌体鉴定
2.纯化的HNSCC SEVs促进内皮管形成
从OSC19,Detroit 562细胞培养液中提出SEV和LEV(SEV的鉴定参见Supplemental Figure 1 A-C),处理HUVEC和HMVEC-dLyAds细胞后,能显著增加内皮管网络的形成(Figure 1F,Supplemental Figure 2C),而LEV不具此作用(Supplemental Figure 2A)。SCC61和FaDu细胞的SEV亦能促进内皮管形成(Supplemental Figure 2B)。表明在体外HNSCC细胞的SEV具促进内皮管形成作用。
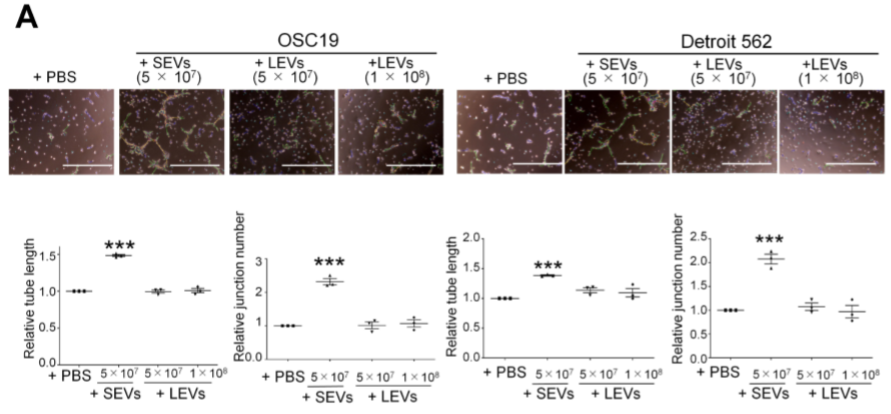
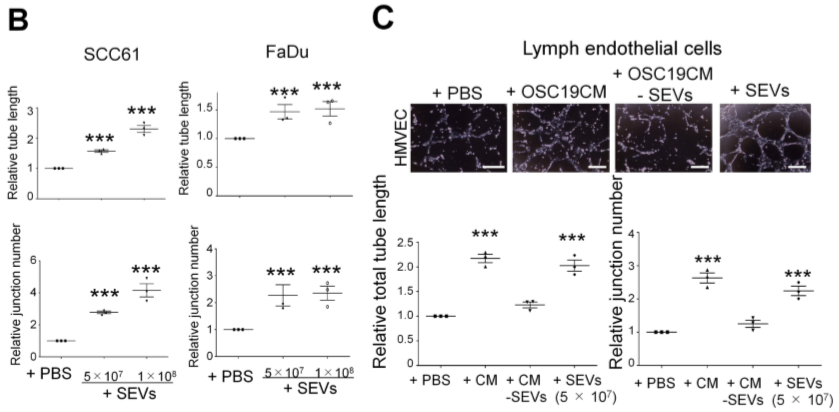
Supplemental Figure 2 源自HNSCC细胞的SEV可促进血管形成
3.蛋白质组学和转录组学分析确定EPHB2为候选的促血管生成EV携带物
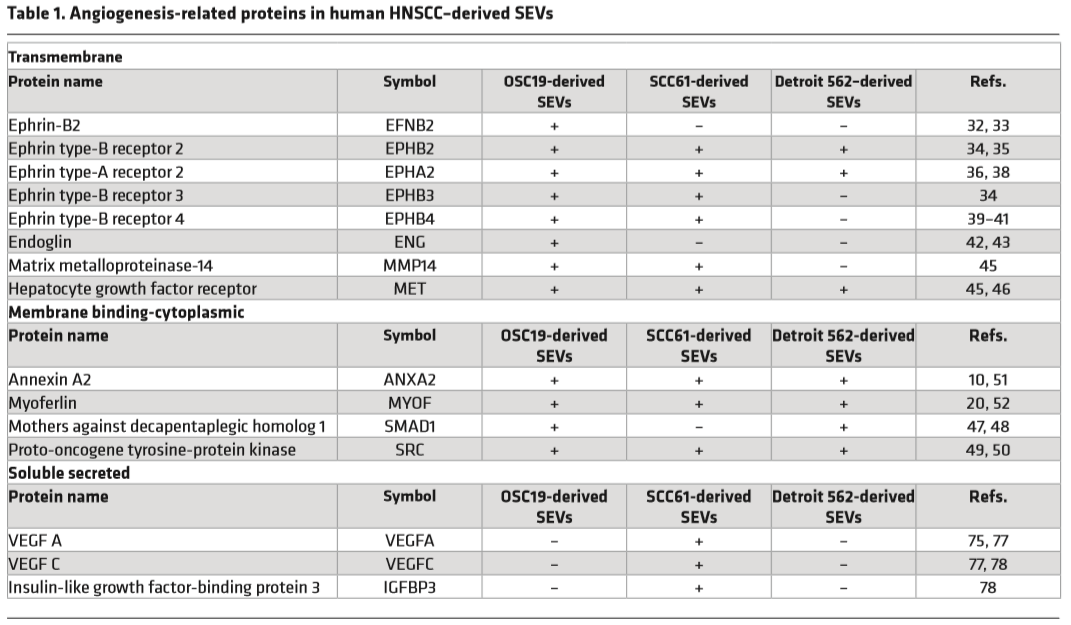
经蛋白质组学分析3种不同细胞来源的SEV,发现其含多种ephrin和ephrin受体(Eph)家族蛋白(Table 1)。结合TCGA数据库和TCGA RNA-Seq数据分析,显示EPHB2的过表达(而非EPHA2的过表达)与HNSCC患者的生存率降低显着相关(Figure 2A),且血管生成基因集与HNSCC肿瘤中的EPHB2 mRNA表达密切相关(Figure 2B)。
TCGA RNA-Seq数据分析Cortactin(CTTN)的过表达与HNSCC患者低存活率相关(Figure 2C),而CTTN与EPHB2的共高表达与肿瘤转移相关(Figure 2D,E)。因此作者选EPHB2作为介导SEV促血管生成作用的候选者。
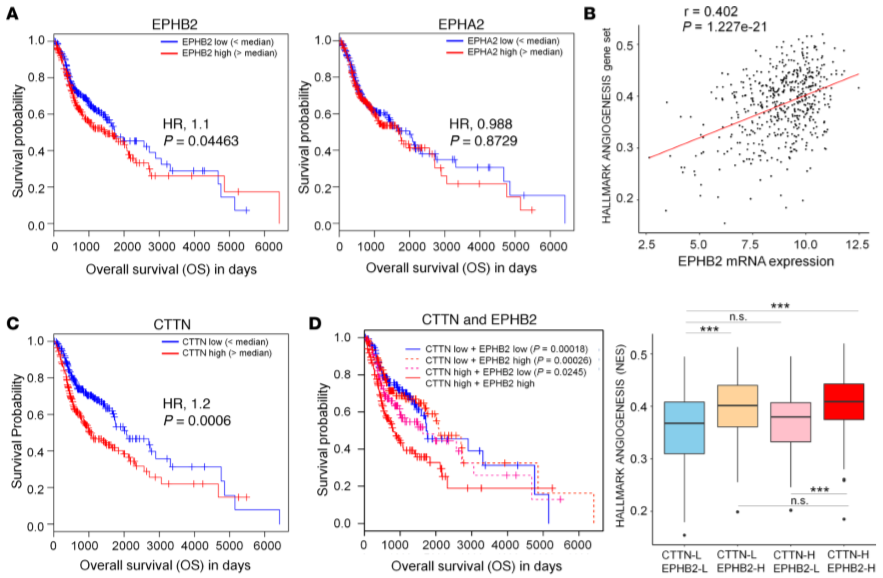
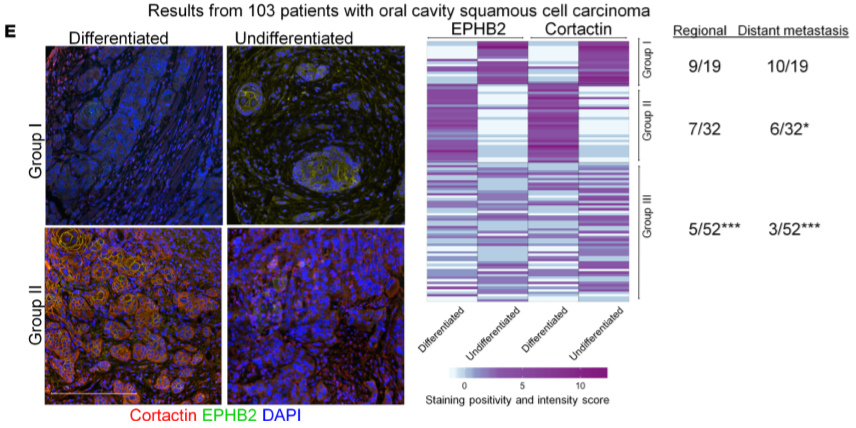
Figure 2 HNSCC肿瘤中EPHB2的高表达与患者存活率和血管形成有关
4.SEV中EPHB2促内皮管形成
EPHB2在OSC19细胞中表达最高,且在SEV中有表达,而在LEV中无(Figure 3A),将OSC19 SEV和重组EPHB2处理HUVEC细胞,均可诱导ephrin-B磷酸化(Figure 3B),但若将SEV先与重组ephrin-B2结合,再处理HUVEC细胞,便降低了SEV诱导管形成能力(Figure 3C,D)。
另用EPHB2-knockdown(EPHB2-KD)或EPHB2过表达(EPHB2-OE)的OSC19细胞SEV处理HUVEC细胞,发现EPHB2-KD SEV处理组的管形成显着减少(Figure 4A,B); EPHB2-OE SEV增加了管形成(Figure 4C,D)。说明了EPHB2参与SEV促血管形成。
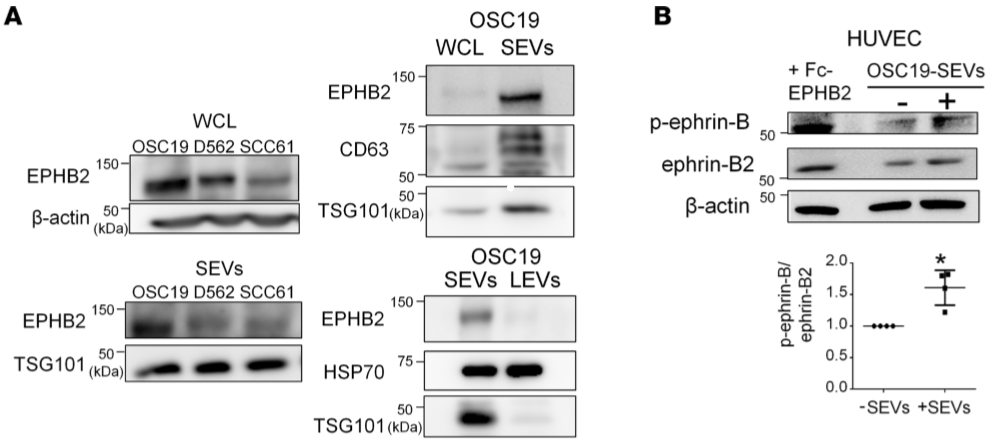
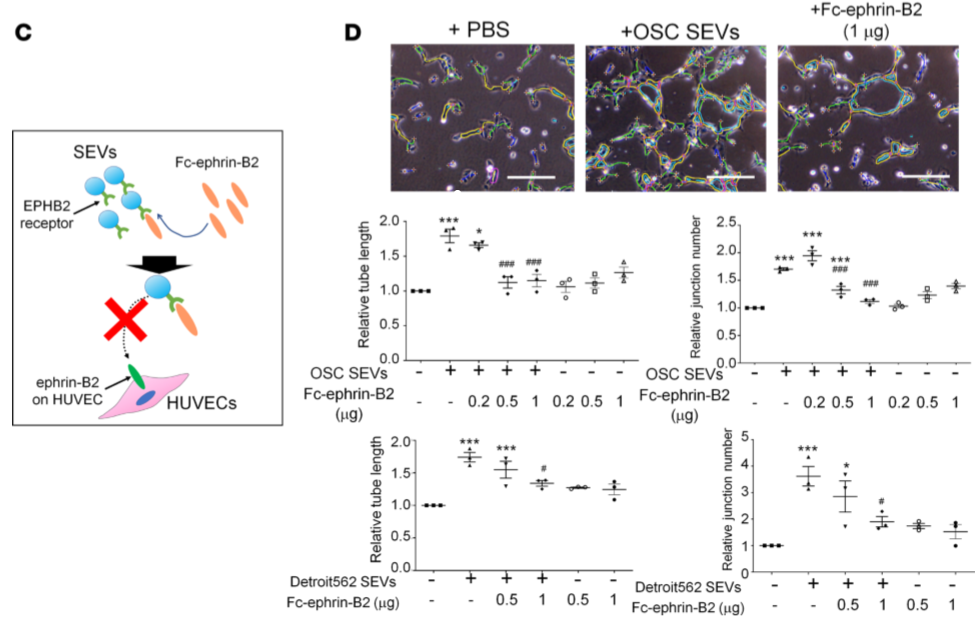
Figure 3 SEV携带EPHB2并诱导ephrin反向信号通路
5.HNSCC的SEV诱导体内血管生成
作者将SEV和生长因子降低的Matrigel植入裸鼠皮下21天,血管标志CD31在SEV作用下明显增多,但EPHB2-KD或Fc-ephrin-B2预处理的SEV组几乎无血管形成(Figure 4E)。另在HNSCC肿瘤模型小鼠中,EPHB2-OE OSC19肿瘤的血管密度显著增加(Figure 4F)。
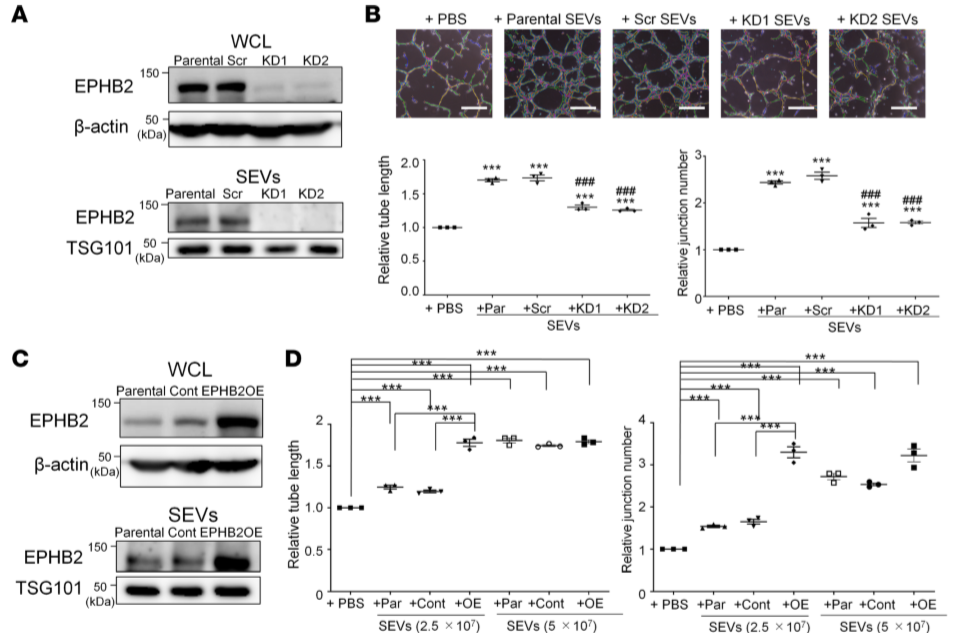
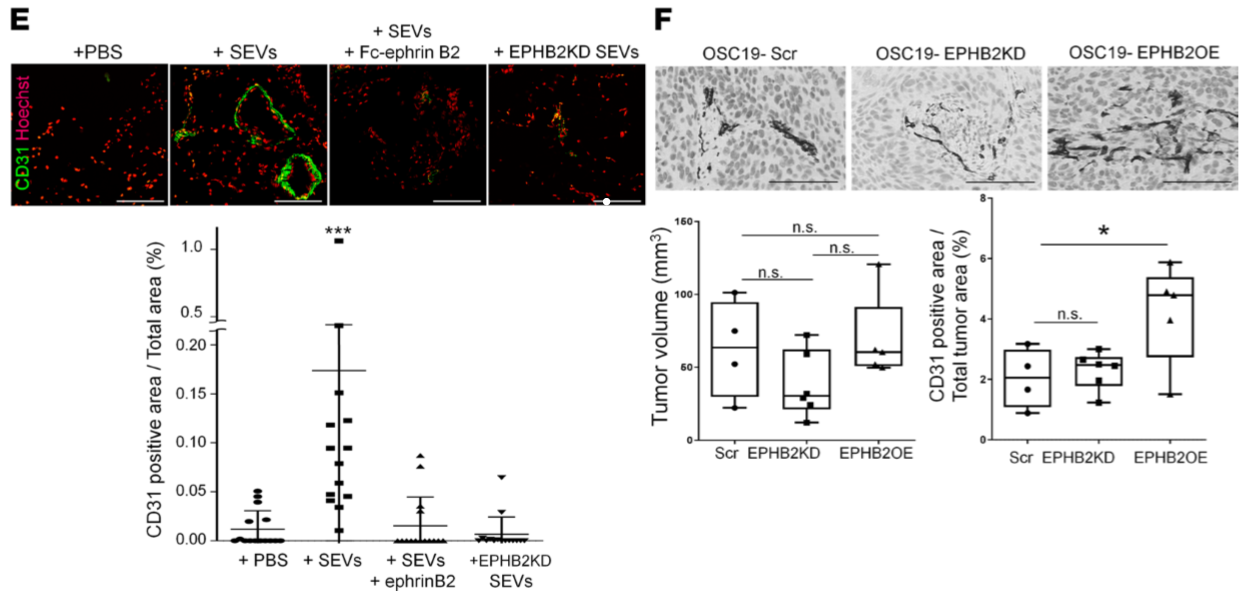
Figure 4 SEV上的EPHB2在体外能促进管形成,在体内能诱导血管形成
6.miRNA不参与HNSCC SEV的促血管形成过程
鉴于一些报告表明miRNA参与EV的促血管生成作用,作者将OSC19细胞中DICER- knockdown(Supplemental Figure 3A),纯化出了成熟的miRNA降低,pre-miRNA增加的SEV(Supplemental Figure 3B),如Supplemental Figure 3C所示,用DICER-KD细胞的EV处理的HUVEC的总管长度和结点数量的分析没有显示出明显的变化。表明miRNA的传递不太可能是HNSCC SEV上EPHB2促进血管生成的机制。
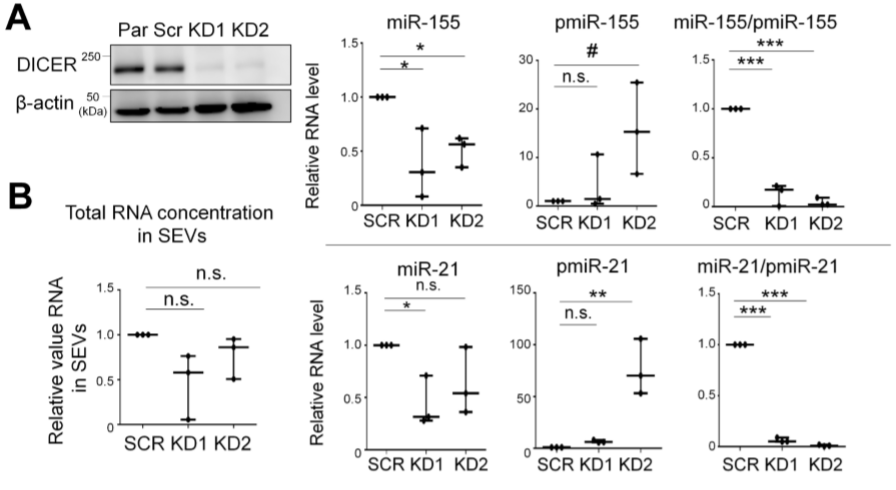
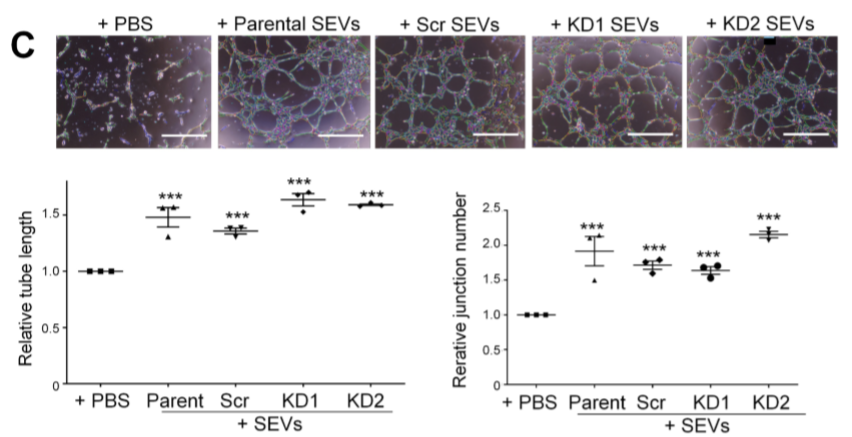
Supplemental Figure 3 miRNA在HNSCC SEV的促血管形成过程中不起关键作用
7.SEV携带的EPHB2通过诱导ephrin反向信号传导促进血管生成
基于SEV可诱导ephrin-B磷酸化,将EPHB2-KD或EPHB2-OE SEV处理HUVEC细胞,发现EPHB2-KD SEV降低细胞中ephrin-B磷酸化,而EPHB2-OE SEV促进细胞中ephrin-B磷酸化, 同时,ephrin-B下游的STAT3的磷酸化与ephrin-B磷酸化保持一致(Figure 5A),使用STAT3的抑制剂即可抑制SEV的促血管形成作用(Figure 5B)。表明SEV携带的EPHB2通过激活ephrin反向信号传导和下游STAT3激活来诱导血管生成。
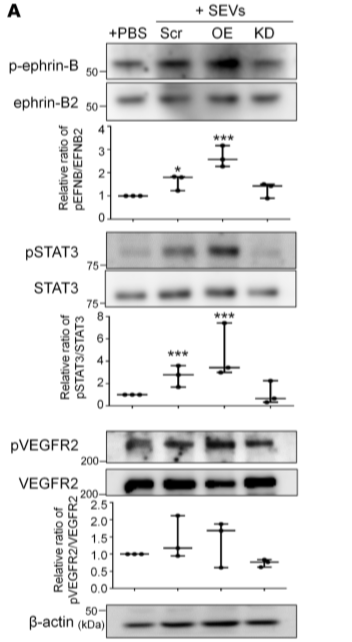
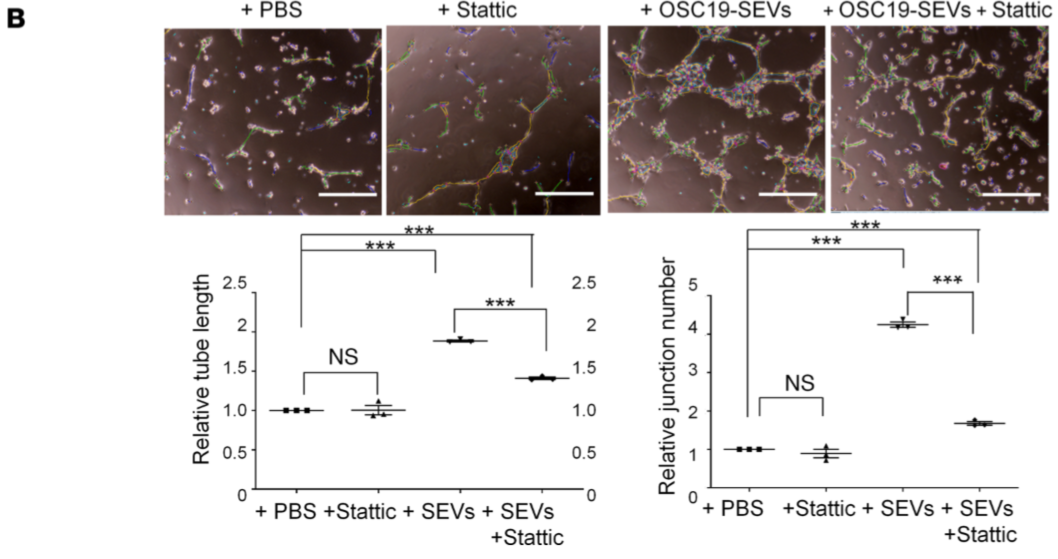
Figure 5 SEV上的EPHB2驱动ephrin-B-STAT3信号级联反应促进血管生成
总结:
如下图所示,作者发现HNSCC分泌的SEV携带的EPHB2可以诱导ephrin-B反向信号传导,进而促肿瘤血管生成。该机制对于理解HNSCC微环境可能很重要,也可能是未来癌症治疗的潜在目标。
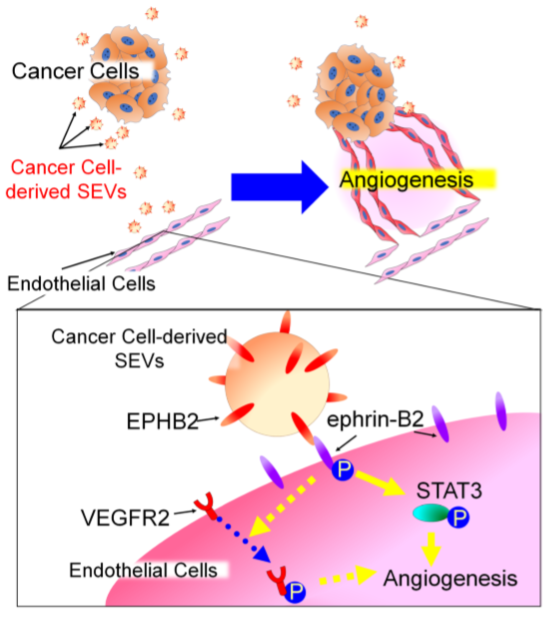
文章链接:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6962030/

技术路线:

研究结果:
1.细胞分泌的SEV与HNSCC诱导的血管形成有关
将人(SCC61,OSC19, Detroit 562)和小鼠(MOC1, MOC2)的HNSCC细胞注射到裸鼠舌头来诱导肿瘤,对肿瘤中内皮细胞标志物CD31进行免疫染色,从Figure 1B,C可以看出Detroit 562和MOC2肿瘤的血管密度要高于其他组,同时Figure 1D也显示出这两个细胞具高分泌SEV能力。表明了血管密度与SEV分泌率有关(Figure1E)。


Figure 1 源自HNSCC细胞的SEV可促进血管形成

Supplemental Figure 1 外泌体鉴定
2.纯化的HNSCC SEVs促进内皮管形成
从OSC19,Detroit 562细胞培养液中提出SEV和LEV(SEV的鉴定参见Supplemental Figure 1 A-C),处理HUVEC和HMVEC-dLyAds细胞后,能显著增加内皮管网络的形成(Figure 1F,Supplemental Figure 2C),而LEV不具此作用(Supplemental Figure 2A)。SCC61和FaDu细胞的SEV亦能促进内皮管形成(Supplemental Figure 2B)。表明在体外HNSCC细胞的SEV具促进内皮管形成作用。


Supplemental Figure 2 源自HNSCC细胞的SEV可促进血管形成
3.蛋白质组学和转录组学分析确定EPHB2为候选的促血管生成EV携带物
经蛋白质组学分析3种不同细胞来源的SEV,发现其含多种ephrin和ephrin受体(Eph)家族蛋白(Table 1)。结合TCGA数据库和TCGA RNA-Seq数据分析,显示EPHB2的过表达(而非EPHA2的过表达)与HNSCC患者的生存率降低显着相关(Figure 2A),且血管生成基因集与HNSCC肿瘤中的EPHB2 mRNA表达密切相关(Figure 2B)。
TCGA RNA-Seq数据分析Cortactin(CTTN)的过表达与HNSCC患者低存活率相关(Figure 2C),而CTTN与EPHB2的共高表达与肿瘤转移相关(Figure 2D,E)。因此作者选EPHB2作为介导SEV促血管生成作用的候选者。


Figure 2 HNSCC肿瘤中EPHB2的高表达与患者存活率和血管形成有关

4.SEV中EPHB2促内皮管形成
EPHB2在OSC19细胞中表达最高,且在SEV中有表达,而在LEV中无(Figure 3A),将OSC19 SEV和重组EPHB2处理HUVEC细胞,均可诱导ephrin-B磷酸化(Figure 3B),但若将SEV先与重组ephrin-B2结合,再处理HUVEC细胞,便降低了SEV诱导管形成能力(Figure 3C,D)。
另用EPHB2-knockdown(EPHB2-KD)或EPHB2过表达(EPHB2-OE)的OSC19细胞SEV处理HUVEC细胞,发现EPHB2-KD SEV处理组的管形成显着减少(Figure 4A,B); EPHB2-OE SEV增加了管形成(Figure 4C,D)。说明了EPHB2参与SEV促血管形成。


Figure 3 SEV携带EPHB2并诱导ephrin反向信号通路
5.HNSCC的SEV诱导体内血管生成
作者将SEV和生长因子降低的Matrigel植入裸鼠皮下21天,血管标志CD31在SEV作用下明显增多,但EPHB2-KD或Fc-ephrin-B2预处理的SEV组几乎无血管形成(Figure 4E)。另在HNSCC肿瘤模型小鼠中,EPHB2-OE OSC19肿瘤的血管密度显著增加(Figure 4F)。


Figure 4 SEV上的EPHB2在体外能促进管形成,在体内能诱导血管形成
6.miRNA不参与HNSCC SEV的促血管形成过程
鉴于一些报告表明miRNA参与EV的促血管生成作用,作者将OSC19细胞中DICER- knockdown(Supplemental Figure 3A),纯化出了成熟的miRNA降低,pre-miRNA增加的SEV(Supplemental Figure 3B),如Supplemental Figure 3C所示,用DICER-KD细胞的EV处理的HUVEC的总管长度和结点数量的分析没有显示出明显的变化。表明miRNA的传递不太可能是HNSCC SEV上EPHB2促进血管生成的机制。


Supplemental Figure 3 miRNA在HNSCC SEV的促血管形成过程中不起关键作用
7.SEV携带的EPHB2通过诱导ephrin反向信号传导促进血管生成
基于SEV可诱导ephrin-B磷酸化,将EPHB2-KD或EPHB2-OE SEV处理HUVEC细胞,发现EPHB2-KD SEV降低细胞中ephrin-B磷酸化,而EPHB2-OE SEV促进细胞中ephrin-B磷酸化, 同时,ephrin-B下游的STAT3的磷酸化与ephrin-B磷酸化保持一致(Figure 5A),使用STAT3的抑制剂即可抑制SEV的促血管形成作用(Figure 5B)。表明SEV携带的EPHB2通过激活ephrin反向信号传导和下游STAT3激活来诱导血管生成。


Figure 5 SEV上的EPHB2驱动ephrin-B-STAT3信号级联反应促进血管生成
总结:
如下图所示,作者发现HNSCC分泌的SEV携带的EPHB2可以诱导ephrin-B反向信号传导,进而促肿瘤血管生成。该机制对于理解HNSCC微环境可能很重要,也可能是未来癌症治疗的潜在目标。







