研载生物科技(上海)有限公司
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
间充质干细胞来源的外泌体通过诱导自噬修复帕金森病模型
1124 人阅读发布时间:2020-05-11 15:31
文献链接:https://doi.org/10.1038/s41419-020-2473-5
患病率逐年增加的帕金森病(PD)是一种进行性神经变性疾病,研究表明人脐带间充质干细胞(hucMSC)因具神经保护作用,对PD具备治疗效果,但其不可控制的分化及低存活于宿主体内限制了其应用,迫切需要具有类似修复作用的替代hucMSCs移植的替代方法。由河北医科大学第一医院于2020年4月在《Cell Death & Disease》(IF:5.959)上发表了论文“Exosomes derived from mesenchymal stem cells repair a Parkinson’s disease model by inducing autophagy” ,对hucMSC分泌的Exos是否可以代替hucMSC发挥作用作了探讨。
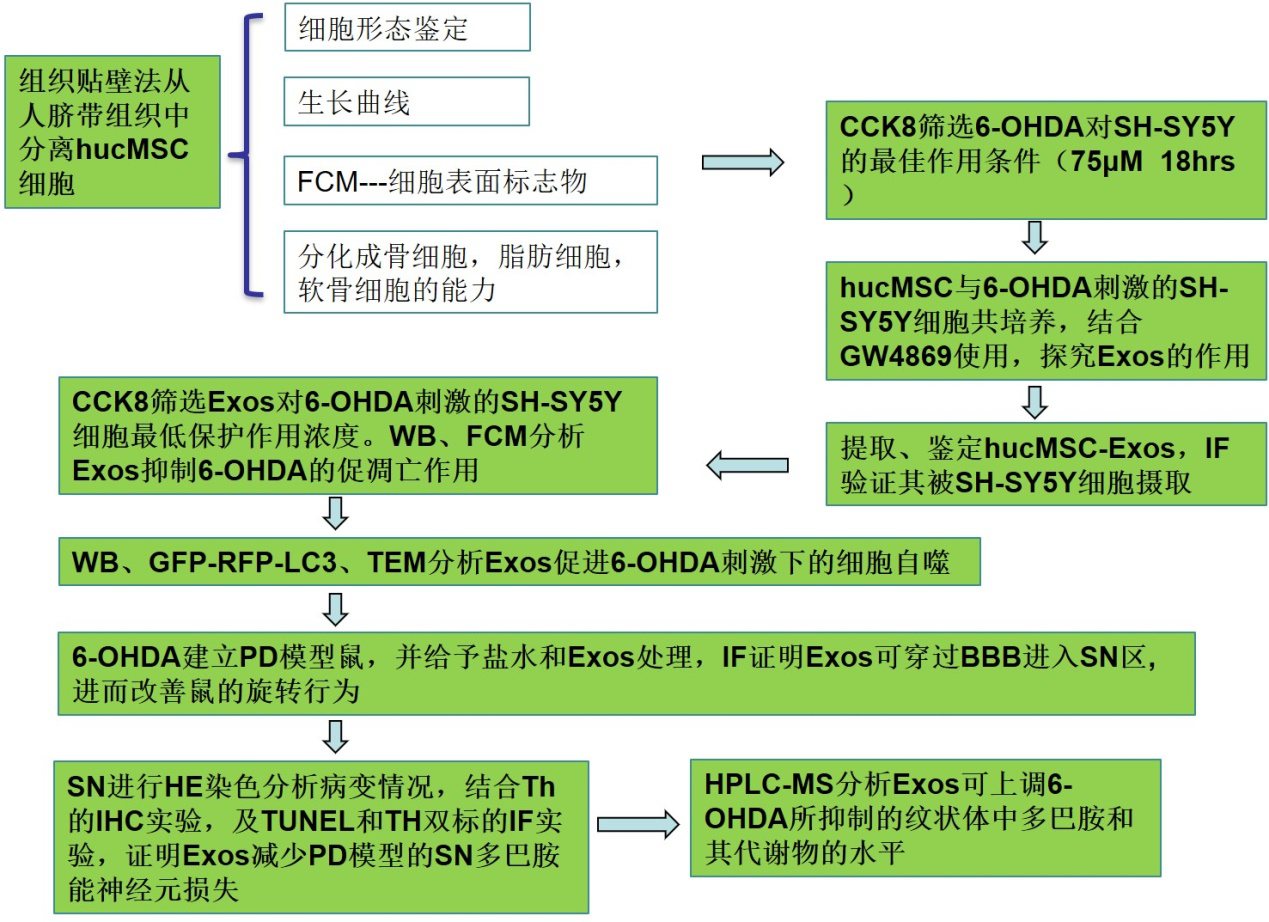
研究结果:
1. hucMSC细胞分离培养鉴定
利用组织块贴壁方法从人脐带中分离出hucMSC细胞,呈现多边形或纺锤形生长(图1a)。生长的第二天,细胞即可进入对数生长期。第三天,由于更换培养基,生长速度减慢,但第二天又迅速增加,表现出强大的自我更新和繁殖能力(图1b)。FCM分析P3代细胞,其高表达干细胞标志物CD90、CD105和CD73,血细胞标志物CD34、CD45和HLA-DR为阴性表达(图1c)。另细胞能在诱导培养基的作用下分化为软骨细胞、成骨及成脂(图1d)。
因此,该细胞为hucMSC细胞,可用于后续实验。
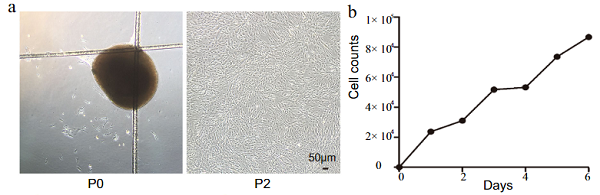
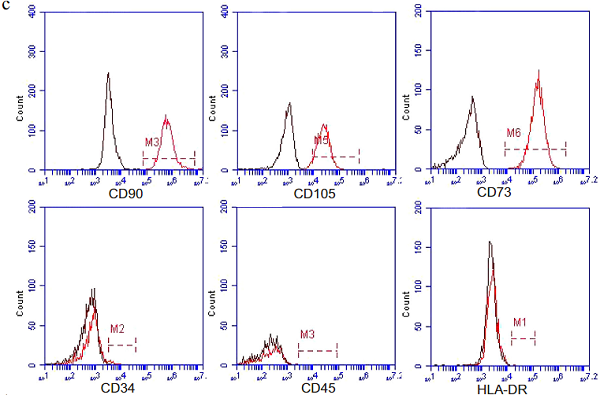
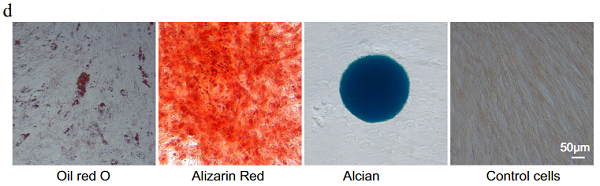
图1 hucMSC的鉴定
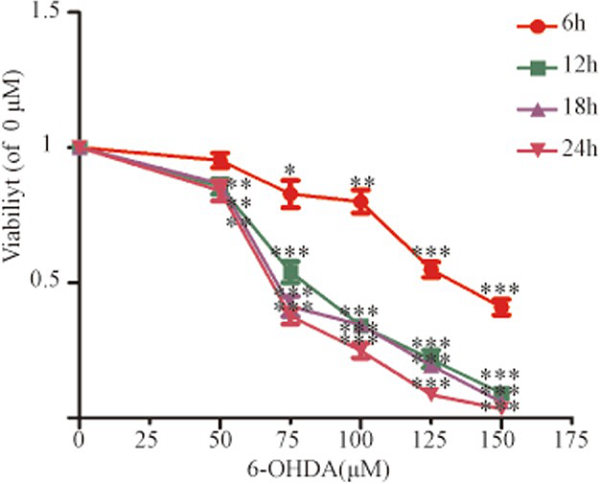
图2 6-OHDA刺激的SH-SY5Y细胞活力
3.hucMSCs逆转6-OHDA抑制的SH-SY5Y细胞增殖,且Exos参与该过程
作者建立hucMSC与6-OHDA刺激的SH-SY5Y细胞共培养体系(图3a),分为5组:对照组,6-OHDA组,6-OHDA + GW4869组,6-OHDA + hucMSCs组和6-OHDA + hucMSCs + GW4869组。hucMSCs逆转6-OHDA抑制的SH -SY5Y细胞增殖,同时GW4869可衰减这种作用(图3b)。该阻止细胞直接接触和大囊泡转移的体系表明了Exos可能参与了hucMSC逆转6-OHDA造成的SH-SY5Y细胞活力降低的过程。
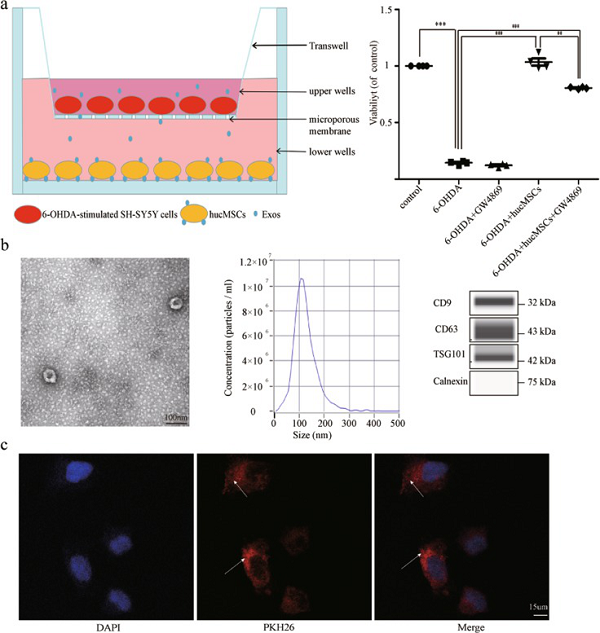
图3 Exos功能及鉴定
3.hucMSCs-Exos鉴定及被SH-SY5Y摄取
超速离心提取hucMSCs在无血清培养基中培养48hrs后上清液中的Exos,TEM 、NTA和Western blot对其进行鉴定(图3b)。另借助IF实验证明PKH26-Exos能成功被SH-SY5Y细胞摄取(图3c)。
4.Exos增强SH-SY5Y细胞活力并减少6-OHDA诱导的凋亡
将SH-SY5Y细胞与不同浓度的Exos共培养12 hrs,再用6-OHDA处理,Exos以剂量依赖方式促细胞增殖,在40ug/ml是显著增强(P < 0.05)(图4a)。另Western blot结果显示,与6-OHDA组相比,剪切后的Caspase3在6-OHDA+Exos组中显著降低(图4b),细胞凋亡亦减少(图4c),表明Exos可降低6-OHDA诱导的细胞凋亡作用。
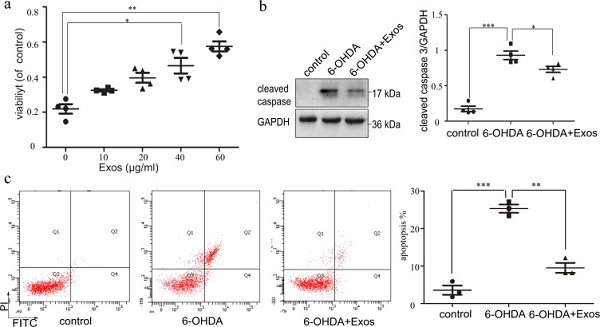
图4 Exos促SH-SY5Y细胞存活抑制凋亡
5. Exos增加6-OHDA刺激的SH-SY5Y细胞自噬水平
为探究Exos是否诱导自噬,作者借助WB分析6-OHDA + Exos组LC3B-II / I和Beclin-1的表达显著增强,而P62的表达下降(图5a)。自噬体与溶酶体融化抑制剂Baf-A1的使用使LC3B-II / I,Beclin-1和p62的水平明显更高,表明Exos激活6-OHDA刺激的SH-SY5Y细胞发生自噬。
GFP-RFP-LC3转染细胞中,用共聚焦显微镜观察自噬体(黄色斑点)和自噬溶酶体(红色斑点)发现,Exos处理增加黄色和红色斑点的数量,Baf-A1在不影响Exos引起的红色斑点数量情况下,进一步增加黄色斑点的数量(图5b),TEM亦证明这一结果(图5c)。
表明由Exos诱导的自噬增加可能为6-OHDA刺激的细胞凋亡提供保护作用。
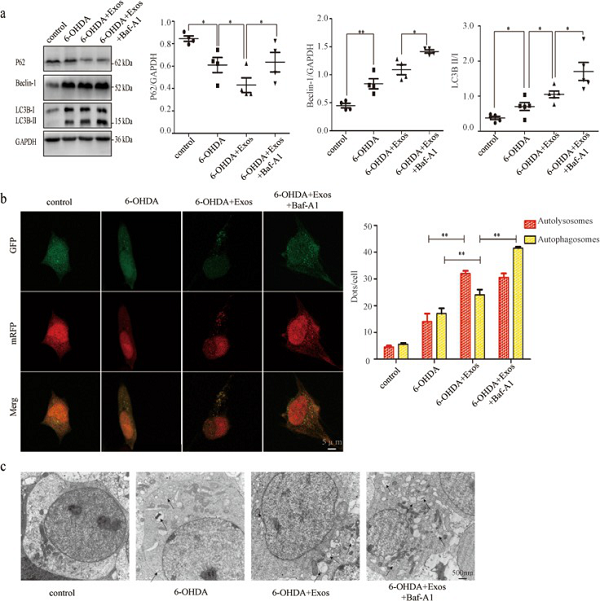
图5 Exos增加6-OHDA刺激的SH-SY5Y细胞自噬的水平
6.Exos可穿过BBB到达脑黑质(SN),缓解PD模型中的不对称旋转
按图6a处理方式,对PD模型鼠给予盐水和Exos处理后,发现Exos能与SN中多巴胺能神经元(TH:酪氨酸羟化酶)共定位(图6b)。另与6-OHDA +盐水组相比,给Exos处理的鼠随着时间的推移,不对称旋转行为明显减少(图6c)。表明,Exos可以穿越BBB并到达SN,进而改善PD模型鼠的行为缺陷。
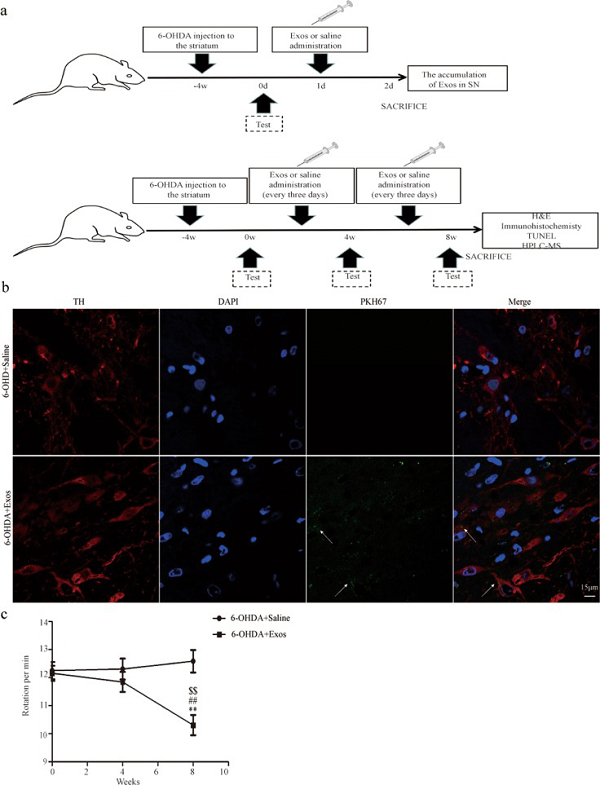
图6 Exos在脑组织SN中的积累并改善PD模型的行为缺陷
7.Exos显著减少PD模型的SN多巴胺能神经元损失
对SN进行HE染色分析,6-OHDA +盐水组细胞间隙中出现收缩,表现不同程度的变性和坏死性,IHC分析TH表明,6-OHDA +盐水组的手术侧表现多巴胺能神经元的减少。而Exos在一定程度上的抑制6-OHDA的作用(图7b、c),表现出对SN多巴胺能神经元的保护作用。
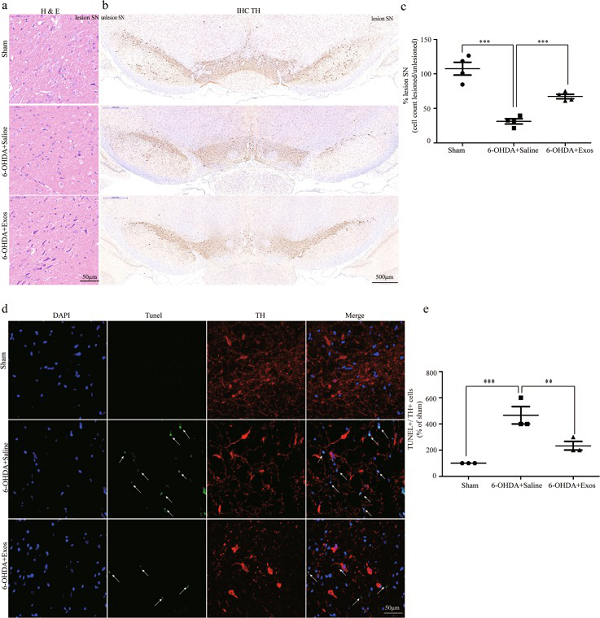
图7 Exos减少PD大鼠模型中SN多巴胺能神经元的丢失和凋亡
8.Exos降低PD大鼠模型中TUNEL + / TH +细胞的数量
如图7d所示,与6-OHDA +盐水组相比, 6-OHDA + Exos组中TUNEL + / TH +细胞的数量明显减少。表明Exos可保护多巴胺能神经元免受6-OHDA刺激。
9. Exos上调PD大鼠纹状体中多巴胺及其代谢物的水平
图 8a显示多巴胺(DA)和其代谢物二羟基苯基乙酸(DOPAC)和高香草酸(HVA)的化学结构式。用HPLC-MS分析它们在不同组纹状体中的含量,与对照相比,6-OHDA +盐水组的DA、DOPAC和HVA水平显著降低。而Exos的存在可改善此反应(图8b)。表明Exos增加纹状体中DA及其代谢产物的水平。
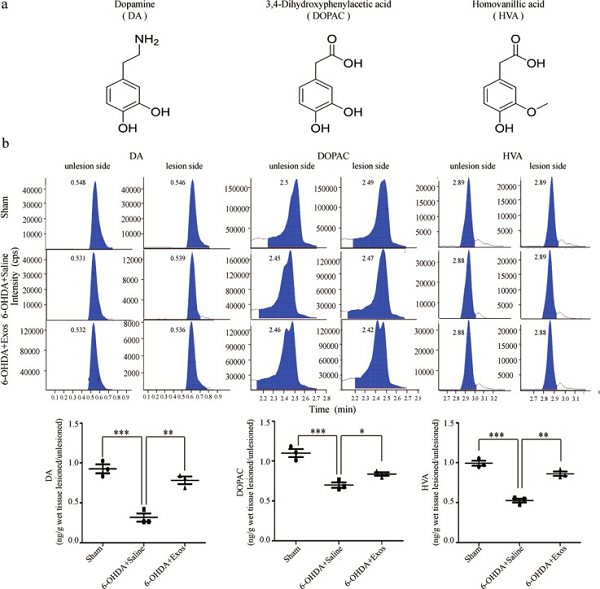
图8 Exos上调PD大鼠模型纹状体中DA及其代谢产物的水平
总结:
本研究发现hucMSCs衍生的能逆转6-OHDA对SH-SY5Y细胞存活的抑制作用,保护PD模型鼠的神经元, 且细胞自噬在介导Exos对PD的治疗过程中起到重要作用。
患病率逐年增加的帕金森病(PD)是一种进行性神经变性疾病,研究表明人脐带间充质干细胞(hucMSC)因具神经保护作用,对PD具备治疗效果,但其不可控制的分化及低存活于宿主体内限制了其应用,迫切需要具有类似修复作用的替代hucMSCs移植的替代方法。由河北医科大学第一医院于2020年4月在《Cell Death & Disease》(IF:5.959)上发表了论文“Exosomes derived from mesenchymal stem cells repair a Parkinson’s disease model by inducing autophagy” ,对hucMSC分泌的Exos是否可以代替hucMSC发挥作用作了探讨。

研究结果:
1. hucMSC细胞分离培养鉴定
利用组织块贴壁方法从人脐带中分离出hucMSC细胞,呈现多边形或纺锤形生长(图1a)。生长的第二天,细胞即可进入对数生长期。第三天,由于更换培养基,生长速度减慢,但第二天又迅速增加,表现出强大的自我更新和繁殖能力(图1b)。FCM分析P3代细胞,其高表达干细胞标志物CD90、CD105和CD73,血细胞标志物CD34、CD45和HLA-DR为阴性表达(图1c)。另细胞能在诱导培养基的作用下分化为软骨细胞、成骨及成脂(图1d)。
因此,该细胞为hucMSC细胞,可用于后续实验。



图1 hucMSC的鉴定
2. 6-羟基多巴胺(6-OHDA)刺激的SH-SY5Y细胞活力
与对照组相比,PD的常用模型药物6-OHDA以剂量依赖性方式抑制SH-SY5Y细胞活力,75 µM的6-OHDA处理细胞18 hours时,细胞活力降低50%(P < 0.001)(图2),因此选择此浓度用于后续实验。
图2 6-OHDA刺激的SH-SY5Y细胞活力
3.hucMSCs逆转6-OHDA抑制的SH-SY5Y细胞增殖,且Exos参与该过程
作者建立hucMSC与6-OHDA刺激的SH-SY5Y细胞共培养体系(图3a),分为5组:对照组,6-OHDA组,6-OHDA + GW4869组,6-OHDA + hucMSCs组和6-OHDA + hucMSCs + GW4869组。hucMSCs逆转6-OHDA抑制的SH -SY5Y细胞增殖,同时GW4869可衰减这种作用(图3b)。该阻止细胞直接接触和大囊泡转移的体系表明了Exos可能参与了hucMSC逆转6-OHDA造成的SH-SY5Y细胞活力降低的过程。

图3 Exos功能及鉴定
3.hucMSCs-Exos鉴定及被SH-SY5Y摄取
超速离心提取hucMSCs在无血清培养基中培养48hrs后上清液中的Exos,TEM 、NTA和Western blot对其进行鉴定(图3b)。另借助IF实验证明PKH26-Exos能成功被SH-SY5Y细胞摄取(图3c)。
4.Exos增强SH-SY5Y细胞活力并减少6-OHDA诱导的凋亡
将SH-SY5Y细胞与不同浓度的Exos共培养12 hrs,再用6-OHDA处理,Exos以剂量依赖方式促细胞增殖,在40ug/ml是显著增强(P < 0.05)(图4a)。另Western blot结果显示,与6-OHDA组相比,剪切后的Caspase3在6-OHDA+Exos组中显著降低(图4b),细胞凋亡亦减少(图4c),表明Exos可降低6-OHDA诱导的细胞凋亡作用。

图4 Exos促SH-SY5Y细胞存活抑制凋亡
5. Exos增加6-OHDA刺激的SH-SY5Y细胞自噬水平
为探究Exos是否诱导自噬,作者借助WB分析6-OHDA + Exos组LC3B-II / I和Beclin-1的表达显著增强,而P62的表达下降(图5a)。自噬体与溶酶体融化抑制剂Baf-A1的使用使LC3B-II / I,Beclin-1和p62的水平明显更高,表明Exos激活6-OHDA刺激的SH-SY5Y细胞发生自噬。
GFP-RFP-LC3转染细胞中,用共聚焦显微镜观察自噬体(黄色斑点)和自噬溶酶体(红色斑点)发现,Exos处理增加黄色和红色斑点的数量,Baf-A1在不影响Exos引起的红色斑点数量情况下,进一步增加黄色斑点的数量(图5b),TEM亦证明这一结果(图5c)。
表明由Exos诱导的自噬增加可能为6-OHDA刺激的细胞凋亡提供保护作用。

图5 Exos增加6-OHDA刺激的SH-SY5Y细胞自噬的水平
6.Exos可穿过BBB到达脑黑质(SN),缓解PD模型中的不对称旋转
按图6a处理方式,对PD模型鼠给予盐水和Exos处理后,发现Exos能与SN中多巴胺能神经元(TH:酪氨酸羟化酶)共定位(图6b)。另与6-OHDA +盐水组相比,给Exos处理的鼠随着时间的推移,不对称旋转行为明显减少(图6c)。表明,Exos可以穿越BBB并到达SN,进而改善PD模型鼠的行为缺陷。

图6 Exos在脑组织SN中的积累并改善PD模型的行为缺陷
7.Exos显著减少PD模型的SN多巴胺能神经元损失
对SN进行HE染色分析,6-OHDA +盐水组细胞间隙中出现收缩,表现不同程度的变性和坏死性,IHC分析TH表明,6-OHDA +盐水组的手术侧表现多巴胺能神经元的减少。而Exos在一定程度上的抑制6-OHDA的作用(图7b、c),表现出对SN多巴胺能神经元的保护作用。

图7 Exos减少PD大鼠模型中SN多巴胺能神经元的丢失和凋亡
8.Exos降低PD大鼠模型中TUNEL + / TH +细胞的数量
如图7d所示,与6-OHDA +盐水组相比, 6-OHDA + Exos组中TUNEL + / TH +细胞的数量明显减少。表明Exos可保护多巴胺能神经元免受6-OHDA刺激。
9. Exos上调PD大鼠纹状体中多巴胺及其代谢物的水平
图 8a显示多巴胺(DA)和其代谢物二羟基苯基乙酸(DOPAC)和高香草酸(HVA)的化学结构式。用HPLC-MS分析它们在不同组纹状体中的含量,与对照相比,6-OHDA +盐水组的DA、DOPAC和HVA水平显著降低。而Exos的存在可改善此反应(图8b)。表明Exos增加纹状体中DA及其代谢产物的水平。

图8 Exos上调PD大鼠模型纹状体中DA及其代谢产物的水平
总结:
本研究发现hucMSCs衍生的能逆转6-OHDA对SH-SY5Y细胞存活的抑制作用,保护PD模型鼠的神经元, 且细胞自噬在介导Exos对PD的治疗过程中起到重要作用。






