研载生物科技(上海)有限公司
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
M2巨噬细胞衍生的外泌体通过靶向E2F2促进胰腺导管腺癌的血管生成和生长
1032 人阅读发布时间:2021-03-22 16:12
预后较差的胰腺导管腺癌(PDAC)作为全球最具致命性的恶性肿瘤,其进展与血管密度正相关。肿瘤相关巨噬细胞(TAM)是外周血单核细胞浸润到实体肿瘤组织中而演变成的巨噬细胞,约占肿瘤基质细胞的15-20%,可诱导内皮细胞增殖和血管生成,但其机制目前尚不清晰。
外泌体为细胞来源的双层膜结构,可通过携带miRNA、mRNA、和蛋白质等,参与胞间的信息传递。近期研究显示巨噬细胞来源的外泌体(MDEs)影响肿瘤的生长、转移和免疫逃逸,且M2 MDEs能通过传递miR-365促进PC耐gemcitabine。上海市第一人民医院裘正军课题组探究了M2 MDEs促进PDACs血管生成的机制,该项研究发表在Molecular Therapy上.。
首先,作者发现PDAC中M2巨噬细胞的量与血管密度成正比,基于这一现象,作者制备了M2 MDEs和M0 MDEs。 通过体外实验证明M2 MDEs可被小鼠主动脉内皮细胞(MAECs)摄取,进而促进细胞迁移、血管形成。同时,建立肿瘤模型,将MDEs注射到瘤体中,与对照组相比,M2 MDEs可促进肿瘤的生长及血管生成。
借助miRNA测序和Q-PCR筛选出M2巨噬细胞富含miR-155和miR-221,而M2 MDEs中富含miR-146、miR-382、miR-155和miR-221,为确定目的分子,作者用M2 MDEs与M0 MDEs处理MAECs,Q-PCR检测出MAECs中miR-155和miR-221在M2 MDEs的作用下高表达。因此,筛选出miR-155-5p和miR-221-5p富含于M2 MDEs中,可由MDEs传递到MAECs细胞中。生信分析miR-155-5p和miR-221-5p的靶基因中E2F2被报道能抑制内皮细胞血管生成。实验验证了miR-155-5p和miR-221-5p是通过靶向E2F2,从而诱导MAECs血管生成。
总而言之,这项研究证实了TAM可通过释放携带miR-155-5p和miR-221-5p的外泌体,抑制E2F2的表达,促进PDAC的血管形成。
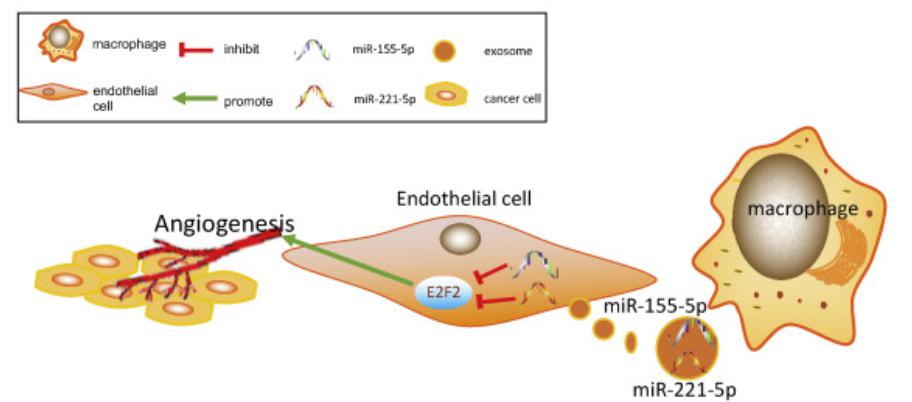
参考文献:Yang, Y., et al. (2020). "M2 macrophage-derived exosomes promote angiogenesis and growth of pancreatic ductal adenocarcinoma by targeting E2F2. Mol Ther. 2021 Mar 3;29(3):1226-1238. doi: 10.1016/j.ymthe.2020.11.024. Epub 2020 Nov 20






