研载生物科技(上海)有限公司
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
牛乳外泌体对IEC-6细胞氧化应激的保护作用
894 人阅读发布时间:2021-04-06 10:56
MicroRNAs (miRNAs)是一种小的非编码RNA,在关键的生物学过程中发挥着介导基因表达的作用。然而,外泌体对肠道氧化应激的影响尚不清楚。针对这一问题,来自同济大学医学院,上海东方医院转化医学研究中心的研究者们分析了氧化应激下IEC-6细胞中牛乳外泌体的潜在作用。他们发现外泌体预处理提高了IEC-6细胞活力和抗氧化酶(SOD和GPX)活性,降低了ROS、LDH和MDA水平。进一步分析发现外泌体预处理导致miR-146a和miR-155水平升高,Nrf2和Ho1基因表达水平下调,HO-1蛋白水平升高。这些结果表明牛乳外泌体对H2O2诱导的氧化应激具有保护作用。该研究发表在European Journal of Nutrition第60卷1期上。


牛奶是人类最常饮用的饮料。富含多种营养物质和生物活性因子。最近的研究发现,牛奶中富含有大量的外泌体。外泌体是细胞外囊泡( EVs)的一种,大小在30-150nm。外泌体广泛分布于组织的细胞外间隙和体液(包括血浆,尿液和牛奶)中。据报道牛乳来源的外泌体在调节免疫功能,减轻疾病和调节肠道菌群中发挥重要作用。牛乳来源的外泌体可预防实验性坏死性小肠结肠炎的发生,延缓关节炎的发生,减轻小肠上皮细胞(IEC)的死亡,加速小肠上皮细胞的生长,并调节基因表达。牛奶外泌体及其载物的膳食消耗会导致循环miRNA的丢失,并引发诸如认知能力的丧失、嘌呤代谢产物水平的增加、生育能力的丧失和免疫反应的改变等表型。
作为日常饮食进入人体的首要障碍,肠道不仅是营养物质吸收和吸收的主要场所,而且还是产生大量活性氧(ROS)的器官之一。 过量ROS引起的氧化损伤是肠道疾病的主要原因之一,包括胃肠道十二指肠溃疡,炎症性肠病和胃肠道(GI)恶性肿瘤,例如胃癌和大肠癌。 因此,如何预防和应对氧化损伤一直是肠道疾病研究的重点和热点。抗氧化酶(如SOD和GPX)是保护细胞免受ROS破坏的最重要的成分。该研究发现牛乳外泌体通过抑制ROS和LDH的释放,以及通过增加SOD和GPX的活性来保护细胞免受氧化应激。
目前,外泌体调节抗氧化酶活性的机制很大程度上是未知的。研究表明,miRNA在几乎所有细胞过程中都发挥着至关重要的作用,从分化和发育到细胞死亡。miRNA是氧化应激的调节剂,能够调节ROS的产生和内源性抗氧化剂的防御能力。牛乳外泌体富含miR-155和miR-146。该研究结果发现外泌体预处理诱导H2O2处理的IEC-6细胞中miR-155和miR-146a水平的增加。
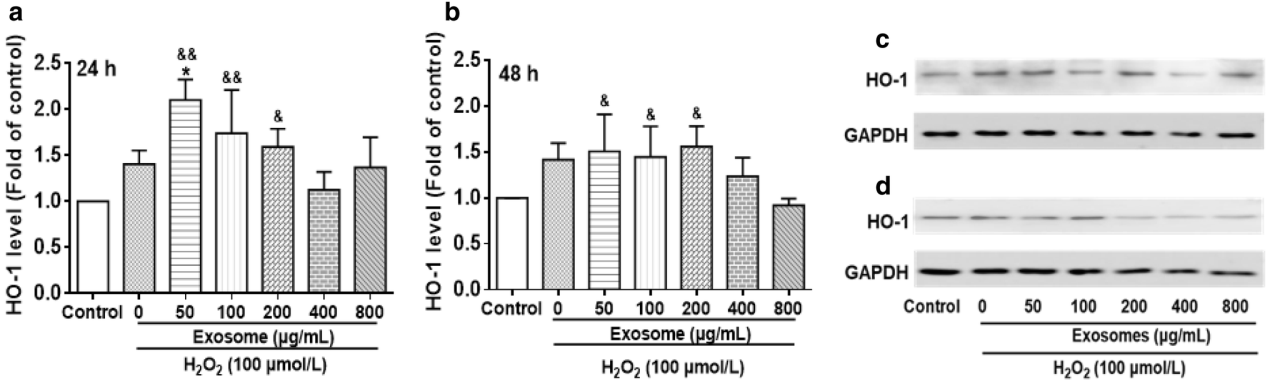
证据表明,一些miRNA(包括miR-155和miR-146a)可以靶向Nrf2“微调”氧化还原稳态。NRF2是一种氧化还原敏感性转录因子,在调节氧化防御中起着关键作用。NRF2通过调节一系列参与抗氧化防御的基因的表达来控制氧化还原稳态。这些基因编码一系列抗氧化酶,包括HO-1,SOD,过氧化氢酶,GPX和谷胱甘肽S-转移酶。该研究分析了外泌体和H2O2处理后NRF2途径变化。他们发现与对照组相比,使用外泌体进行预处理24 h或48 h可使HO-1蛋白水平显着增加。

外泌体对IEC-6细胞中HO-1表达的影响
这项研究为牛乳外泌体对H2O2诱导的IEC-6细胞氧化应激的潜在保护作用提供了重要证据。外泌体预处理可通过增加细胞增殖、清除细胞内ROS和MDA、提高抗氧化酶活性来保护IEC-6细胞免受氧化应激的影响。外泌体预处理提高了细胞内miRNA水平和HO-1蛋白表达。
参考文献:Wang L, Shi Z, Wang X, Mu S, Xu X, Shen L, Li P: Protective effects of bovine milk exosomes against oxidative stress in IEC-6 cells. Eur J Nutr 2021, 60(1):317-327.
这项研究为牛乳外泌体对H2O2诱导的IEC-6细胞氧化应激的潜在保护作用提供了重要证据。外泌体预处理可通过增加细胞增殖、清除细胞内ROS和MDA、提高抗氧化酶活性来保护IEC-6细胞免受氧化应激的影响。外泌体预处理提高了细胞内miRNA水平和HO-1蛋白表达。
参考文献:Wang L, Shi Z, Wang X, Mu S, Xu X, Shen L, Li P: Protective effects of bovine milk exosomes against oxidative stress in IEC-6 cells. Eur J Nutr 2021, 60(1):317-327.






