研载生物科技(上海)有限公司
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
CAF分泌的miR-522可抑制铁死亡并促进胃癌的获得性耐药
1051 人阅读发布时间:2022-03-28 18:05
铁死亡是一种非凋亡性细胞死亡的新模式,其特征是脂质过氧化产物以细胞铁依赖性方式蓄积。近期的研究表明,激活与受精症相关的途径可以有效地阻止肿瘤的发展,并能增强化学疗法,靶向疗法甚至免疫疗法的作用。实体瘤微环境中的良性细胞通常有助于肿瘤的发展和耐药性。例如,癌症相关的成纤维细胞(CAF)通过分泌各种生物活性物质(包括外泌体)来支持肿瘤的进展和耐药性。然而,CAF在调节脂类代谢以及癌细胞的铁死亡中的作用仍是未知的。来自天津医科大学肿瘤医院的Guoguang Ying课题组的 研究人员发现CAF分泌的外泌体miR-522通过靶向花生四烯酸15脂氧合酶(ALOX15)并阻断脂质ROS的积聚来抑制癌细胞的铁死亡。相关研究结果发表于 Molecular Cancer杂志上。
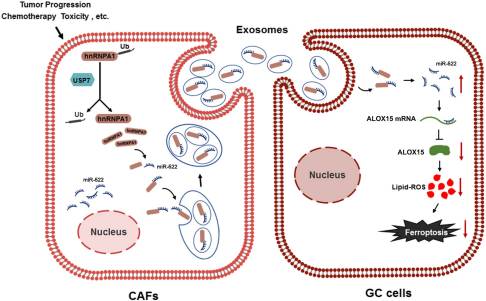 铁死亡是一种调控细胞死亡的新形式,涉及铁依赖性脂质过氧化物(脂质-ROS)的积累,并导致细胞的致命性损害。近期的研究已经证明了铁死亡在介导某些类型的癌症的肿瘤发展和耐药性中起重要作用,但是详细的分子机制仍然知之甚少。肿瘤微环境(TME)由细胞外基质和间充质细胞类型组成,包括成纤维细胞,炎性细胞,周细胞和内皮细胞。肿瘤相关成纤维细胞(CAF)是肿瘤微环境中基质细胞的主要类型,并表现出独特的致瘤特性。
铁死亡是一种调控细胞死亡的新形式,涉及铁依赖性脂质过氧化物(脂质-ROS)的积累,并导致细胞的致命性损害。近期的研究已经证明了铁死亡在介导某些类型的癌症的肿瘤发展和耐药性中起重要作用,但是详细的分子机制仍然知之甚少。肿瘤微环境(TME)由细胞外基质和间充质细胞类型组成,包括成纤维细胞,炎性细胞,周细胞和内皮细胞。肿瘤相关成纤维细胞(CAF)是肿瘤微环境中基质细胞的主要类型,并表现出独特的致瘤特性。
外泌体属于典型直径为30–100 nm的细胞外囊泡(EV)家族,大多数细胞类型都分泌这种外泌体。在过去的十年中,外泌体通过传递蛋白质,脂质,lncRNA,circRNA和microRNA被视为细胞间通讯中的新型信息传递者。近期的研究表明,源自CAF的外泌体可促进肿瘤转移并增加癌细胞的化学耐药性。已有研究发现来自CAF的Exosome-miR-21参与了结直肠癌的奥沙利铂耐药性。并且,CAF分泌的exo-miR-146a可以调节胰腺癌细胞的存活和增殖。但是,尚未确定来自CAF的外泌体在调节癌细胞中脂质代谢和铁死亡的潜在作用。
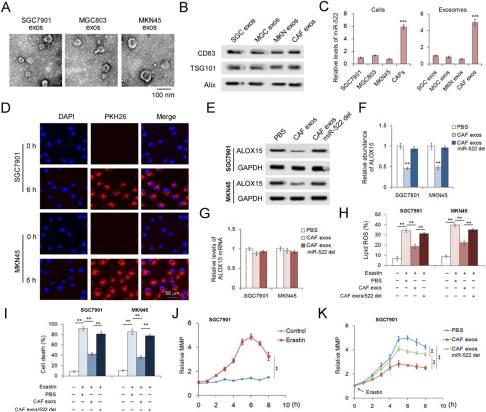 CAF分泌exo-miR-522来抑制胃癌细胞的铁死亡
CAF分泌exo-miR-522来抑制胃癌细胞的铁死亡
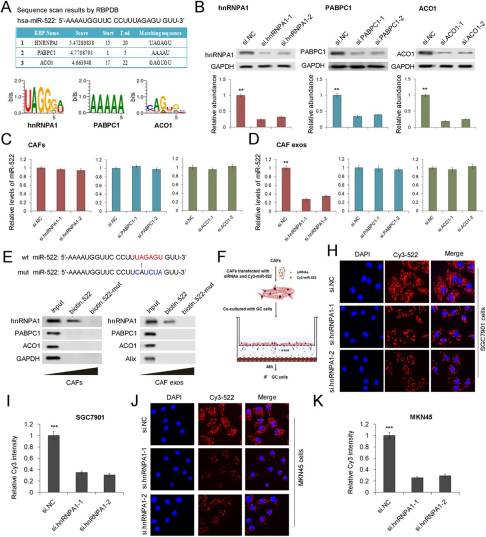 hnRNPA1介导的miR-522进入CAF外泌体的直接证据
hnRNPA1介导的miR-522进入CAF外泌体的直接证据
在这项研究中,研究人员发现ALOX15与胃癌中脂质ROS的产生密切相关,并且外泌体miR-522可作为ALOX15的潜在抑制剂。然后,通过使用原代基质细胞和癌细胞,他们证明了外泌体miR-522主要来源于肿瘤微环境中的CAF。此外,他们还发现泛素特异性蛋白酶7(USP7)/ 异质性胞核核糖核蛋白A1(HNRNPA1)在CAF中过表达促进了miR-522进入外泌体。并且,USP7可以通过去泛素化作用使CAF中的HNRNPA1稳定下来,从而导致外泌体miR-522的分泌增加。他们还通过体外实验证明有助于降低化疗期间的药物敏感性。体内实验表明顺铂和紫杉醇通过激活USP7 / hnRNPA1轴来促进CAF分泌miR-522,从而导致ALOX15抑制并减少脂质-ROS在癌细胞中的蓄积,并导致化学敏感性降低。这些结果表明CAF分泌外泌体miR-522通过靶向ALOX15并阻断脂质ROS的积聚来抑制胃癌细胞的铁死亡。
参考文献:
Zhang H, Deng T, Liu R, Ning T, Yang H, Liu D, Zhang Q, Lin D, Ge S, Bai M et al: CAF secreted miR-522 suppresses ferroptosis and promotes acquired chemo-resistance in gastric cancer. Mol Cancer 2020, 19(1):43.

外泌体属于典型直径为30–100 nm的细胞外囊泡(EV)家族,大多数细胞类型都分泌这种外泌体。在过去的十年中,外泌体通过传递蛋白质,脂质,lncRNA,circRNA和microRNA被视为细胞间通讯中的新型信息传递者。近期的研究表明,源自CAF的外泌体可促进肿瘤转移并增加癌细胞的化学耐药性。已有研究发现来自CAF的Exosome-miR-21参与了结直肠癌的奥沙利铂耐药性。并且,CAF分泌的exo-miR-146a可以调节胰腺癌细胞的存活和增殖。但是,尚未确定来自CAF的外泌体在调节癌细胞中脂质代谢和铁死亡的潜在作用。


在这项研究中,研究人员发现ALOX15与胃癌中脂质ROS的产生密切相关,并且外泌体miR-522可作为ALOX15的潜在抑制剂。然后,通过使用原代基质细胞和癌细胞,他们证明了外泌体miR-522主要来源于肿瘤微环境中的CAF。此外,他们还发现泛素特异性蛋白酶7(USP7)/ 异质性胞核核糖核蛋白A1(HNRNPA1)在CAF中过表达促进了miR-522进入外泌体。并且,USP7可以通过去泛素化作用使CAF中的HNRNPA1稳定下来,从而导致外泌体miR-522的分泌增加。他们还通过体外实验证明有助于降低化疗期间的药物敏感性。体内实验表明顺铂和紫杉醇通过激活USP7 / hnRNPA1轴来促进CAF分泌miR-522,从而导致ALOX15抑制并减少脂质-ROS在癌细胞中的蓄积,并导致化学敏感性降低。这些结果表明CAF分泌外泌体miR-522通过靶向ALOX15并阻断脂质ROS的积聚来抑制胃癌细胞的铁死亡。
参考文献:
Zhang H, Deng T, Liu R, Ning T, Yang H, Liu D, Zhang Q, Lin D, Ge S, Bai M et al: CAF secreted miR-522 suppresses ferroptosis and promotes acquired chemo-resistance in gastric cancer. Mol Cancer 2020, 19(1):43.






