研载生物科技(上海)有限公司
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
干货:铁死亡的机制原理
16130 人阅读发布时间:2022-04-11 11:26

铁死亡是最近公认的一种调节性细胞死亡形式,了解铁死亡的分子机制和信号通路可能为调节人类疾病中的细胞存活和死亡提供新的诊断和治疗方法。研载生物为您解读的这篇综述,从几个重要问题着手总结了铁死亡的调控机制和信号通路,并讨论了铁死亡在疾病中的作用。
概述:
1.铁死亡是一种依赖铁和ROS的调节性细胞死亡 (RCD) 形式。
2.铁死亡在形态、生化和遗传水平上与其他形式的RCD不同。
3.几种分子(如VDAC2/3、谷胱甘肽过氧化物酶(GPX4)、热休克蛋白beta‑1(HSPB1)、核因子E2相关因子2(NRF2)、NADPH氧化酶(NOX)、p53和SLC7A11)通过直接或间接靶向铁代谢和脂质过氧化来调节铁死亡。
4.失调的铁死亡与多种生理和病理过程有关,如癌细胞死亡、组织损伤和T细胞免疫。
问题1,铁死亡的发现历程是怎样的?●铁死亡是RCD的一种术语,最近由Brent R Stockwell博士的实验室在2012年提出。在他们最初的研究中,铁死亡在形态学、生化和遗传水平上与其他类型的RCD明显不同,如细胞凋亡、坏死性凋亡和自噬性细胞死亡(如下表)。
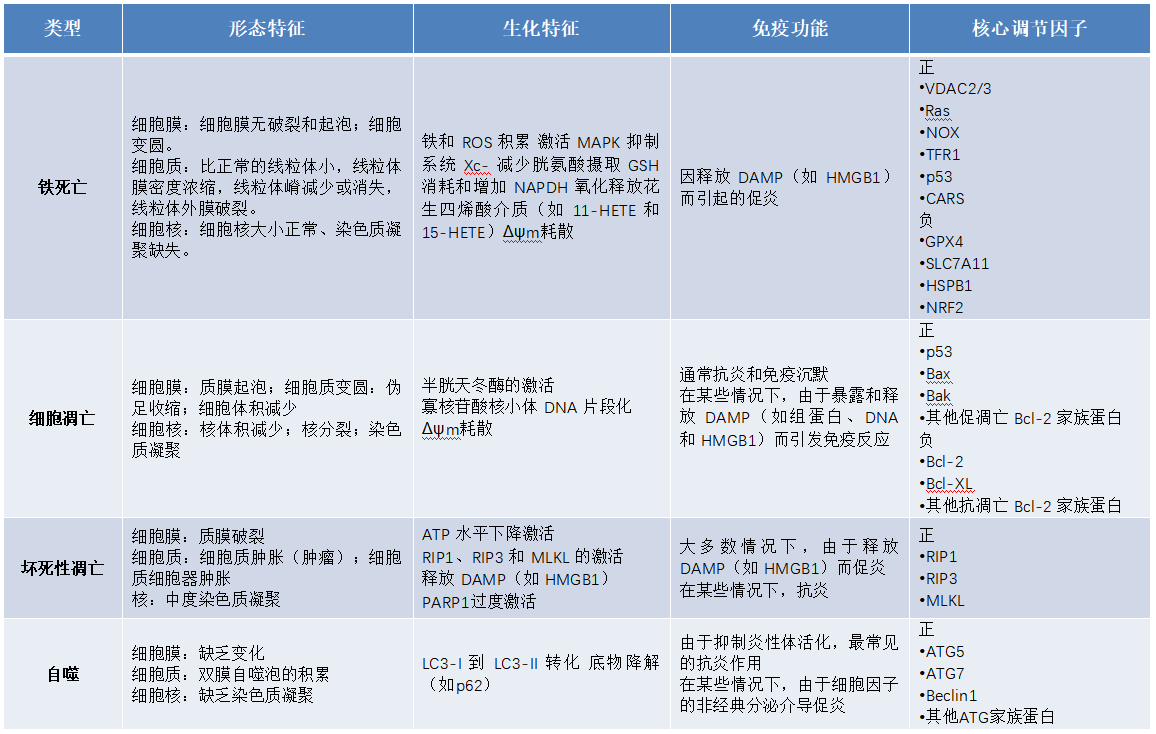
● 诱导剂是在铁死亡的概念被发明之前发现的。2003 年首次被确定为铁死亡诱导剂,erastin 被发现是合成致死的,在人类包皮成纤维细胞(BJeLR)中表达工程突变的Ras癌基因,但不是它们的同基因初级对应物。Ras选择性致死小分子(RSL)‑3和RSL5 后来于2008年在另一项高通量小分子筛选研究中被发现,该研究以非凋亡方式选择性杀死 BJeLR 细胞。小分子抑制剂(如Z‑VAD‑FMK、BOC‑D‑FMK、wortmannin和necrostatin‑1)不能逆转RSL诱导的细胞死亡(如下表)。相反,抗氧化剂(如维生素E)和铁螯合剂(如甲磺酸去铁胺)可阻止RSL诱导的细胞死亡。因此,铁死亡通常是指一种依赖铁的、非凋亡形式的RCD。
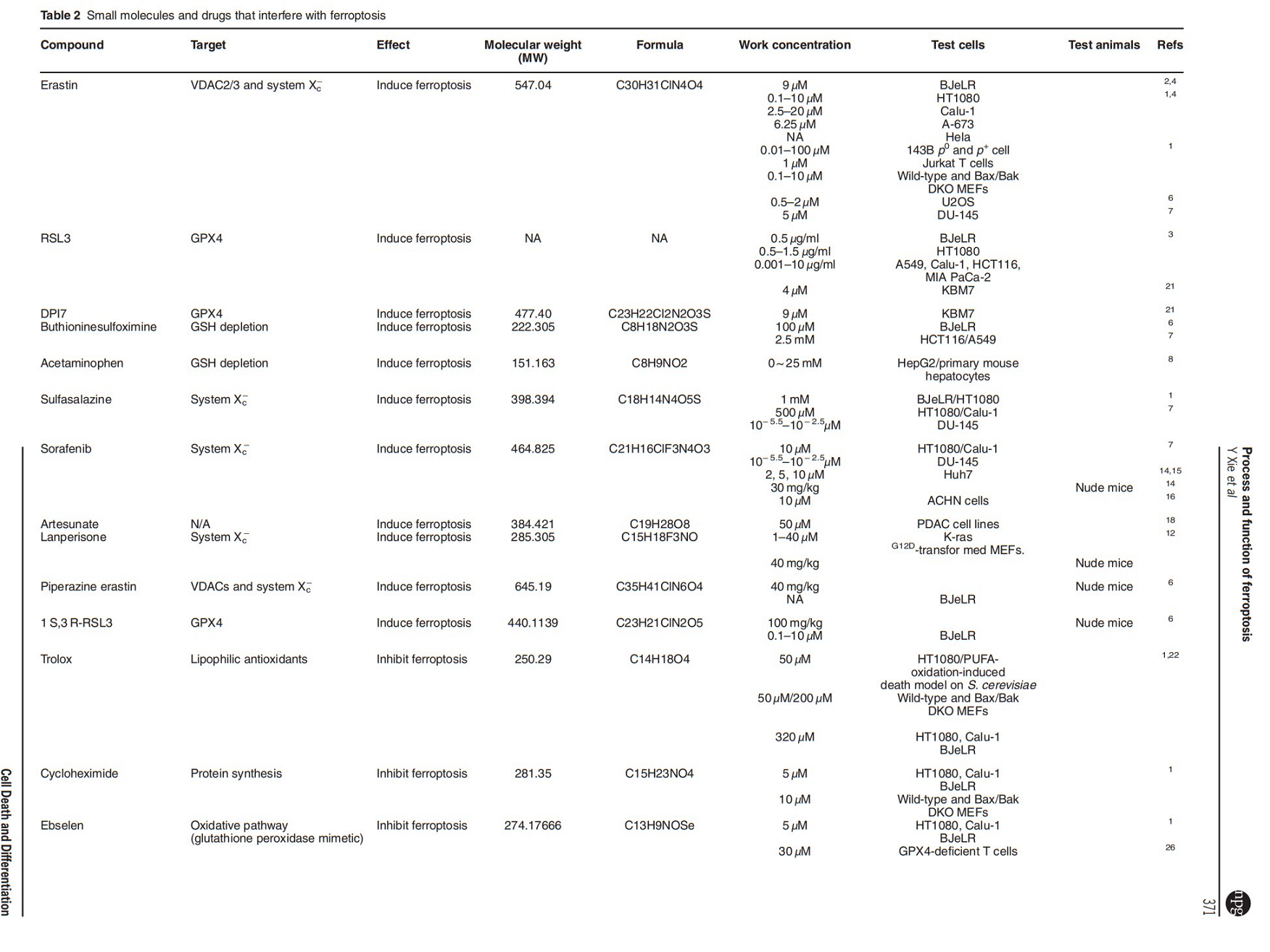
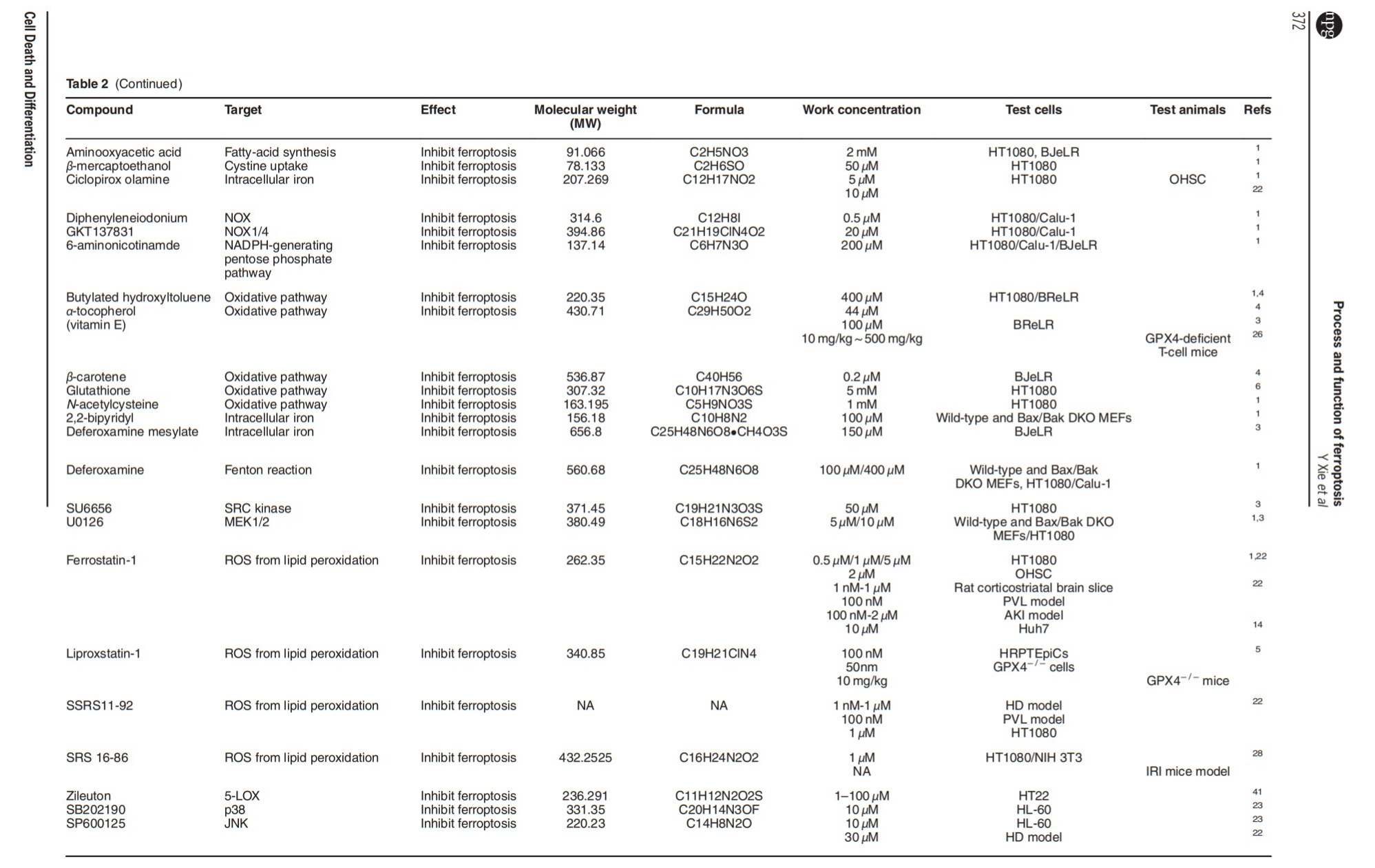
问题2,铁死亡在形态学上是如何体现的?
● 铁死亡细胞表现出线粒体形态和嵴结构的改变。BJeLR细胞经erastin处理后,铁死亡观察到线粒体膜密度增加和线粒体嵴减少/消失的小于正常线粒体。通过在永生化成纤维细胞和肾组织中基因失活GPX4诱导铁死亡与线粒体外膜破裂相关,使用透射电子显微镜观察到。相反,在癌细胞中使用erastin治疗后,核的结构完整性得以保留。在癌细胞中使用erastin治疗后,未观察到核浓缩或染色质边缘。这些形态学特征帮助我们区分铁死亡与细胞凋亡、坏死性凋亡和自噬。
问题3,不同类型诱导剂如何诱导铁死亡?
●Erastin:由erastin 引发的细胞死亡被抗氧化剂和铁螯合剂显著抑制,表明erastin 诱导的铁死亡需要 ROS 和铁依赖的信号传导。
● RSL3和RSL5:铁、ROS 和 MEK 是 RSL3和 RSL5诱导的携带致癌Ras的肿瘤细胞铁死亡所必需的。RSL5需要VDAC2/3,但RSL3诱导的铁死亡不需要。RSL3是 GPX4的直接抑制剂。与GPX4结合后,RSL3使GPX4失活,从而诱导脂质过氧化产生ROS。I型RSL 如erastin和RSL5可以靶向上游调节因子(如VDAC和系统Xc ‑)以诱导铁死亡。II型RSL如RSL3可通过抑制下游调节因子(如GPX4)引发铁死亡。放线军酮显著抑制RSL5,但不抑制RSL3诱导的铁死亡。
● 丁硫氨酸亚砜亚胺 (BSO) :BSO抑制GSH合成,降低GPX活性和增加ROS水平,从而导致Ras突变细胞中的铁死亡。
● 对乙酰氨基酚:对乙酰氨基酚导致GSH耗竭并增加肝损伤。对乙酰氨基酚在原代小鼠肝细胞中诱导铁死亡,但在HepG2肝癌细胞系中没有。
● FIN:FIN会产生ROS,而BHT强烈抑制这种致命的ROS诱导的细胞死亡。FIN 化合物(II 类FIN)直接抑制GPX4活性而不会耗尽GSH。
● 丁硫氨酸亚砜亚胺 (BSO) :BSO抑制GSH合成,降低GPX活性和增加ROS水平,从而导致Ras突变细胞中的铁死亡。
● 兰哌酮: 兰哌酮可以通过诱导ROS选择性杀死K‑Ras突变的小鼠胚胎成纤维细胞,ROS是通过铁和Ras/RAF/MEK/ERK信号传导介导的。
● 丁硫氨酸亚砜亚胺 (BSO) :BSO抑制GSH合成,降低GPX活性和增加ROS水平,从而导致Ras突变细胞中的铁死亡。
● 柳氮磺胺吡啶:抑制NF‑κB信号通路,柳氮磺吡啶还抑制Xc‑系统转运蛋白,柳氮磺吡啶治疗癌细胞也会引发铁死亡。
● 索拉非尼:索拉非尼诱导某些癌细胞如肝细胞癌 (HCC) 细胞的铁死亡。Rb(原型肿瘤)和NRF2的表达可以抑制索拉非尼诱导的HCC铁死亡。索拉非尼在铁死亡中的机制和作用可能取决于Xc‑系统功能的抑制,而不是GPX4活性。
● 青蒿琥酯:青蒿琥酯选择性地诱导K‑Ras突变胰腺导管腺癌细胞 (PDAC) 细胞系的铁死亡,但不会诱导人胰腺导管上皮细胞或野生型K‑Ras PDAC细胞。 这个过程可以被铁螯合剂去铁胺阻断。
问题4,铁死亡在信号通路上是如何被调控的?
铁代谢和脂质过氧化信号越来越被认为是铁死亡的中心介质。此外,丝裂原活化蛋白激酶(MAPK)通路的激活还会导致癌细胞铁死亡。
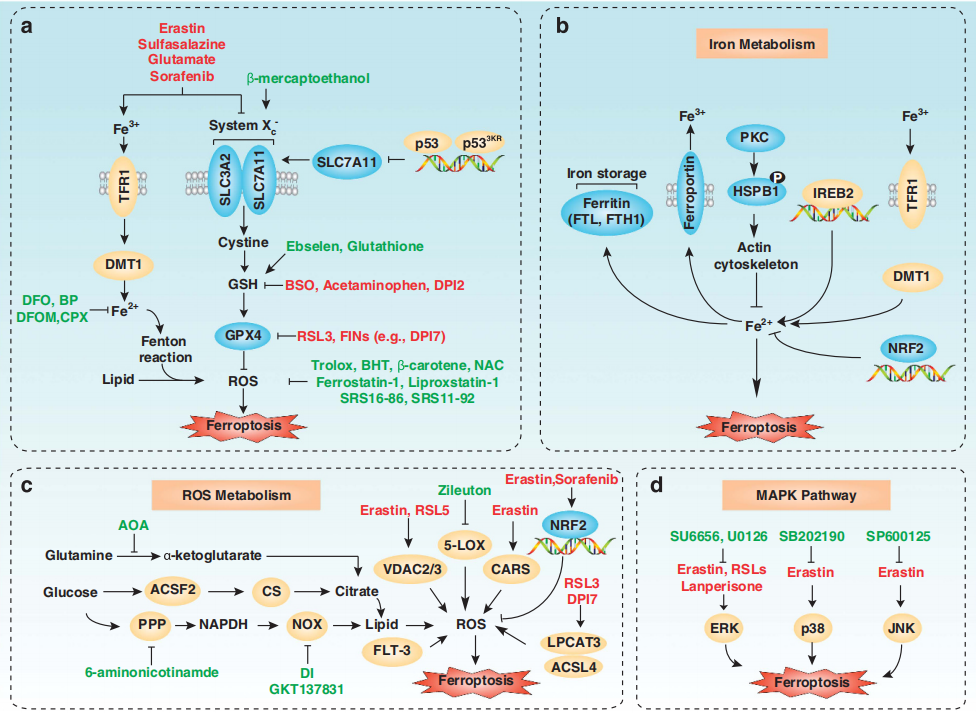
铁死亡的分子机制和信号通路 (a) 铁死亡的核心调节因子,(b–d) 铁代谢的作用
●Iron:过量的铁通过芬顿反应产生ROS导致铁死亡。与抗铁死亡细胞相比,具有 Ras 突变的铁死亡敏感细胞增加了TFR1并降低了铁蛋白(FTL和FTH1)的表达。这表明铁摄取增加和铁储存减少可能导致铁死亡期间的铁过载。事实上,铁螯合剂(如去铁胺、甲磺酸去铁胺、环吡酮胺)减少的铁超负荷抑制了erastin介导的铁死亡,而提供外源性铁源(如柠檬酸铁铵、柠檬酸铁和六水合氯化fe)会增强erastin诱导的死亡。IREB2是铁代谢的主要转录因子。RNAi 抑制IREB2 表达显著增加铁代谢相关基因表达并限制erastin诱导的铁死亡。因此,参与铁吸收和利用的细胞系统是铁死亡的诱导所必需的。
● ROS:通过 芬顿反应产生铁介导的ROS,烟酰胺腺嘌呤二核苷酸磷酸(NADPH)依赖性脂质过氧化和GSH耗竭对于铁死亡的诱导也很重要。GSH耗竭导致GPX4失活通过脂质过氧化产生的ROS积累引发铁死亡。线粒体脂肪酸代谢提供了铁死亡所需的特定脂质前体。ACSF2和CS是铁死亡中线粒体脂肪酸代谢所必需的。敲除ACSF2和CS可抑制erastin诱导的铁死亡。谷氨酰胺转化为α‑酮戊二酸还可产生脂质。这个过程可以被小分子转氨酶抑制剂氨基氧乙酸阻断。
ROS可以与脂质膜的多不饱和脂肪酸(PUFAs)反应并诱导脂质过氧化。GPX4 失活后,花生四烯酸 (AA) 和其他PUFAs的消耗是铁执死行亡所的必需的。GPX4 缺陷细胞表现出富含AA的氧化膜,这有助于铁死亡。用5‑、12‑和15‑氢过氧二十碳四烯酸 (HPETE) 处理)可加速铁死亡过程。甾醇载蛋体白2(一种用于线粒体的脂质转运蛋白)可挽救 GPX4-/- 细胞免于铁死亡。因此,铁死亡是由线粒体外脂质过氧化引发的,这与氧化脂质介质的释放有关。这些耐 Erastin 的 DU-145 细胞也对柳氮磺胺吡啶、索拉非尼和 RSL3 表现出耐药性,这表明耐药性不太可能是由于系统 Xc(-) 活性增加所致。
● MAPK:阻断 Ras/Raf/MEK/ERK 通路可抑制Ras突变癌细胞中erastin诱导的铁死亡。JNK和p38,对erastin诱导的白血病细胞死亡很重要。SP600125(一种抑制剂JNK 磷酸化)和SB202190(p38 活化抑制剂)降低了HL‑60细胞中由Erastin 诱导的细胞毒性。
问题5,铁死亡正负调控因子有哪些?
正调控因子
●Vdac2/3: VDAC2/3 在铁死亡中具有积极作用,因为敲低 VDAC2/3抑制了Ras 突变细胞中erastin诱导的铁死亡。
●Ras:Erastin 在Ras突变体细胞中表现出基因选择性杀伤力。一些正常的Ras野生型细胞,如肾小管细胞、T 细胞和成纤维细胞对erastin 敏感。
● TFR1: 与抗铁死亡细胞(如BJ细胞)相比,铁死亡敏感细胞(如BJeLR细胞)中 TFR1的表达为上调。相比之下,FTH1和FTL的表达在铁死亡敏感细胞(如BJeLR 细胞)中下调,表明铁储存也影响铁死亡。shRNA敲低TFR1可抑制Erastin诱导的BJeLR细胞铁死亡,证实抑制铁摄取可防止铁死亡。
● NOX:典型的NOX抑制剂diphenyleneiodonium和NOX1-/4特异性抑制剂 GKT137831部分抑制了Calu-1和HT1080细胞中erastin诱导的铁死亡。
●p53: 已发现 p53 的激活是某些癌细胞中铁死亡所必需的。这个过程依赖于 SLC7A11 的直接转录抑制,SLC7A11 是系统 Xc(-) 的关键组成部分
● CARS:敲低CARS可抑制erastin诱导的铁死亡,而过表达CARS可增强几种癌细胞对erastin的敏感性。
负调控因子
● GPX4:GPX4是RLS3的直接目标。GPX4的敲低以铁、MEK和ROS依赖性方式诱导铁死亡,而GPX4的过表达导致对RSL3的抗性。
●System Xc‑:System Xc‑在结构上由SLC7A11和SLC3A2组成。RNAi抑制 SLC7A11 表达增加了erastin的抗癌活性,而通过基因转染过表达SLC7A11减少了erastin诱导的铁死亡。
● HSPB1:在几种人类癌细胞中,在使用erastin处理后,转录因子热休克因子‑1 (HSF‑1)明显诱导 HSPB1表达。HSPB1的过表达抑制了erastin诱导的铁死亡。
● NRF2:NRF2在HCC细胞中具有抗铁死亡作用。NRF2和这些NRF2靶向基因的敲低加速了HCC细胞中Erastin或索拉非尼诱导的铁死亡。
问题6,铁死亡测定方法有哪些?
体外:
●细胞活力:钙黄乙酰氧甲酯(Calcein AM)活力测定、alamarBlue活力测定,台盼蓝试验和CCK8测定。
● 铁水平:Phen Green SK(PGSK)是一种细胞膜可渗透染料,用于通过流式细胞术或共聚焦显微镜监测活细胞中的细胞内铁水平。它显示PGSK在与足够的细胞铁结合后,在erastin处理后绿色自发荧光减弱。Iron Assay Kit 提供了一种简单方便的方法来测量样品中的亚铁和/或铁离子。
● ROS水平:细胞通过C11‑BODIPY探针长时间检测脂质过氧化并将荧光从红色变为绿色,而铁死亡抑制剂限制了这种转变。
体内:在小鼠中用RSL3和erastin治疗后,PTGS2编码环加氧酶2(COX‑2)显著上调。上调的PTGS2仅表明铁死亡开始,不影响铁死亡发展。组织和铁中铁
参考文献:
Xie Y, Hou W, Song X, Yu Y, Huang J, Sun X, Kang R, Tang D. Ferroptosis: process and function. Cell Death Differ. 2016 Mar;23(3):369-79. doi: 10.1038/cdd.2015.158. Epub 2016 Jan 22. PMID: 26794443; PMCID: PMC5072448.
【欢迎来电/邮件咨询】联系人:刘经理
电话:021-54376058
手机:13917998048 (7:00-24:00, 周末节假日不休)
邮箱:yanzaibio@yihaowan.cn, yanzaibio@163.com
官网:www.yihaowan.com.cn
地址: 上海市闵行区放鹤路1088号博济科技园6号楼109室






