研载生物科技(上海)有限公司
9 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
文献支持
血管生成实验
询价
公司新闻/正文
人血管类器官穿透人脑类器官形成血管样系统
775 人阅读发布时间:2022-05-16 11:22
二维培养不适合维持人体组织的结构和功能,因此近几年来类器官被开发并应用于药物发现和再生医学的研究,但随着类器官体积的增加,缺氧及代谢废物会导致组织坏死,因此类器官血管化在类器官研究过程中至关重要,此次为大家带来一篇关于人脑类器官血管化的研究。

以期的研究用培养的内皮细胞EC在皮质类器官中建立血管结构,但培养的EC缺乏小管发生和组织特异性,使其不太可能发育成血管,此外仅EC不能建立完整的血管结构。然而研究表明人类干细胞来源的人类血管类器官hBVO可以重建人类血管的结构和功能,但未研究其与其他细胞类型之间的相互作用,在此文章中,作者将hBVO解离成小团块,与皮质类器官共培养,以模拟胚胎神经血管的发育,结果显示hBVO在神经细胞系中具有血管化能力。
技术路线:
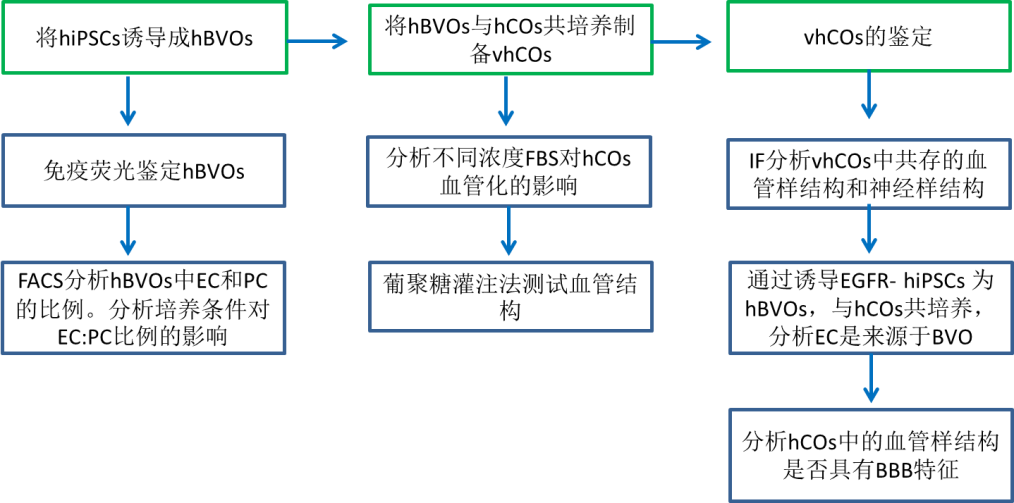
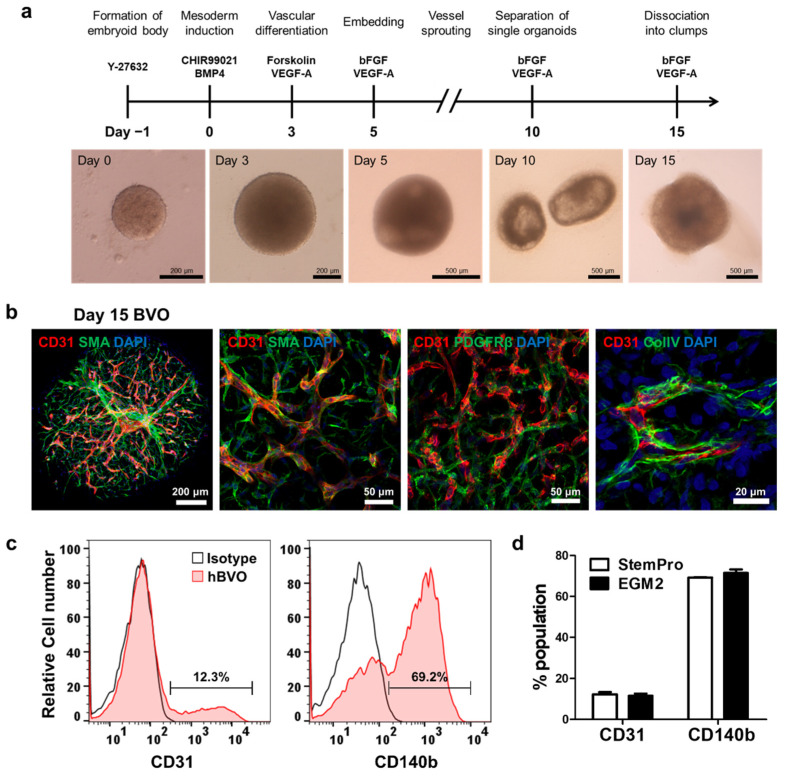
1. hBVOs的制备
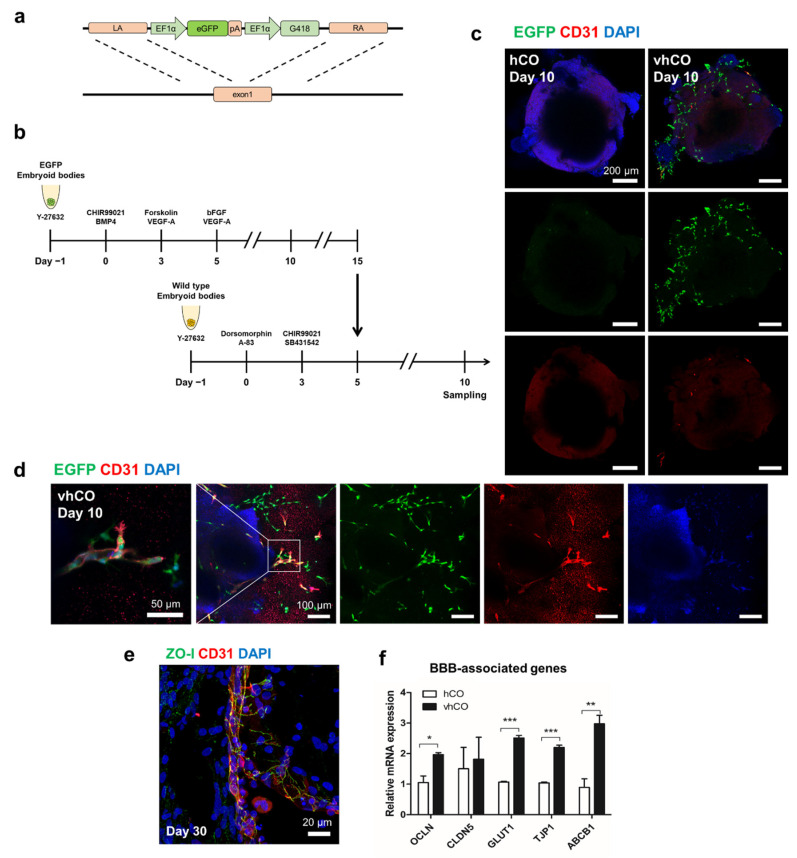
用CHIR99021 和BMP4将hiPSC诱导成中胚层后,用VEGF-A和forakolin诱导其分化成血管细胞,在第5天,将其被嵌入到含有VEGF-A和bFGF的Collagen I/Matrigel 溶液中。血管发生后,将hBVO分离成单个类器官。Confocal显示hBVO 中有网状CD31+ 内皮网络包裹在SMA+ SMC 或 PDGFRβ+ PC中,同时有collagen IV+ 基底膜。表明,2周内hiPSCs可分化成hBVOs,且由典型的血管细胞类型和细胞外基质组成。
在人大脑的血管中,PC与EC的比率是1:1,以维持BBB的完整性。但hBVO由12.3±1.8% 的EC和69.2±0.38% 的PC组成,PC大约是EC的5倍。为了增加 EC 的比例,作者通过将StemPro34培养基换为 EGM-2,但细胞比例没有改变。
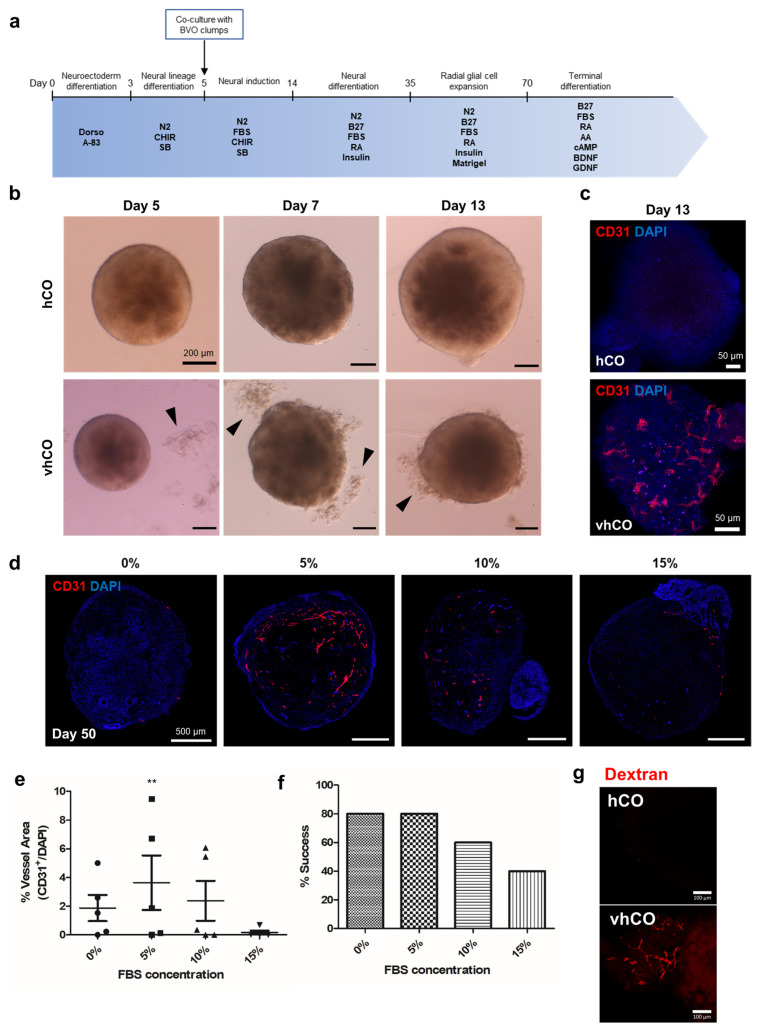
2. 脑类器官的血管化
为验证hBVO是否可以使脑类器官血管化。作者首先用accutase解离人脑类器官hCOs和hBVOs,用血细胞计数器计数后,将第15天的hBVO被解离成团块,以1:10的比例添加到第5天的hCOs中,在培养基中维持一段时间,再嵌入到培养基稀释的基质胶中。培养到第13天后,将类器官转移到摇床上培养。第13天的类器官表面即可检测到CD31+ 血管样细胞。说明hBVOs和hCOs的共培养形成了 vhCOs。
接者,作者优化了培养基中FBS 浓度。发现与其他浓度相比,5% FBS培养基中的 vhCOs 显示出更多的血管样网络。在0%和5% FBS条件下,80%的vhCOs在第50天成功形成CD31+ 内皮样网络。表明5% FBS对hCOs的血管化是最佳的。通过葡聚糖灌注实验,发现vhCOs中的管状结构清晰可见,而hCOs没有荧光信号,证明了在vhCOs中存在可灌注的血管网络。但这并不意味着vhCOs中的血管样结构具有血脑屏障BBB样通透性。
3. vhCO的鉴定
为了确定vhCO中的血管样管是否表现出血管的典型结构,在第30天对其进行了免疫荧光染色,发现内皮样管富含SMA + SMC样细胞,在其外围检测到PDGFRβ+ PC和collagen IV+ 基底膜。CD144+和KDR+内皮祖细胞样细胞也存在于vhCOs的血管样结构中。结合Confocal呈现的TUJ1+神经元细胞和CD31+ECs,表明vhCO一个由神经细胞和血管样结构组成的复杂系统。说明,hBVO在vhCOs中形成了典型的血管样结构,并可与神经样网络共存50天。
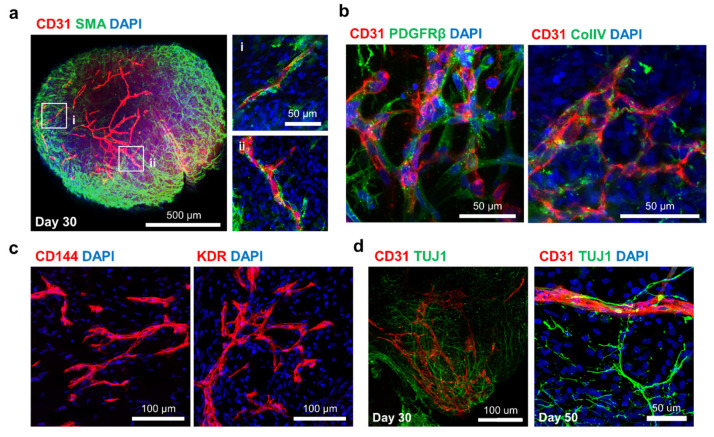
为确定EC是源自hBVO,作者将表达EGFP的iPSC诱导分化为hBVO,与hCOs培养3天后,EGFP+细胞存在于vhCOs的表面,但不存在于 hCOs 的表面。鉴于CD31+ECs均表达EGFP,而部分EGFP+细胞表达 CD31,该结果表明 vhCOs 中的血管网络来源于 hBVOs。
第30天ZO-1+紧密连接蛋白位于vhCO中的ECs之间。同时RT-qPCR显示,与hCO相比,紧密连接相关基因(Occludin、葡萄糖转运蛋白1、ABCB1和ZO-1)的表达水平在 vhCO 中显着上调。而GFAP+星形胶质细胞样细胞没有像体内神经血管系统一样覆盖 vhCOs 中的 CD31+内皮管。尽管vhCOs表达了与 BBB相关的紧密连接蛋白,但它并没有显示出类似内的形态学表型。
讨论:
作者的研究表明,hBVO可以渗入hCO形成血管化人脑类器官,vhCOs可以作为研究人类皮质发育和神经血管疾病的模型,亦可作为药物筛选和脑血管药效学的替代物。
【欢迎来电/邮件咨询】
电话:021-54376058
手机:18516646410/13917998048(微信同号)
邮箱:yanzaibio@yihaowan.cn, yanzaibio@163.com
地址: 上海市闵行区放鹤路1088号博济科技园6号楼109室

以期的研究用培养的内皮细胞EC在皮质类器官中建立血管结构,但培养的EC缺乏小管发生和组织特异性,使其不太可能发育成血管,此外仅EC不能建立完整的血管结构。然而研究表明人类干细胞来源的人类血管类器官hBVO可以重建人类血管的结构和功能,但未研究其与其他细胞类型之间的相互作用,在此文章中,作者将hBVO解离成小团块,与皮质类器官共培养,以模拟胚胎神经血管的发育,结果显示hBVO在神经细胞系中具有血管化能力。
技术路线:

1. hBVOs的制备
用CHIR99021 和BMP4将hiPSC诱导成中胚层后,用VEGF-A和forakolin诱导其分化成血管细胞,在第5天,将其被嵌入到含有VEGF-A和bFGF的Collagen I/Matrigel 溶液中。血管发生后,将hBVO分离成单个类器官。Confocal显示hBVO 中有网状CD31+ 内皮网络包裹在SMA+ SMC 或 PDGFRβ+ PC中,同时有collagen IV+ 基底膜。表明,2周内hiPSCs可分化成hBVOs,且由典型的血管细胞类型和细胞外基质组成。
在人大脑的血管中,PC与EC的比率是1:1,以维持BBB的完整性。但hBVO由12.3±1.8% 的EC和69.2±0.38% 的PC组成,PC大约是EC的5倍。为了增加 EC 的比例,作者通过将StemPro34培养基换为 EGM-2,但细胞比例没有改变。

2. 脑类器官的血管化
为验证hBVO是否可以使脑类器官血管化。作者首先用accutase解离人脑类器官hCOs和hBVOs,用血细胞计数器计数后,将第15天的hBVO被解离成团块,以1:10的比例添加到第5天的hCOs中,在培养基中维持一段时间,再嵌入到培养基稀释的基质胶中。培养到第13天后,将类器官转移到摇床上培养。第13天的类器官表面即可检测到CD31+ 血管样细胞。说明hBVOs和hCOs的共培养形成了 vhCOs。
接者,作者优化了培养基中FBS 浓度。发现与其他浓度相比,5% FBS培养基中的 vhCOs 显示出更多的血管样网络。在0%和5% FBS条件下,80%的vhCOs在第50天成功形成CD31+ 内皮样网络。表明5% FBS对hCOs的血管化是最佳的。通过葡聚糖灌注实验,发现vhCOs中的管状结构清晰可见,而hCOs没有荧光信号,证明了在vhCOs中存在可灌注的血管网络。但这并不意味着vhCOs中的血管样结构具有血脑屏障BBB样通透性。

3. vhCO的鉴定
为了确定vhCO中的血管样管是否表现出血管的典型结构,在第30天对其进行了免疫荧光染色,发现内皮样管富含SMA + SMC样细胞,在其外围检测到PDGFRβ+ PC和collagen IV+ 基底膜。CD144+和KDR+内皮祖细胞样细胞也存在于vhCOs的血管样结构中。结合Confocal呈现的TUJ1+神经元细胞和CD31+ECs,表明vhCO一个由神经细胞和血管样结构组成的复杂系统。说明,hBVO在vhCOs中形成了典型的血管样结构,并可与神经样网络共存50天。

为确定EC是源自hBVO,作者将表达EGFP的iPSC诱导分化为hBVO,与hCOs培养3天后,EGFP+细胞存在于vhCOs的表面,但不存在于 hCOs 的表面。鉴于CD31+ECs均表达EGFP,而部分EGFP+细胞表达 CD31,该结果表明 vhCOs 中的血管网络来源于 hBVOs。
第30天ZO-1+紧密连接蛋白位于vhCO中的ECs之间。同时RT-qPCR显示,与hCO相比,紧密连接相关基因(Occludin、葡萄糖转运蛋白1、ABCB1和ZO-1)的表达水平在 vhCO 中显着上调。而GFAP+星形胶质细胞样细胞没有像体内神经血管系统一样覆盖 vhCOs 中的 CD31+内皮管。尽管vhCOs表达了与 BBB相关的紧密连接蛋白,但它并没有显示出类似内的形态学表型。

讨论:
作者的研究表明,hBVO可以渗入hCO形成血管化人脑类器官,vhCOs可以作为研究人类皮质发育和神经血管疾病的模型,亦可作为药物筛选和脑血管药效学的替代物。
【欢迎来电/邮件咨询】
电话:021-54376058
手机:18516646410/13917998048(微信同号)
邮箱:yanzaibio@yihaowan.cn, yanzaibio@163.com
地址: 上海市闵行区放鹤路1088号博济科技园6号楼109室






