研载生物科技(上海)有限公司
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
【Redox Biol】11+高分文章,干细胞外泌体如何做铁死亡研究?值得观看!
2330 人阅读发布时间:2023-07-20 13:54
急性肺损伤是最早且最严重的一种脓毒症引起的并发症,巨噬细胞和肺微血管内皮细胞(PMVECs)是急性肺损伤最重要的介质和受害者。如何减轻PMVECs损伤,恢复细胞功能和血管完整性是脓毒症致急性肺损伤治疗的重要靶点。
据报道,铁死亡在癫痫发作、急性肝损伤、急性肺损伤等多种疾病的发生和发展中起着至关重要的作用。有研究报道,铁死亡与脓毒症患者常见的多器官功能障碍综合征(MODS)有关。

作为细胞间通讯的重要手段,ADSCs外泌体是损伤后组织修复和再生的重要介质。作者前期研究表明,ADSCs外泌体可以调控巨噬细胞和肺组织中的Keap1/Nrf2通路,从而对CLP诱导的肺损伤起到保护作用。然而,ADSCs外泌体是否可以通过Keap1/Nrf2/GPX4途径保护PMVECs形成铁凋亡尚不清楚。因此,作者在【Redox Biol】上发表的一篇题为“miR-125b-5p in adipose derived stem cells exosome alleviates pulmonary microvascular endothelial cells ferroptosis via Keap1/Nrf2/GPX4 in sepsis lung injury”的研究中,作者研究了ADSCs外泌体的抗氧化作用及其与Keap1/Nrf2/GPX4轴的关系。该研究揭示了ADSCs外泌体通过Keap1/Nrf2/GPX4轴缓解炎症诱导的PMVECs铁死亡并保护肺损伤免受败血症的影响。
研究结果
1.ADSCs和外泌体的表征
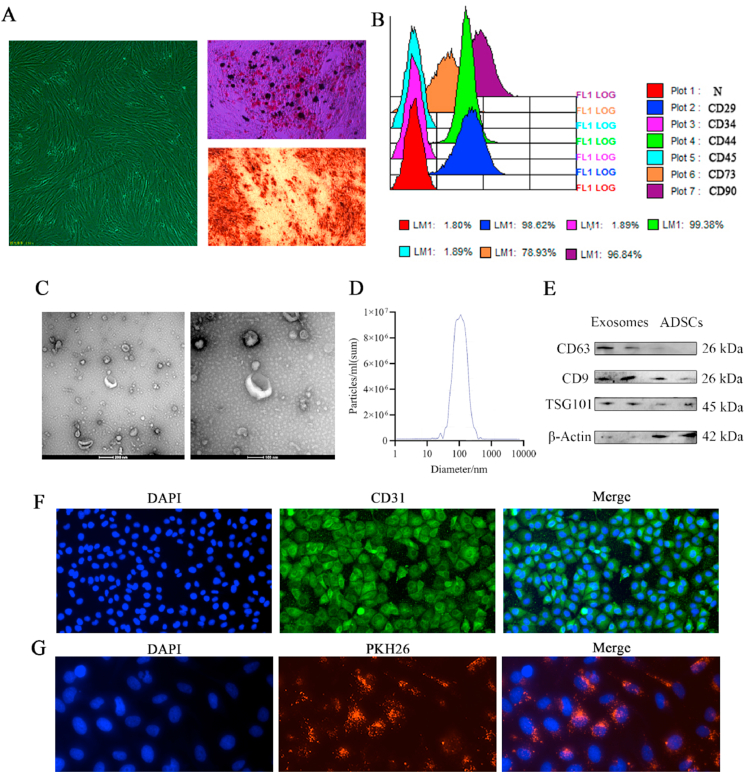
图1A:从脂肪组织中分离的原代ADSCs在倒置显微镜下呈纺锤状。
图1B:流式细胞术显示特异性间充质干细胞表面标志物 CD29、CD44、CD73、CD90在ADSCs中呈阳性表达,CD34和CD45几乎不表达。
图1C:透射电镜ADSCs外泌体呈现杯装典型外泌体形态。
图1D:NTA显示ADSCs外泌体直径在50-150nm之间,平均颗粒直径为117.5 nm。
图1E:Western Blot检测外泌体分子标记TSG-101、CD63和CD9高度表达。
图1F:免疫荧光染色结果显示,分离PMVECs的CD31染色呈阳性,表明成功分离PMVECs。
图1G:OKH67标记的ADSCs外泌体被PMVECs吸收。
2.ADSCs外泌体改善炎症反应诱导的PMVECs损伤
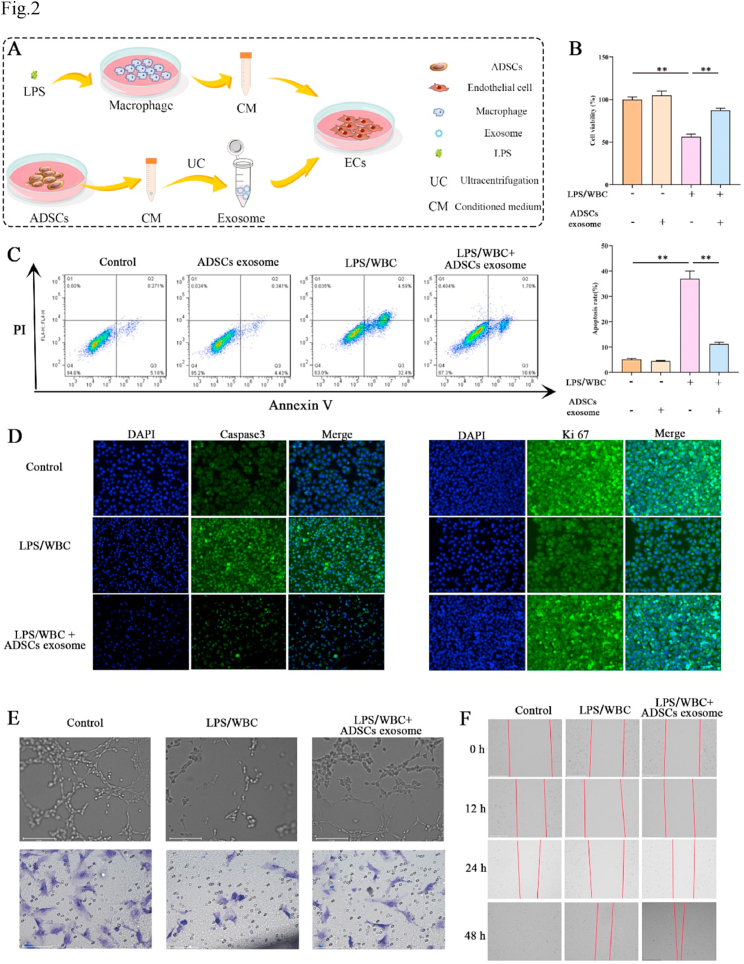
图2A:细胞实验示意图,将LPS诱导的RAW264.7细胞条件培养基(CM)加入PMVECs细胞中诱导损伤。同时,将ADSCs外泌体添加到PMVECs中以保护巨噬细胞CM诱导的损伤。
图2B:CCK8检测不同处理后PMVECs细胞活力,结果表明LPS诱导的巨噬细胞CM处理PMVECs的细胞活力减弱。
图2C:流式细胞术显示LPS诱导巨噬细胞CM处理PMVECs凋亡率显著高于未处理PMVECs。
图2D:不同处理PMVECs的Caspase3和Ki67免疫荧光染色,Caspase3免疫荧光结果验证巨噬细胞CM对PMVECs凋亡的上调作用和ADSCs的下调作用。用LPS诱导的巨噬细胞CM处理PMVECs时,Ki67的荧光强度降低,而使用ADSCs外泌体时Ki67的荧光强度升高。
图2E:不同处理PMVECs的血管生成和迁移检测。在成管实验中,巨噬细胞CM组的成管数量低于对照组和ADSCs外泌体组。
图2F:划痕实验显示不同处理后PMVECs有迁移。transwell和划痕实验显示,巨噬细胞CM损害了PMEVCs迁移能力,而ADSCs外泌体可以恢复迁移能力。
3.ADSCs外泌体减少PMVECs中炎症反应诱导的ROS积累
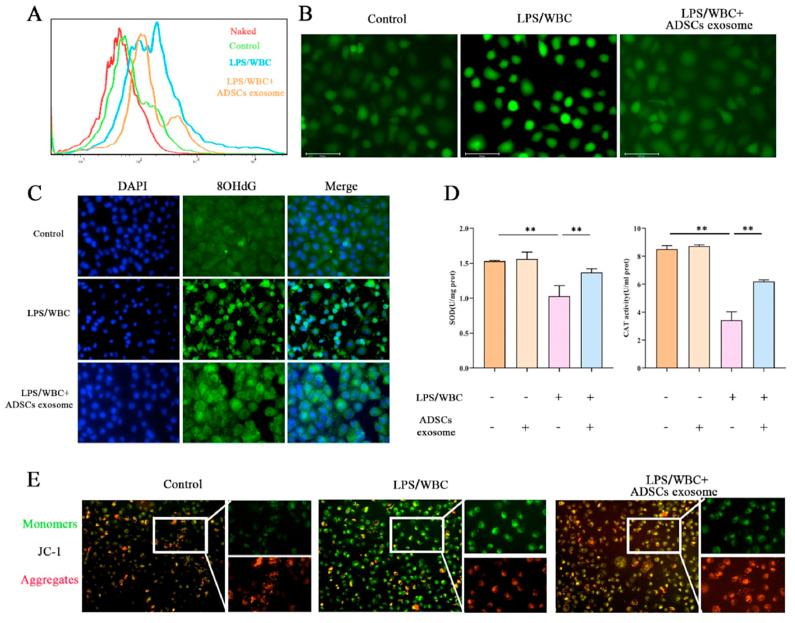
图3A:流式细胞术检测不同处理PMVECs的ROS含量。
图3B:不同处理PMVECs中ROS的免疫荧光检测。流式细胞术和免疫荧光结果显示,当PMVECs暴露于LPS诱导的巨噬细胞CM时,ROS的积累显著增加,而ADSCs外泌体则减缓了ROS的积累。
图3C:不同处理PMVECs的8OHdG免疫荧光染色,结果显示LPS诱导的巨噬细胞CM可增加PMVECs中8-OHdG表达,而ADSCs外泌体抵消了巨噬细胞CM的上调作用。
图3D:不同处理PMVECs中SOD和CAT含量。结果显示暴露于LPS诱导的巨噬细胞CM时,PMVECs中SOD含量和CAT活性降低,ADSCs外泌体可以提高PMVECs中SOD含量和CAT活性。
图3E:JC1染色显示不同处理PMVECs的线粒体膜电位,线粒体膜去极化后胞浆中JC-1单体形式的绿色荧光,线粒体中电位依赖性聚集的红色荧光。结果显示在对照组和ADSCs外泌体组,大部分线粒体显示红色荧光,而在LPS诱导的巨噬细胞CM中,荧光以绿色为主。即对照组和ADSCs外泌体组的MMP均高于CM组。
4.ADSCs外泌体减少PMVECs中炎症反应诱导的铁死亡
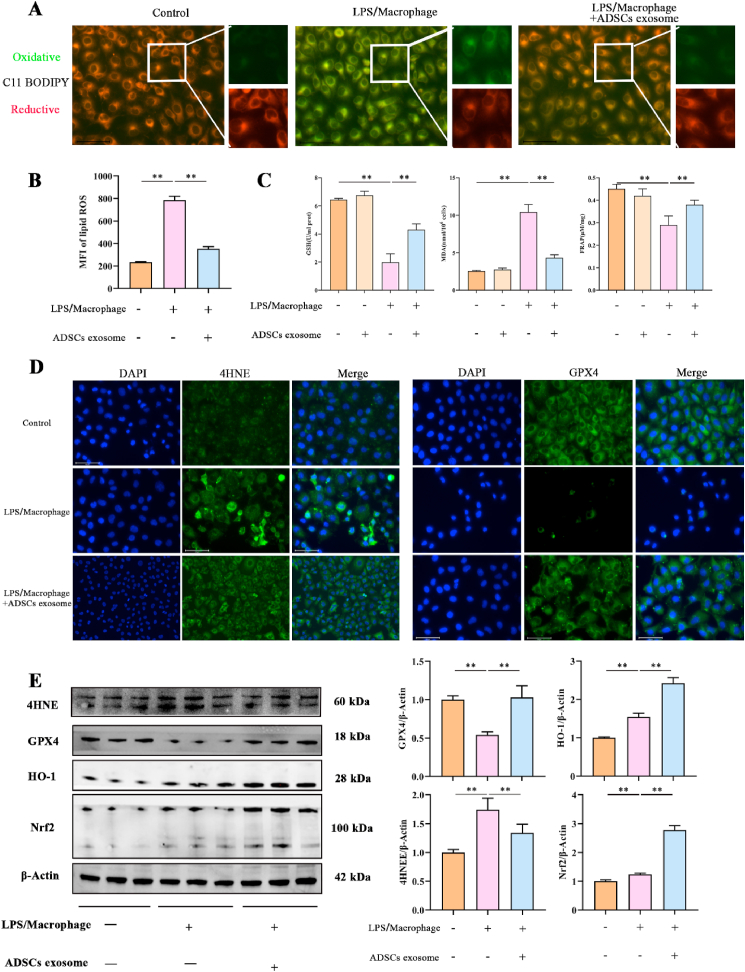
图4A:C11 BODIPY染色显示不同处理的PMVECs脂质过氧化,氧化质膜脂质荧光为绿色,还原性质膜脂质荧光为红色。
图4B:不同处理PMVECs脂质ROS的平均荧光强度。结果显示LPS诱导的巨噬细胞CM显著增加了PMVECs的脂质过氧化表达,而ADSCs外泌体则降低了表达。同样,LPS诱导的巨噬细胞CM和ADSCs外泌体对其他铁死亡相关指标也有相同的影响。
图4C:不同处理PMVECs中GSH、MDA、FRAP含量,结果显示LPS诱导巨噬细胞CM下调GSH和FRAP表达,增加MDA表达。但ADSCs外泌体可以减轻CM诱导的GSH和FRAP下调和MDA增加。
图4D:不同处理PMVECs的4HNE(左)和GPX4(右)免疫荧光染色,结果显示LPS诱导的巨噬细胞CM使4HNE的荧光强度增强,GPX4的荧光强度减弱。
图4E:Western blot检测不同处理PMVECs中4HNE、GPX4、HO-1、Nrf2的表达,结果证实LPS诱导巨噬细胞CM和ADSCs外泌体对4HNE和GPX4表达的调节作用相同。
5.ADSCs外泌体通过上调PMVECs中的GPX4来减轻炎症反应诱导的铁死亡
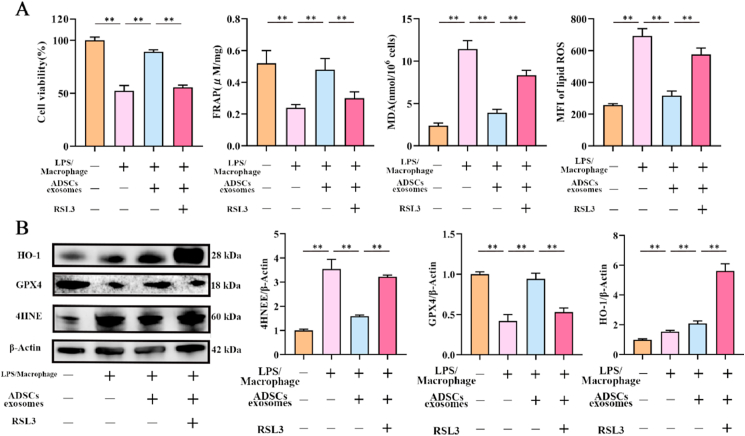
图5A:LPS/巨噬细胞、LPS/巨噬细胞+ ADSCs外泌体、LPS/巨噬细胞+ ADSCs外泌体+ RSL3处理PMVECs的细胞活力、FRAP、MDA和MFI含量的检测,结果显示当GPX4的表达被RSL3抑制时,即使ADSCs外泌体处理PMVEs,细胞活力和FRAP含量急剧下降。相反,当RSL3抑制GPX4表达时,脂质过氧化及其产物水平显著升高。
图5B:Western blot检测LPS/巨噬细胞、LPS/巨噬细胞+ ADSCs外泌体、LPS/巨噬细胞+ ADSCs外泌体+ RSL3处理PMVECs的4HNE、GPX4和HO-1表达。结果显示RSL3处理PMVECs后,4HNE和HO-1的表达明显升高,GPX4的表达明显抑制。当GPX4的表达被RSL3抑制时,ADSCs外泌体对炎症反应诱导的铁死亡的保护作用被取消。
6.ADSCs外泌体调控PMVECs中Nrf2通路的表达
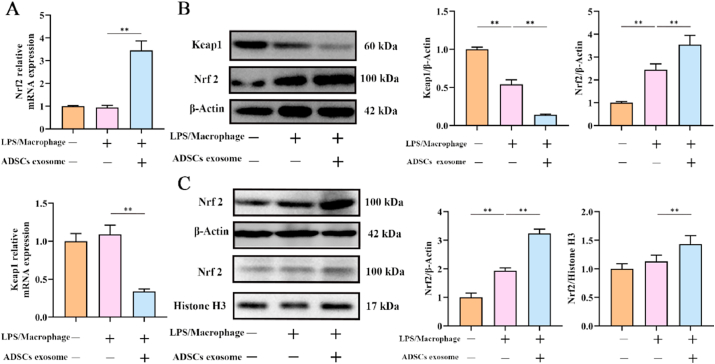
图6A:PCR检测不同PMVECs细胞中Nrf2和Keap1 mRNA的表达。
图6B:Western blot检测不同pmves细胞中Nrf2和Keap1蛋白表达。Western blot和PCR结果表明ADSCs外泌体可以增加Nrf2的表达,同时下调Nrf2负调控因子Keap1的表达。
图6C:Western blot检测不同PMVECs细胞质和细胞核中Nrf2的表达。结果显示ADSCs外泌体可以轻微增加细胞质中Nrf2的表达,而显著增加细胞核中Nrf2的表达。
7.ADSCs外泌体通过递送miR-125b-5p调控PMVECs中的Nrf2通路
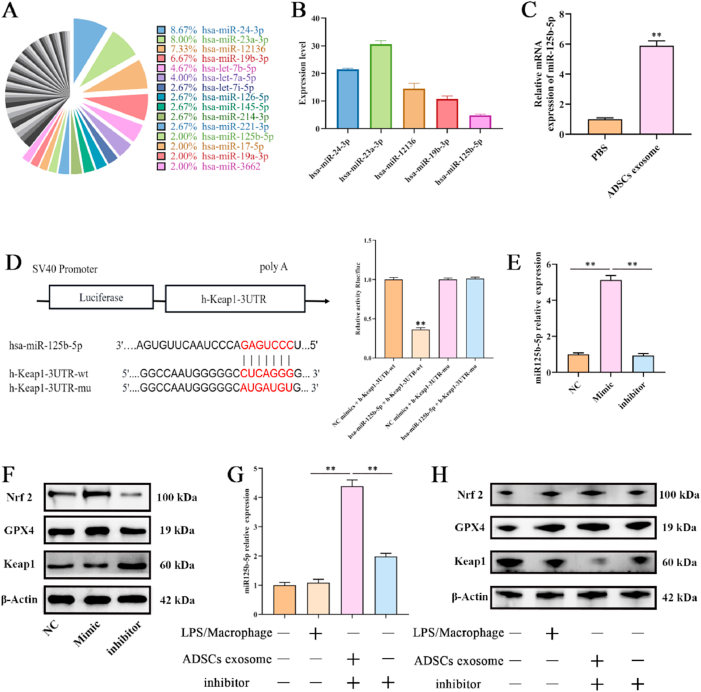
图7A:miRNA微阵列结果显示miRNAs在总miRNA读数中的相对百分比,在ADSCs外泌体中检测到多达63种已鉴定的miRNA。前15个最丰富的miRNA占一般以上。
图7B:PCR检测miR-24-3p、miR-23a-3p、miR-12136、miR-19b-3p和miR-125b-5p在ADSCs外泌体中的表达。
图7C:PCR检测miR-125b-5p在PBS和ADSCs外泌体处理的PMVECs中的表达。
图7D:双荧光素酶报告基因分析,验证miR-125b-5p对Keap1的调控作用。
图7E:PCR检测miR-125b-5p在NC、miR-125b-5p mimic和inhibitor处理的PMVECs中的表达。
图7F:Western blot检测在NC、miR-125b-5p mimic和inhibitor处理PMVECs中Keap1、Nrf2和GPX4的表达。
图7G: PCR检测miR-125b-5p在不同处理的PMVECs中表达。
图7H: Western blot检测在不同处理的PMVECs中Keap1、Nrf2和GPX4表达。结果表明当ADSCs外泌体中miR-125b-5p的表达被抑制剂抑制时, Keap1的下调和Nrf2和GPX4的上调得到缓解。
8.ADSCs外泌体减轻CLP诱导的小鼠急性肺损伤
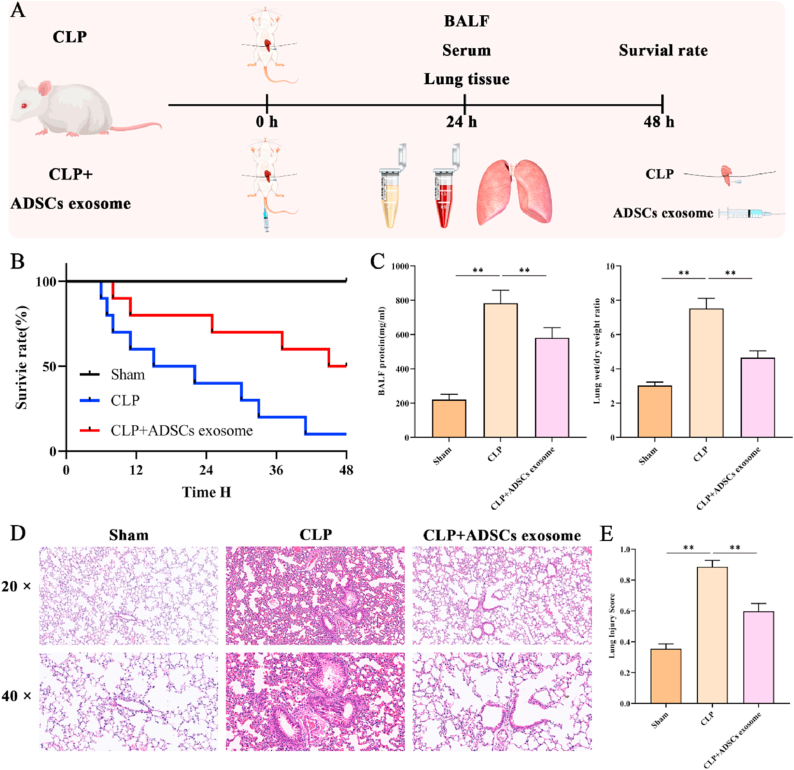
图8A:动物实验示意图,建立CLP脓毒症模型,并用ADSCs外泌体处理。
图8B:CLP和ADSCs外泌体对BALB/C小鼠的生存曲线,结果显示CLP组小鼠24 h死亡一半,48 h死亡80%。当用ADSCs外泌体处理时,死亡率在24小时下降到10%,在48小时下降到60%。
图8C:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织中BALF蛋白含量和干湿比,CLP组小鼠的BALF蛋白浓度和干湿比均显著高于sham组和ADSCs外泌体组。
图8D:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织HE染色,结果显示,与假手术组相比,CLP组肺泡毛细血管肿胀充血,肺泡腔出血,并伴有炎症细胞浸润。
图8E:CLP和ADSCs外泌体处理BALB/C小鼠肺组织肺损伤评分,CLP提高了小鼠肺损伤评分,而ADSCs外泌体降低了肺损伤评分。
9. ADSCs外泌体减轻CLP诱导的小鼠炎症反应
采用ELISA和PCR法检测小鼠肺组织和血清中炎症因子,MPO免疫组化染色、巨噬细胞标志物免疫荧光染色等方法检测小鼠CLP和ADSCs外泌体处理后的炎症反应。结果表明,ADSCs外泌体减轻了CLP诱导的小鼠炎症反应。
10.ADSCs外泌体可减轻CLP诱导的ROS并提高小鼠抗氧化能力
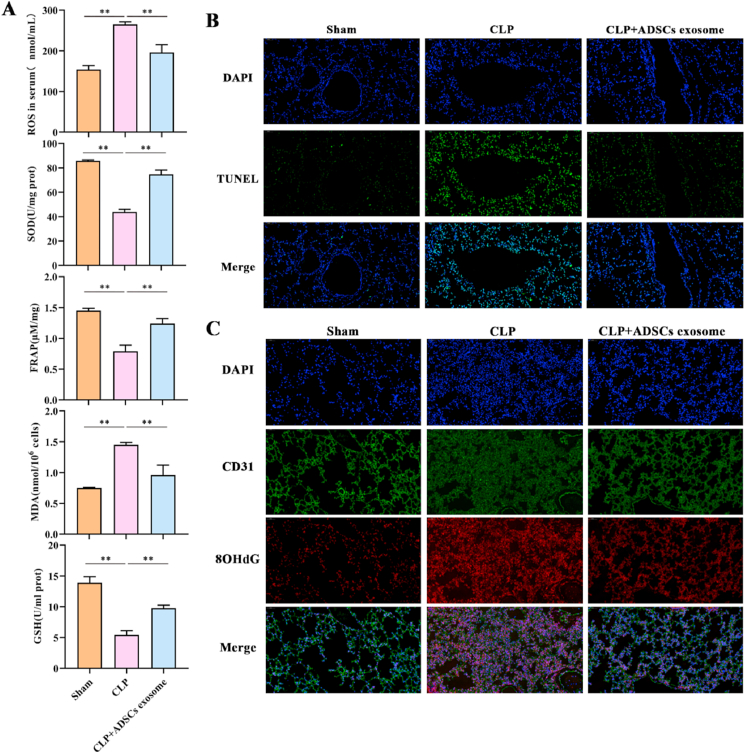
图9A:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织中ROS、SOD、FRAP、MDA和GSH含量。
图9B: CLP和ADSCs外泌体处理的BALB/C小鼠肺组织的TUNEL免疫荧光染色结果显示CLP增加小鼠肺组织的凋亡,而ADSCs外泌体减轻脓毒症大鼠肺组织的凋亡。
图9C:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织的CD31和8OHdG双免疫荧光染色显示CLP组CD31阳性细胞中8OHdG的表达明显升高,而ADSCs外泌体组表达低于CLP组。
11.ADSCs外泌体通过上调肺组织中的GPX4减轻CLP诱导的铁死亡
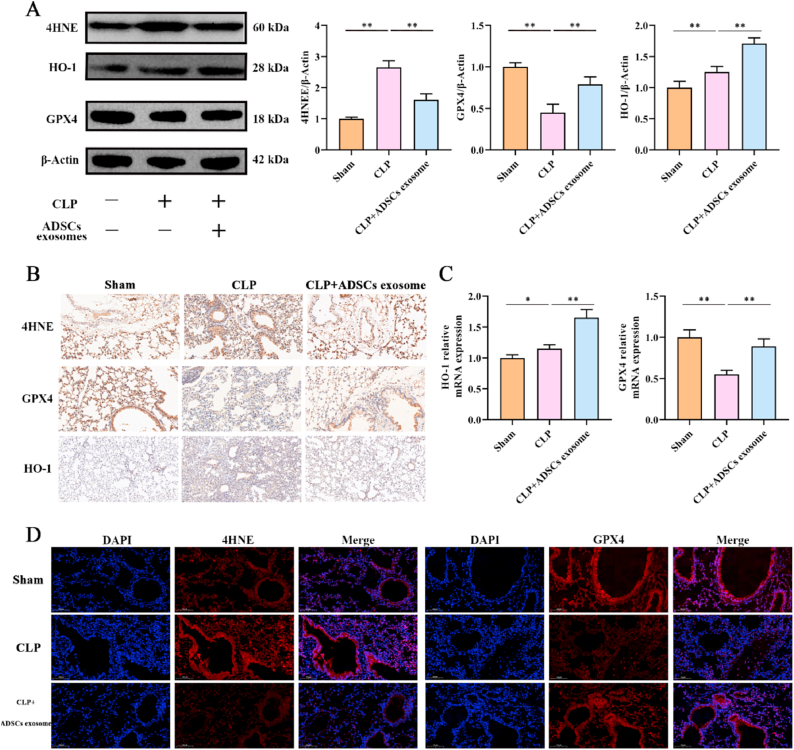
图10A:Western blot检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中4HNE、GPX4、HO-1的表达,结果显示CLP处理肺组织中4HNE蛋白表达显著增加,而ADSCs外泌体处理肺组织中4HNE蛋白表达显著降低。相反,当CLP处理GPX4时,GPX4的表达下调,而当添加ADSCs外泌体时,GPX4的表达上调。有趣的是CLP和ADSCs外泌体均可增加HO-1的表达,而ADSCs外泌体比CLP更能增加HO-1的表达。
图10B:分别用4HNE、GPX4和HO-1免疫组化染色检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中4HNE、GPX4和HO-1的表达,结果显示,CLP处理使肺组织中4HNE和HO-1阳性细胞增加,GPX4阳性细胞减少。
图10C:PCR检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中HO-1和GPX4 mRNA表达,结果显示CLP和ADSCs外泌体对HO-1和GPX4表达的调节作用相同。
图10D:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织中4HNE和GPX4免疫荧光染色,结果显示CLP增加了肺组织中4HNE的表达,降低了GPX4的表达,而ADSCs外泌体增加了GPX4的表达,降低了4HNE的表达。
12.ADSCs外泌体在CLP诱导的急性肺损伤中调控Keap1/Nrf2的表达
图11A:Western blot检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中Nrf2和Keap1的表达;PCR检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中Nrf2 RNA表达。
图11B:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织中Nrf2和CD31双免疫荧光染色结果。Nrf2免疫组化染色检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中Nrf2的表达。
总结
在本研究中,作者发现LPS刺激巨噬细胞CM诱导PMVECs损伤并增加铁死亡,而ADSCs外泌体可以减轻损伤并减少铁死亡。此外,在LPS刺激的巨噬细胞CM处理的PMVECs中,ADSCs外泌体上调GPX4的表达。进一步的GPX4抑制实验表明,ADSCs外泌体通过上调PMVECs中的GPX4来减轻炎症反应诱导的铁凋亡。同时,ADSCs外泌体可以增加GPX4的调节因子Nrf2的表达和核移位,降低Nrf2的负调节因子Keap1的表达。此外,miRNA分析表明,ADSCs外泌体中miR-125b-5p的富集抑制了Keap1的表达,减轻了铁死亡。在CLP诱导的脓毒症模型中,ADSCs外泌体可以减轻肺组织氧化应激损伤和铁上沉,同时显著增加Nrf2和GPX4的表达。总之,作者发现了一种新的潜在治疗机制,即通过ADSCs外泌体递送miR-125b-5p可以通过调节Keap1/Nrf2/GPX4的表达,减轻炎症诱导的脓毒症PMVECs铁死亡诱导的急性肺损伤,从而改善脓毒症急性肺损伤。
据报道,铁死亡在癫痫发作、急性肝损伤、急性肺损伤等多种疾病的发生和发展中起着至关重要的作用。有研究报道,铁死亡与脓毒症患者常见的多器官功能障碍综合征(MODS)有关。

作为细胞间通讯的重要手段,ADSCs外泌体是损伤后组织修复和再生的重要介质。作者前期研究表明,ADSCs外泌体可以调控巨噬细胞和肺组织中的Keap1/Nrf2通路,从而对CLP诱导的肺损伤起到保护作用。然而,ADSCs外泌体是否可以通过Keap1/Nrf2/GPX4途径保护PMVECs形成铁凋亡尚不清楚。因此,作者在【Redox Biol】上发表的一篇题为“miR-125b-5p in adipose derived stem cells exosome alleviates pulmonary microvascular endothelial cells ferroptosis via Keap1/Nrf2/GPX4 in sepsis lung injury”的研究中,作者研究了ADSCs外泌体的抗氧化作用及其与Keap1/Nrf2/GPX4轴的关系。该研究揭示了ADSCs外泌体通过Keap1/Nrf2/GPX4轴缓解炎症诱导的PMVECs铁死亡并保护肺损伤免受败血症的影响。
研究结果
1.ADSCs和外泌体的表征

图1A:从脂肪组织中分离的原代ADSCs在倒置显微镜下呈纺锤状。
图1B:流式细胞术显示特异性间充质干细胞表面标志物 CD29、CD44、CD73、CD90在ADSCs中呈阳性表达,CD34和CD45几乎不表达。
图1C:透射电镜ADSCs外泌体呈现杯装典型外泌体形态。
图1D:NTA显示ADSCs外泌体直径在50-150nm之间,平均颗粒直径为117.5 nm。
图1E:Western Blot检测外泌体分子标记TSG-101、CD63和CD9高度表达。
图1F:免疫荧光染色结果显示,分离PMVECs的CD31染色呈阳性,表明成功分离PMVECs。
图1G:OKH67标记的ADSCs外泌体被PMVECs吸收。
2.ADSCs外泌体改善炎症反应诱导的PMVECs损伤

图2A:细胞实验示意图,将LPS诱导的RAW264.7细胞条件培养基(CM)加入PMVECs细胞中诱导损伤。同时,将ADSCs外泌体添加到PMVECs中以保护巨噬细胞CM诱导的损伤。
图2B:CCK8检测不同处理后PMVECs细胞活力,结果表明LPS诱导的巨噬细胞CM处理PMVECs的细胞活力减弱。
图2C:流式细胞术显示LPS诱导巨噬细胞CM处理PMVECs凋亡率显著高于未处理PMVECs。
图2D:不同处理PMVECs的Caspase3和Ki67免疫荧光染色,Caspase3免疫荧光结果验证巨噬细胞CM对PMVECs凋亡的上调作用和ADSCs的下调作用。用LPS诱导的巨噬细胞CM处理PMVECs时,Ki67的荧光强度降低,而使用ADSCs外泌体时Ki67的荧光强度升高。
图2E:不同处理PMVECs的血管生成和迁移检测。在成管实验中,巨噬细胞CM组的成管数量低于对照组和ADSCs外泌体组。
图2F:划痕实验显示不同处理后PMVECs有迁移。transwell和划痕实验显示,巨噬细胞CM损害了PMEVCs迁移能力,而ADSCs外泌体可以恢复迁移能力。
3.ADSCs外泌体减少PMVECs中炎症反应诱导的ROS积累

图3A:流式细胞术检测不同处理PMVECs的ROS含量。
图3B:不同处理PMVECs中ROS的免疫荧光检测。流式细胞术和免疫荧光结果显示,当PMVECs暴露于LPS诱导的巨噬细胞CM时,ROS的积累显著增加,而ADSCs外泌体则减缓了ROS的积累。
图3C:不同处理PMVECs的8OHdG免疫荧光染色,结果显示LPS诱导的巨噬细胞CM可增加PMVECs中8-OHdG表达,而ADSCs外泌体抵消了巨噬细胞CM的上调作用。
图3D:不同处理PMVECs中SOD和CAT含量。结果显示暴露于LPS诱导的巨噬细胞CM时,PMVECs中SOD含量和CAT活性降低,ADSCs外泌体可以提高PMVECs中SOD含量和CAT活性。
图3E:JC1染色显示不同处理PMVECs的线粒体膜电位,线粒体膜去极化后胞浆中JC-1单体形式的绿色荧光,线粒体中电位依赖性聚集的红色荧光。结果显示在对照组和ADSCs外泌体组,大部分线粒体显示红色荧光,而在LPS诱导的巨噬细胞CM中,荧光以绿色为主。即对照组和ADSCs外泌体组的MMP均高于CM组。
4.ADSCs外泌体减少PMVECs中炎症反应诱导的铁死亡

图4A:C11 BODIPY染色显示不同处理的PMVECs脂质过氧化,氧化质膜脂质荧光为绿色,还原性质膜脂质荧光为红色。
图4B:不同处理PMVECs脂质ROS的平均荧光强度。结果显示LPS诱导的巨噬细胞CM显著增加了PMVECs的脂质过氧化表达,而ADSCs外泌体则降低了表达。同样,LPS诱导的巨噬细胞CM和ADSCs外泌体对其他铁死亡相关指标也有相同的影响。
图4C:不同处理PMVECs中GSH、MDA、FRAP含量,结果显示LPS诱导巨噬细胞CM下调GSH和FRAP表达,增加MDA表达。但ADSCs外泌体可以减轻CM诱导的GSH和FRAP下调和MDA增加。
图4D:不同处理PMVECs的4HNE(左)和GPX4(右)免疫荧光染色,结果显示LPS诱导的巨噬细胞CM使4HNE的荧光强度增强,GPX4的荧光强度减弱。
图4E:Western blot检测不同处理PMVECs中4HNE、GPX4、HO-1、Nrf2的表达,结果证实LPS诱导巨噬细胞CM和ADSCs外泌体对4HNE和GPX4表达的调节作用相同。
5.ADSCs外泌体通过上调PMVECs中的GPX4来减轻炎症反应诱导的铁死亡

图5A:LPS/巨噬细胞、LPS/巨噬细胞+ ADSCs外泌体、LPS/巨噬细胞+ ADSCs外泌体+ RSL3处理PMVECs的细胞活力、FRAP、MDA和MFI含量的检测,结果显示当GPX4的表达被RSL3抑制时,即使ADSCs外泌体处理PMVEs,细胞活力和FRAP含量急剧下降。相反,当RSL3抑制GPX4表达时,脂质过氧化及其产物水平显著升高。
图5B:Western blot检测LPS/巨噬细胞、LPS/巨噬细胞+ ADSCs外泌体、LPS/巨噬细胞+ ADSCs外泌体+ RSL3处理PMVECs的4HNE、GPX4和HO-1表达。结果显示RSL3处理PMVECs后,4HNE和HO-1的表达明显升高,GPX4的表达明显抑制。当GPX4的表达被RSL3抑制时,ADSCs外泌体对炎症反应诱导的铁死亡的保护作用被取消。
6.ADSCs外泌体调控PMVECs中Nrf2通路的表达

图6A:PCR检测不同PMVECs细胞中Nrf2和Keap1 mRNA的表达。
图6B:Western blot检测不同pmves细胞中Nrf2和Keap1蛋白表达。Western blot和PCR结果表明ADSCs外泌体可以增加Nrf2的表达,同时下调Nrf2负调控因子Keap1的表达。
图6C:Western blot检测不同PMVECs细胞质和细胞核中Nrf2的表达。结果显示ADSCs外泌体可以轻微增加细胞质中Nrf2的表达,而显著增加细胞核中Nrf2的表达。
7.ADSCs外泌体通过递送miR-125b-5p调控PMVECs中的Nrf2通路

图7A:miRNA微阵列结果显示miRNAs在总miRNA读数中的相对百分比,在ADSCs外泌体中检测到多达63种已鉴定的miRNA。前15个最丰富的miRNA占一般以上。
图7B:PCR检测miR-24-3p、miR-23a-3p、miR-12136、miR-19b-3p和miR-125b-5p在ADSCs外泌体中的表达。
图7C:PCR检测miR-125b-5p在PBS和ADSCs外泌体处理的PMVECs中的表达。
图7D:双荧光素酶报告基因分析,验证miR-125b-5p对Keap1的调控作用。
图7E:PCR检测miR-125b-5p在NC、miR-125b-5p mimic和inhibitor处理的PMVECs中的表达。
图7F:Western blot检测在NC、miR-125b-5p mimic和inhibitor处理PMVECs中Keap1、Nrf2和GPX4的表达。
图7G: PCR检测miR-125b-5p在不同处理的PMVECs中表达。
图7H: Western blot检测在不同处理的PMVECs中Keap1、Nrf2和GPX4表达。结果表明当ADSCs外泌体中miR-125b-5p的表达被抑制剂抑制时, Keap1的下调和Nrf2和GPX4的上调得到缓解。
8.ADSCs外泌体减轻CLP诱导的小鼠急性肺损伤

图8A:动物实验示意图,建立CLP脓毒症模型,并用ADSCs外泌体处理。
图8B:CLP和ADSCs外泌体对BALB/C小鼠的生存曲线,结果显示CLP组小鼠24 h死亡一半,48 h死亡80%。当用ADSCs外泌体处理时,死亡率在24小时下降到10%,在48小时下降到60%。
图8C:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织中BALF蛋白含量和干湿比,CLP组小鼠的BALF蛋白浓度和干湿比均显著高于sham组和ADSCs外泌体组。
图8D:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织HE染色,结果显示,与假手术组相比,CLP组肺泡毛细血管肿胀充血,肺泡腔出血,并伴有炎症细胞浸润。
图8E:CLP和ADSCs外泌体处理BALB/C小鼠肺组织肺损伤评分,CLP提高了小鼠肺损伤评分,而ADSCs外泌体降低了肺损伤评分。
9. ADSCs外泌体减轻CLP诱导的小鼠炎症反应
采用ELISA和PCR法检测小鼠肺组织和血清中炎症因子,MPO免疫组化染色、巨噬细胞标志物免疫荧光染色等方法检测小鼠CLP和ADSCs外泌体处理后的炎症反应。结果表明,ADSCs外泌体减轻了CLP诱导的小鼠炎症反应。
10.ADSCs外泌体可减轻CLP诱导的ROS并提高小鼠抗氧化能力

图9A:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织中ROS、SOD、FRAP、MDA和GSH含量。
图9B: CLP和ADSCs外泌体处理的BALB/C小鼠肺组织的TUNEL免疫荧光染色结果显示CLP增加小鼠肺组织的凋亡,而ADSCs外泌体减轻脓毒症大鼠肺组织的凋亡。
图9C:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织的CD31和8OHdG双免疫荧光染色显示CLP组CD31阳性细胞中8OHdG的表达明显升高,而ADSCs外泌体组表达低于CLP组。
11.ADSCs外泌体通过上调肺组织中的GPX4减轻CLP诱导的铁死亡

图10A:Western blot检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中4HNE、GPX4、HO-1的表达,结果显示CLP处理肺组织中4HNE蛋白表达显著增加,而ADSCs外泌体处理肺组织中4HNE蛋白表达显著降低。相反,当CLP处理GPX4时,GPX4的表达下调,而当添加ADSCs外泌体时,GPX4的表达上调。有趣的是CLP和ADSCs外泌体均可增加HO-1的表达,而ADSCs外泌体比CLP更能增加HO-1的表达。
图10B:分别用4HNE、GPX4和HO-1免疫组化染色检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中4HNE、GPX4和HO-1的表达,结果显示,CLP处理使肺组织中4HNE和HO-1阳性细胞增加,GPX4阳性细胞减少。
图10C:PCR检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中HO-1和GPX4 mRNA表达,结果显示CLP和ADSCs外泌体对HO-1和GPX4表达的调节作用相同。
图10D:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织中4HNE和GPX4免疫荧光染色,结果显示CLP增加了肺组织中4HNE的表达,降低了GPX4的表达,而ADSCs外泌体增加了GPX4的表达,降低了4HNE的表达。
12.ADSCs外泌体在CLP诱导的急性肺损伤中调控Keap1/Nrf2的表达
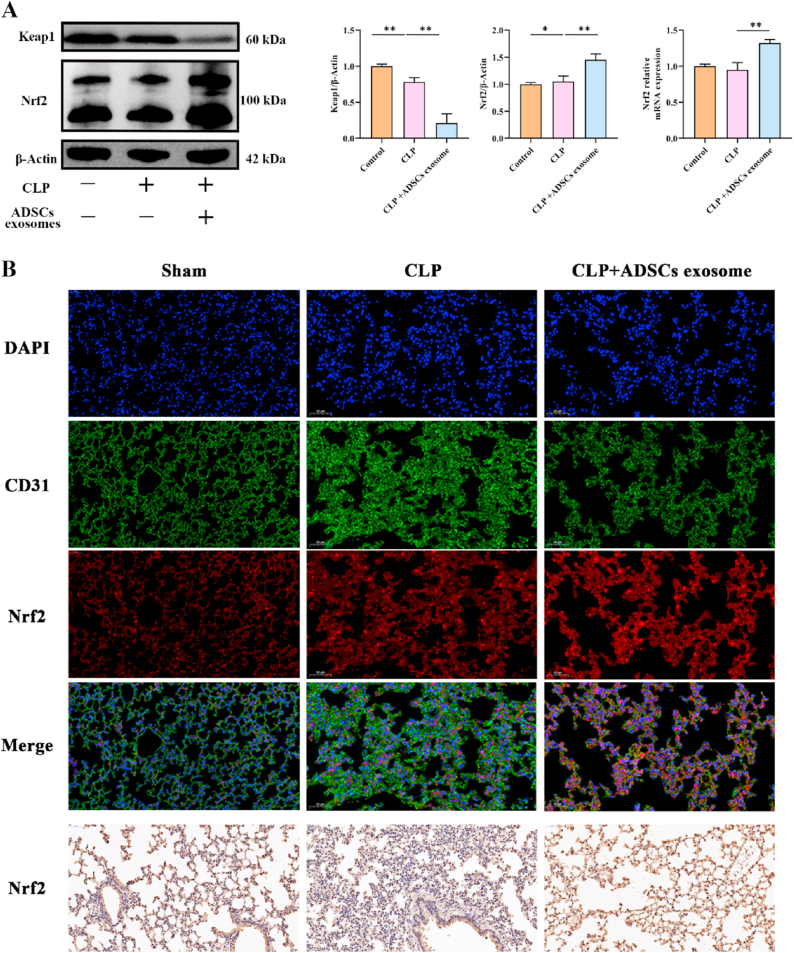

图11A:Western blot检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中Nrf2和Keap1的表达;PCR检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中Nrf2 RNA表达。
图11B:CLP和ADSCs外泌体处理的BALB/C小鼠肺组织中Nrf2和CD31双免疫荧光染色结果。Nrf2免疫组化染色检测CLP和ADSCs外泌体处理BALB/C小鼠肺组织中Nrf2的表达。
总结
在本研究中,作者发现LPS刺激巨噬细胞CM诱导PMVECs损伤并增加铁死亡,而ADSCs外泌体可以减轻损伤并减少铁死亡。此外,在LPS刺激的巨噬细胞CM处理的PMVECs中,ADSCs外泌体上调GPX4的表达。进一步的GPX4抑制实验表明,ADSCs外泌体通过上调PMVECs中的GPX4来减轻炎症反应诱导的铁凋亡。同时,ADSCs外泌体可以增加GPX4的调节因子Nrf2的表达和核移位,降低Nrf2的负调节因子Keap1的表达。此外,miRNA分析表明,ADSCs外泌体中miR-125b-5p的富集抑制了Keap1的表达,减轻了铁死亡。在CLP诱导的脓毒症模型中,ADSCs外泌体可以减轻肺组织氧化应激损伤和铁上沉,同时显著增加Nrf2和GPX4的表达。总之,作者发现了一种新的潜在治疗机制,即通过ADSCs外泌体递送miR-125b-5p可以通过调节Keap1/Nrf2/GPX4的表达,减轻炎症诱导的脓毒症PMVECs铁死亡诱导的急性肺损伤,从而改善脓毒症急性肺损伤。






