研载生物科技(上海)有限公司
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
综述:【J Extracell Vesicles】16+,组织外泌体在肿瘤及非肿瘤性疾病中的进展
624 人阅读发布时间:2023-09-13 17:24
Ti - EVs存在于组织间质中,在细胞间通讯中起关键作用,与从体液或细胞培养上清液中获得的EVs相比,直接从组织中分离的EVs具有组织特异性、准确反映组织微环境等优点。今天湾湾分享一篇关于组织源性EVs的综述文章,发表在【J Extracell Vesicles】杂志上题为“Tissue‐derived extracellular vesicles in cancers and non‐cancer diseases: Present and future”,该综述总结了Ti - EVs治疗癌症和非癌症疾病的新进展。提出了Ti - EVs在基础研究和临床实践中的应用前景。回顾和比较了癌症和非癌症疾病之间Ti - EVs分离和表征的工作流程。

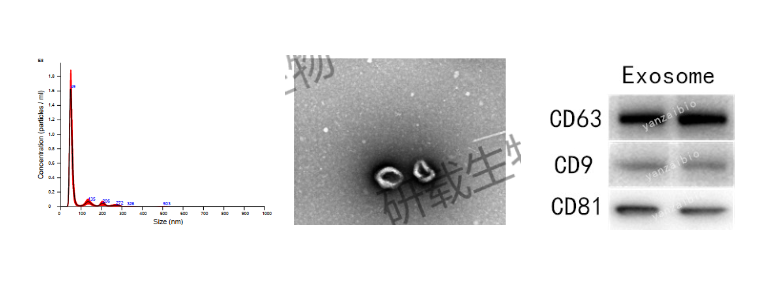
研载生物外泌体提取方面具有丰富的经验,可以处理不同类型样本,包括细胞上清、血浆/血清、体液、组织、植物等。在组织源性外泌体方面已成功进行脑、心、肝、脾、肺、肾、海洋组织等外泌体提取,并通过粒径分析、透射电镜、Western Blot鉴定符合外泌体表征特性。
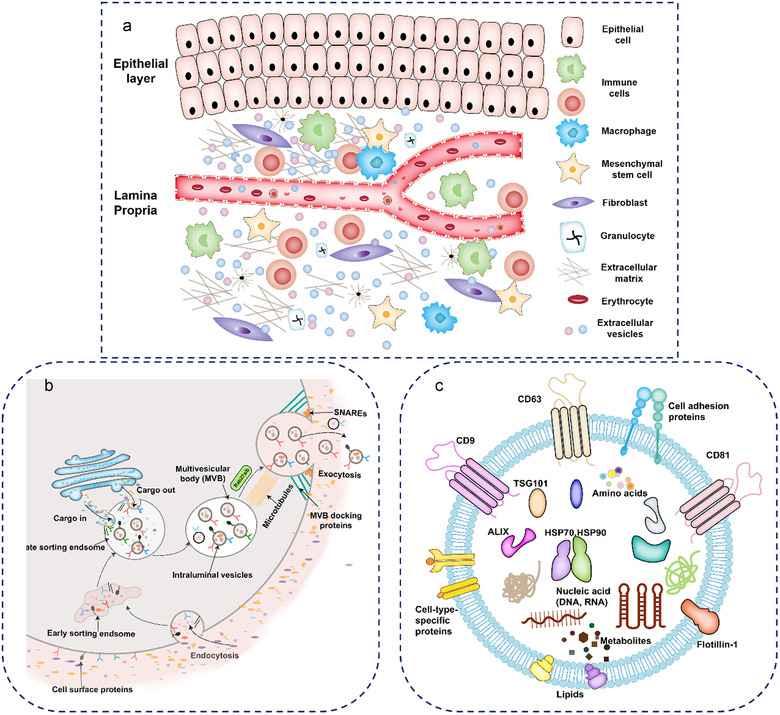
1.组织源性EVs的生物发生和鉴定(如图1)。
由于一些有利的特性,Ti-EVs越来越受到关注。 Ti‐EVs由组织微环境中大多数细胞类型脱落的囊泡组成,特别是TME,并且更准确地反映细胞的病理生理特征和行为,因为组织的三维(3D)结构和细胞特性被保留;利用从肿瘤和邻近非肿瘤组织中获得的具有共同生物学特性的EVs, Ti - EVs分析可以比较EVs成分;与体液来源的EVs相比,Ti - EVs样品含有最少的污染物,因为它是单一的组织来源;尚未充分探索肿瘤内异质性(ITH)与肿瘤进化的潜在相关性。对多个地点和不同疾病演变阶段取样的Ti -EVs进行分析,可能有助于了解TME的时空异质性。就癌症而言,Ti‐EVs可能对调节肿瘤细胞定植和生长的TME至关重要。
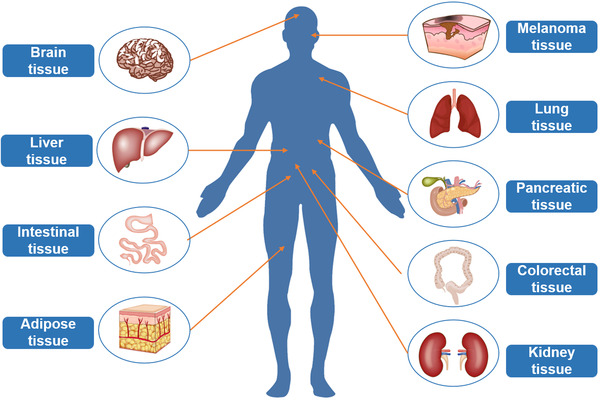
2.组织源性 Ti‐EVs研究中涉及的组织类型(如图2)
左侧部分展示了一些与非癌症疾病有关的组织类型,包括脑组织(主要是阿尔茨海默病)、用于 Ti‐EVs分离标准方案的肝组织、肠组织和一些代谢性疾病的脂肪组织。另一部分是一些与癌症相关的组织,包括黑色素瘤、肺癌、胰腺癌、结直肠癌和肾细胞癌等。组织Ti-EVs是某种疾病所特有的,对其内容物的成分分析,如蛋白组学、RNA测序可以用于疾病的早期诊断;由于Ti‐EVs可以实现疾病发展的多阶段,多点位取样,所以可以检测疾病的进展。
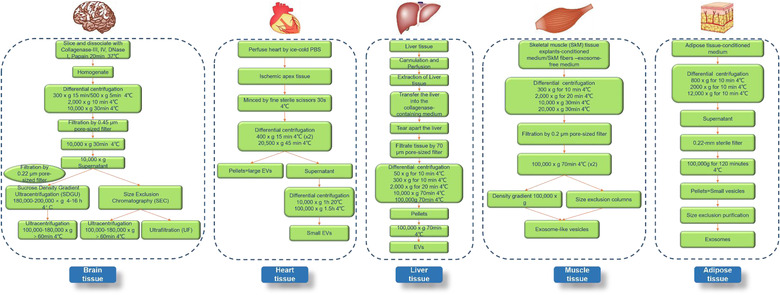
3.多种癌症组织(图3)和非癌组织(图4)中EVs分离方法
a.用于从多种类型的癌症组织中分离细胞外囊泡(EVs)的方案示意图概述
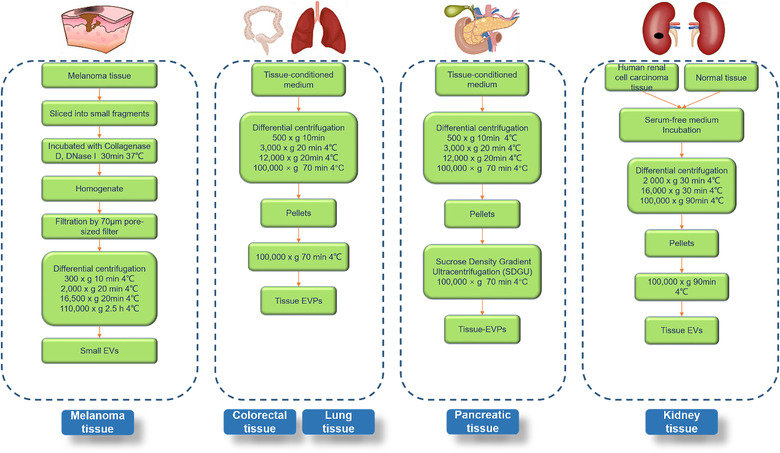
b.从多个非癌组织中分离细胞外囊泡(ev)的方法概述
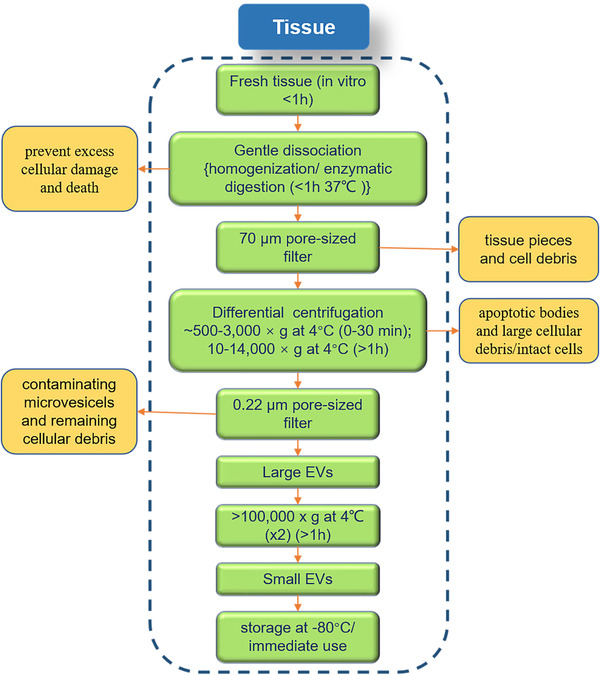
4.常用的Ti-EVs分离方法(图5)
常用的方法可用于从多种类型的组织中提取Ti-EVs。组织样品在解剖后立即用温和的机械力或酶处理,1小时被认为是有利的持续时间;在4°C下,以~ 500 -3000g的速度离心,可以去除凋亡小体和大细胞碎片/完整细胞;在4℃条件下,以10 ~ 14000 g的速度离心,然后通过0.22 μm的过滤器,去除任何污染的微囊泡和残留的细胞碎片后,可以获得大的EVs;在4°C下,超离心速度超过100,000g,该过程应超过1 h;最后,提取的Ti‐EVs可以立即使用或在- 80°C下保存数年。
研载生物能够为您提供包括外泌体、m6A甲基化、细胞焦亡、铁死亡、IncRNA、circRNA、细胞、分子实验、动物模型、组织病理学等多项基础医学科研技术服务,并建立了涵盖实验设计、项目实施、结果整理、数据分析及策略咨询等一站式的科研服务体系。
联系方式:
电话:18516646410
13917998408
座机:021-54376058
Q Q:2195165458
欢迎咨询~


研载生物外泌体提取方面具有丰富的经验,可以处理不同类型样本,包括细胞上清、血浆/血清、体液、组织、植物等。在组织源性外泌体方面已成功进行脑、心、肝、脾、肺、肾、海洋组织等外泌体提取,并通过粒径分析、透射电镜、Western Blot鉴定符合外泌体表征特性。

1.组织源性EVs的生物发生和鉴定(如图1)。
由于一些有利的特性,Ti-EVs越来越受到关注。 Ti‐EVs由组织微环境中大多数细胞类型脱落的囊泡组成,特别是TME,并且更准确地反映细胞的病理生理特征和行为,因为组织的三维(3D)结构和细胞特性被保留;利用从肿瘤和邻近非肿瘤组织中获得的具有共同生物学特性的EVs, Ti - EVs分析可以比较EVs成分;与体液来源的EVs相比,Ti - EVs样品含有最少的污染物,因为它是单一的组织来源;尚未充分探索肿瘤内异质性(ITH)与肿瘤进化的潜在相关性。对多个地点和不同疾病演变阶段取样的Ti -EVs进行分析,可能有助于了解TME的时空异质性。就癌症而言,Ti‐EVs可能对调节肿瘤细胞定植和生长的TME至关重要。

2.组织源性 Ti‐EVs研究中涉及的组织类型(如图2)
左侧部分展示了一些与非癌症疾病有关的组织类型,包括脑组织(主要是阿尔茨海默病)、用于 Ti‐EVs分离标准方案的肝组织、肠组织和一些代谢性疾病的脂肪组织。另一部分是一些与癌症相关的组织,包括黑色素瘤、肺癌、胰腺癌、结直肠癌和肾细胞癌等。组织Ti-EVs是某种疾病所特有的,对其内容物的成分分析,如蛋白组学、RNA测序可以用于疾病的早期诊断;由于Ti‐EVs可以实现疾病发展的多阶段,多点位取样,所以可以检测疾病的进展。

3.多种癌症组织(图3)和非癌组织(图4)中EVs分离方法
a.用于从多种类型的癌症组织中分离细胞外囊泡(EVs)的方案示意图概述

b.从多个非癌组织中分离细胞外囊泡(ev)的方法概述

4.常用的Ti-EVs分离方法(图5)
常用的方法可用于从多种类型的组织中提取Ti-EVs。组织样品在解剖后立即用温和的机械力或酶处理,1小时被认为是有利的持续时间;在4°C下,以~ 500 -3000g的速度离心,可以去除凋亡小体和大细胞碎片/完整细胞;在4℃条件下,以10 ~ 14000 g的速度离心,然后通过0.22 μm的过滤器,去除任何污染的微囊泡和残留的细胞碎片后,可以获得大的EVs;在4°C下,超离心速度超过100,000g,该过程应超过1 h;最后,提取的Ti‐EVs可以立即使用或在- 80°C下保存数年。

研载生物能够为您提供包括外泌体、m6A甲基化、细胞焦亡、铁死亡、IncRNA、circRNA、细胞、分子实验、动物模型、组织病理学等多项基础医学科研技术服务,并建立了涵盖实验设计、项目实施、结果整理、数据分析及策略咨询等一站式的科研服务体系。
联系方式:
电话:18516646410
13917998408
座机:021-54376058
Q Q:2195165458
欢迎咨询~







