研载生物科技(上海)有限公司
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
【Adv Sci】15+,外泌体转移LINC00668通过促进炎症性肠病NETs形成促进血栓形成
2175 人阅读发布时间:2023-11-06 15:22
流行病学研究显示炎症性肠病(IBD)与血栓形成风险增加之间存在关联。然而,IBD如何影响血栓形成仍然未知。目前的研究表明,在葡聚糖硫酸钠(DSS)诱导的IBD小鼠中,中性粒细胞细胞外陷阱(NETs)的形成显著增加,这反过来又以NETs依赖的方式促进血栓形成。湾湾今天分享的是一篇发表在【Advanced Science】上的题为“Exosomes-transferred LINC00668 Contributes to Thrombosis by Promoting NETs Formation in Inflammatory Bowel Disease”的研究,在本研究中,作者假设炎症肠上皮细胞(IEC)分泌的外泌体可能通过诱导NETs的释放来促进血栓形成。作者确定了负责外泌体诱导NETs形成的重要生物分子,并探索了IEC衍生的外泌体如何促进NETs形成和血栓形成的潜在机制。

研究结果
1.DSS诱导肠道炎症小鼠血栓形成增加与NETs形成相关
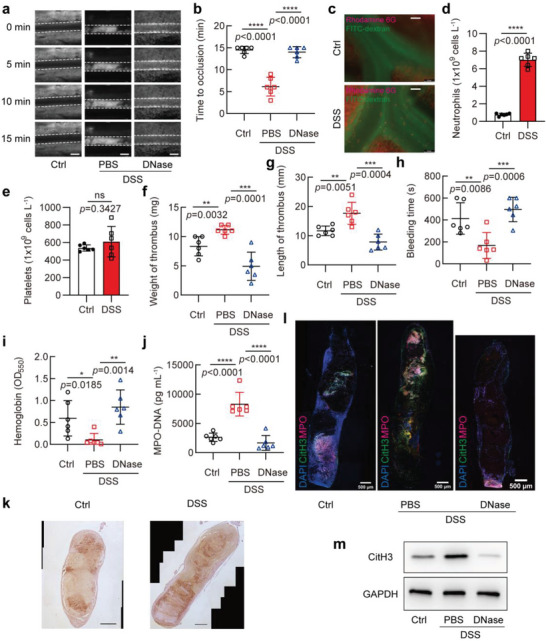
图1a:通过尾静脉给药或不给药DNase I (DNase)的对照组或3% DSS (PBS)处理小鼠血栓形成的代表性图像。
图1b:按(a)处理的三组小鼠血管闭塞时间。
图1c:肠系膜静脉的代表性图像,罗丹明6G标记的白细胞和血小板(红色)和FITC‐葡聚糖标记的血流(绿色)。
图1d-e:对照组和DSS组小鼠治疗7天后血浆中性粒细胞计数(d)和血小板计数(e)。通过EDTA抗凝全血用五类血细胞分析仪进行分析。
图1f-g:按(a)处理的小鼠下腔静脉狭窄手术治疗,测量3组采集的血栓重量和长度。
图1H:按(a)处理小鼠尾出血时间。
图1i:利用酶标仪测定红细胞破裂后释放的血红蛋白在550 nm波长处的吸光度,测定失血量。
图1j:采用MPO‐DNA ELISA法测定(a)处理的三组小鼠血浆NETs。
图1k:Ly6G代表性免疫组化染色图像。
图1l:按(a)处理的三组小鼠下腔静脉血栓瓜氨酸组蛋白H3(绿色)和MPO(洋红色)染色。
图1m:下腔静脉狭窄术后2天全血栓中CitH3表达的Western blot分析。
综上所述,得出结论,中性粒细胞以NETs依赖的方式促进血栓形成。
2.从DSS诱导的IBD小鼠血浆中分泌外泌体在IBD相关血栓形成中起重要作用
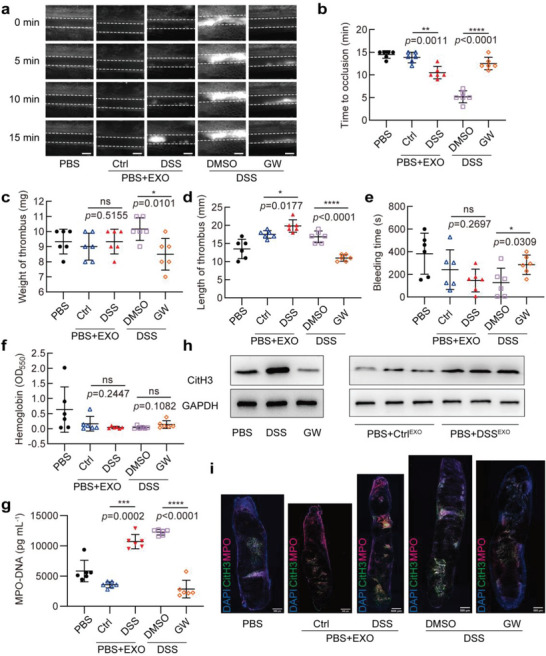
图2a:五组不同处理小鼠血栓形成的代表性图像
图2b:同(a)处理的5组小鼠血管闭塞时间。
图2c-d:按(a)处理的小鼠下腔静脉狭窄手术治疗,48 h后,测量5组小鼠的重量和血栓长度。
图2e:同(a)处理的5组小鼠尾出血时间。
图2f:用酶标仪测定5组小鼠在550 nm波长处的血红蛋白吸光度,测定失血量。图2g:采用MPO‐DNA ELISA法测定5组小鼠血浆中NETs的含量。
图2h: PBS处理小鼠通过尾静脉注射从Ctrl (CtrlEXO)或DSS处理(DSSEXO)小鼠中分离的外泌体,并在下腔静脉狭窄术后2天获得的整个血栓中进行CitH3表达的Western blot分析。
图2i:与(a)相同处理的5组小鼠下腔静脉血栓中CitH3(绿色)和MPO(洋红色)染色。
这些结果表明,使用GW4869抑制外泌体释放可以通过降低外周血和静脉血栓形成中的NETs水平来延缓DSS治疗小鼠的血栓形成。
3.发炎的IECs诱导中性粒细胞生成NETs
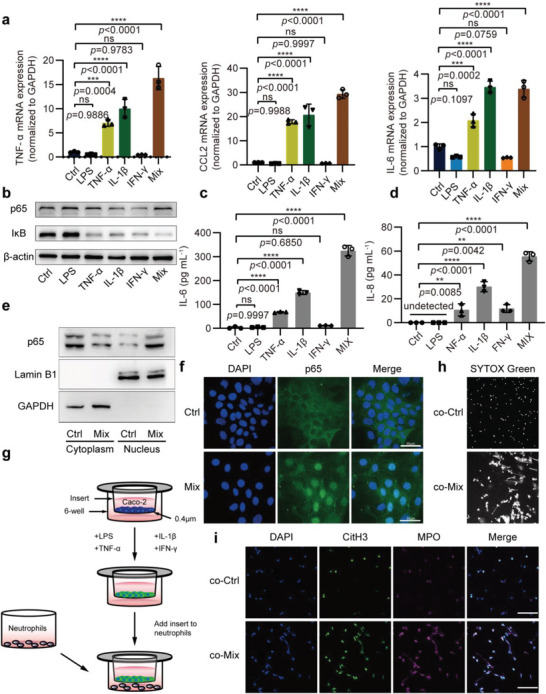
图3a:通过qPCR分析检测用PBS (Ctrl)、10µg mL−1 LPS (LPS)、50µg mL−1 TNF‐α (TNF‐α)、25µg mL−1 IL‐1β (IL‐1β)、50µg mL−1 IFN‐γ (IFN‐γ)或以上四种因素的混合物(Mix)处理的Caco-2细胞中TNF‐α、CCL2和IL‐6 mRNA的表达。
图3b):Western blot分析6组(a)处理的Caco‐2细胞中p65和 IκB的表达。
图3c-d: ELISA检测6组(a)处理的Caco‐2细胞培养上清中IL - 6和IL - 8的表达。
图3e):Western blot分析测定PBS (Ctrl)或Mix处理的Caco‐2细胞中NFκB p65的核和细胞质表达。
图3f):PBS (Ctrl)或Mix处理的Caco‐2细胞中的p65(绿色)染色,细胞核用DAPI(蓝色)染色。
图3g:Caco- 2细胞(上室)和中性粒细胞(下室)的Transwell共培养系统示意图。
图3h:与Ctrl或Mix处理的Caco-2细胞共培养后中性粒细胞胞外DNA SYTOX Green染色的代表性图像。
图3i:用Ctrl或Mix处理的Caco-2细胞与中性粒细胞共培养,细胞核用DAPI(蓝色)染色,其中CitH3(绿色)和MPO(洋红色)染色。
总的来说,这些数据表明炎症的IECs可以诱导中性粒细胞产生NETs。
4.发炎的IECs衍生外泌体促进中性粒细胞释放NETs
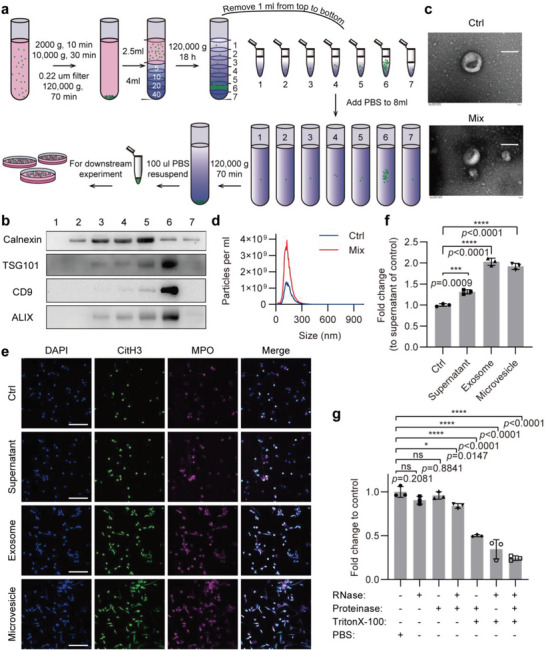
图4a:用Ctrl或Mix处理的Caco-2细胞培养上清制备外泌体示意图。
图4b:Western blot检测外泌体分离过程中ER相关蛋白calnexin和外泌体标记物TSG101、CD9和ALIX。
图4c:从Ctrl或Mix处理的Caco-2细胞分离的外泌体的电镜图像。
图4d:从Ctrl或Mix处理的Caco-2细胞分离的外泌体的纳米颗粒跟踪分析。
图4e:对Mix处理的Caco-2细胞上清液、外泌体或微泡处理的中性粒细胞进行CitH3(绿色)和MPO(洋红色)的免疫荧光染色。
图4f:通过测定SYTOX Green在523 nm处的OD来定量NETs的释放,倍增变化归一化到对照上清(Ctrl)。
图4g)将PBS‐、RNase‐、蛋白酶‐、RNase +蛋白酶‐、蛋白酶+ Triton X‐100‐、RNase + Triton X‐100‐、RNase +蛋白酶+ Triton X‐100‐或RNase +蛋白酶+ Triton X‐100‐处理过的外泌体添加到中性粒细胞中,然后通过测量Ex485、Em520处SYTOX Green的荧光检测NETs的定量。
总之,这些结果提供了明确的证据,证明炎症Caco-2细胞分泌的外泌体直接促进中性粒细胞以依赖外泌体RNA的方式释放NETs。
5.IEC外泌体诱导NETs形成分子LINC00668的鉴定
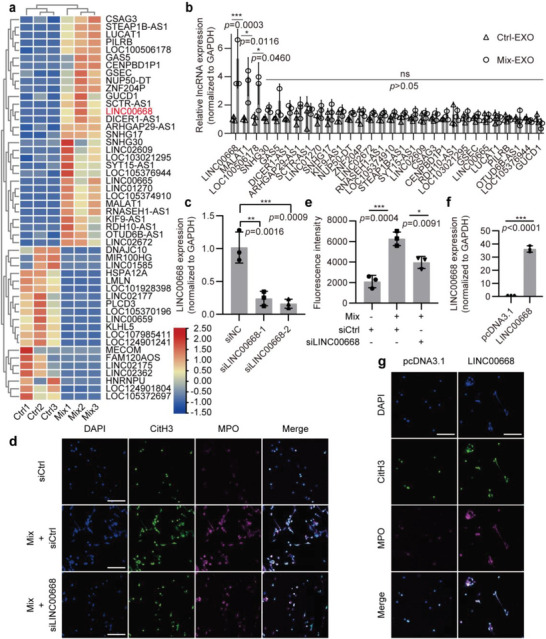
图5a:选择并总结经Ctrl或Mix处理的Caco-2细胞外泌体中差异表达的lncRNAs。热图显示显著变化的lncRNAs,用红色(上调)和蓝色(下调)表示。
图5b:qPCR验证显著上调的lncRNAs子集。将其相对表达量归一化为GAPDH。
图5c:利用两个靶向LINC00668不同区域的siRNAs在Caco‐2细胞中敲低LINC00668,通过qPCR检测敲低效率。
图5d:将转染siCtrl或siLINC00668的Caco-2细胞与中性粒细胞共培养4小时,对中性粒细胞进行CitH3(绿色)、MPO(品红)和DAPI(蓝色)的免疫荧光染色。
图5e:通过测量SYTOX Green在Ex485, Em520处的荧光,定量siCtrl或siLINC00668转染的中性粒细胞中的NETs。
图5f:设计构建LINC00668过表达质粒,并通过qPCR验证过表达效率。
图5g:将pcDNA3.1和LINC00668过表达质粒分别转染到中性粒细胞中,用免疫荧光法对中性粒细胞进行CitH3(绿色)、MPO(洋红色)和DAPI(蓝色)染色。
这些结果表明,在IBD患者中,LINC00668的表达和NETs含量的变化与IBD小鼠模型相似,说明LINC00668在IBD患者中发挥的作用与在IBD小鼠模型中相同。
6.LINC00668促进NE从细胞质颗粒转运到细胞核并诱导NETs释放
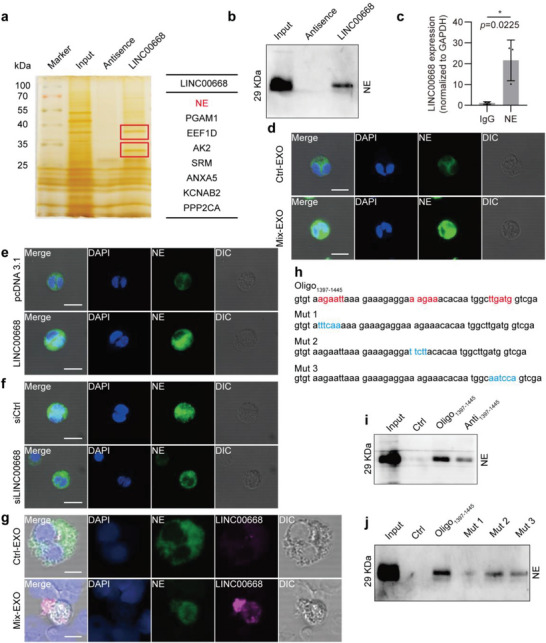
图6a:通过生物素化LINC00668拉降和质谱法鉴定HL - 60细胞中与LINC00668相互作用的蛋白。
图6b:用生物素化的LINC00668或其反义序列(antisence)拉低HL-60细胞中与LINC00668相关的蛋白,并使用抗NE抗体进行Western blotting分析沉淀。
图6c:在过表达LINC00668的HL-60细胞中,用IgG或抗NE抗体拉下RNA -蛋白免疫沉淀,用qRT-PCR检测LINC00668。
图6d:中性粒细胞与从Ctrl(Ctrl‐EXO)或Mix(Mix‐EXO)处理的Caco‐2细胞分离的外泌体孵育,免疫荧光染色检测NE的亚细胞定位。
图6e:用过表达pcDNA3.1或LINC00668的质粒转染中性粒细胞,免疫荧光染色检测NE的亚细胞定位。
图6f:用siCtrl或siLINC00668转染Caco‐2细胞,并用Mix刺激24小时。从培养上清中分离外泌体,用于处理中性粒细胞,并使用免疫荧光染色检测NE亚细胞定位。
图6g:用从Ctrl(Ctrl‐EXO)或Mix (Mix‐EXO) Caco‐2细胞分离的外泌体处理中性粒细胞,用NE和LINC00668荧光原位杂交(FISH)对中性粒细胞进行免疫荧光染色。
图6h: LINC00668序列(Oligo1397‐1445)中1397-1445个核苷酸位置的序列和Oligo1397‐1445序列中结合位点1、2和3的3个突变体(Mut 1、Mut 2和Mut 3)。
图6i:将HL‐60细胞裂解物与生物素化的Oligo1397‐1445、Oligo1397‐1445的反义序列(Anti1397‐1445)或Ctrl孵育,Western blot分析检测Oligo‐蛋白免疫沉淀中的NE水平。
图6j: 将HL‐60细胞裂解物与生物素化的Oligo1397‐1445或结合位点1、2和3 (Mut 1、Mut 2和Mut 3)的突变体一起孵育,Western blot分析检测Oligo‐蛋白免疫沉淀中的NE水平。
这些发现表明,Mix‐EXO中含有的LINC00668促进了中性粒细胞中NE的核易位。
7.小檗碱通过阻断LINC00668与NE的结合抑制NETs的形成
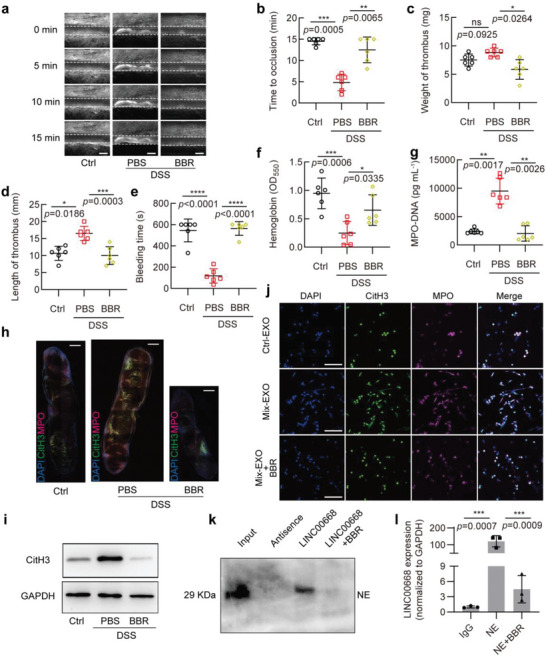
图7a:小鼠单独饮水(Ctrl)或3% DSS联合PBS (PBS)或BBR (BBR)腹腔注射后血栓形成的代表性图像。
图7b:按(a)处理的3组小鼠血管闭塞时间。
图7c-d:按(a)处理的小鼠下腔静脉狭窄手术,48 h后,测量3组小鼠的重量和血栓长度。
图7e:尾出血时间见(a)。
图7f:用酶标仪测定血红蛋白在550nm波长处的吸光度,测定失血量。
图7g:采用MPO‐DNA ELISA法测定(a)处理的3组小鼠血浆NETs。
图7h:同(a)处理的3组小鼠下腔静脉血栓形成的血栓中CitH3(绿色)和MPO(洋红色)染色。
图7i:下腔静脉狭窄术后2天全血栓中CitH3表达的Western blot分析。
图7j:中性粒细胞与从Ctrl (Ctrl‐EXO)或Mix处理(Mix‐EXO) Caco‐2细胞分离的外泌体孵育,然后用BBR处理或不处理。对中性粒细胞进行CitH3(绿色)、MPO(品红色)和DAPI(蓝色)的免疫荧光染色。
图7k:用生物素化的LINC00668(含或不含BBR或其反义序列)拉低HL‐60细胞裂解物,并使用抗NE抗体进行Western blotting分析沉淀。
图7l:在过表达LINC00668的HL-60细胞中,用IgG或抗NE抗体拉下的RNA -蛋白免疫沉淀物中检测LINC00668的qRT - PCR。结果与IgG免疫沉淀物相关。
这些结果表明BBR可以有效抑制NETs的释放和随后的血栓形成。
结论
本研究的新发现包括:1)DSS诱导的IBD小鼠的NETs形成显著增加;2)炎症条件下IECs释放的外泌体通过促进中性粒细胞释放NETs促进血栓形成;3)在IECs来源的外泌体中高度富集的LINC00668介导NE从细胞质颗粒向细胞核的易位,从而刺激组蛋白裂解和染色质去浓缩,导致NETs释放;4) BBR通过抑制LINC00668与NE的相互作用,抑制NE的核易位和随后的NETs形成,从而发挥其抗血栓作用。这些观察结果为外泌体介导的NETs形成将IBD和血栓形成联系起来提供了机制解释。






