研载生物科技(上海)有限公司
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
植物外泌体(PDEs)真能「碾压」传统草药提取物?这篇综述从提取到临床全覆盖,拿捏草药创新核心!
15942 人阅读发布时间:2025-09-18 11:29
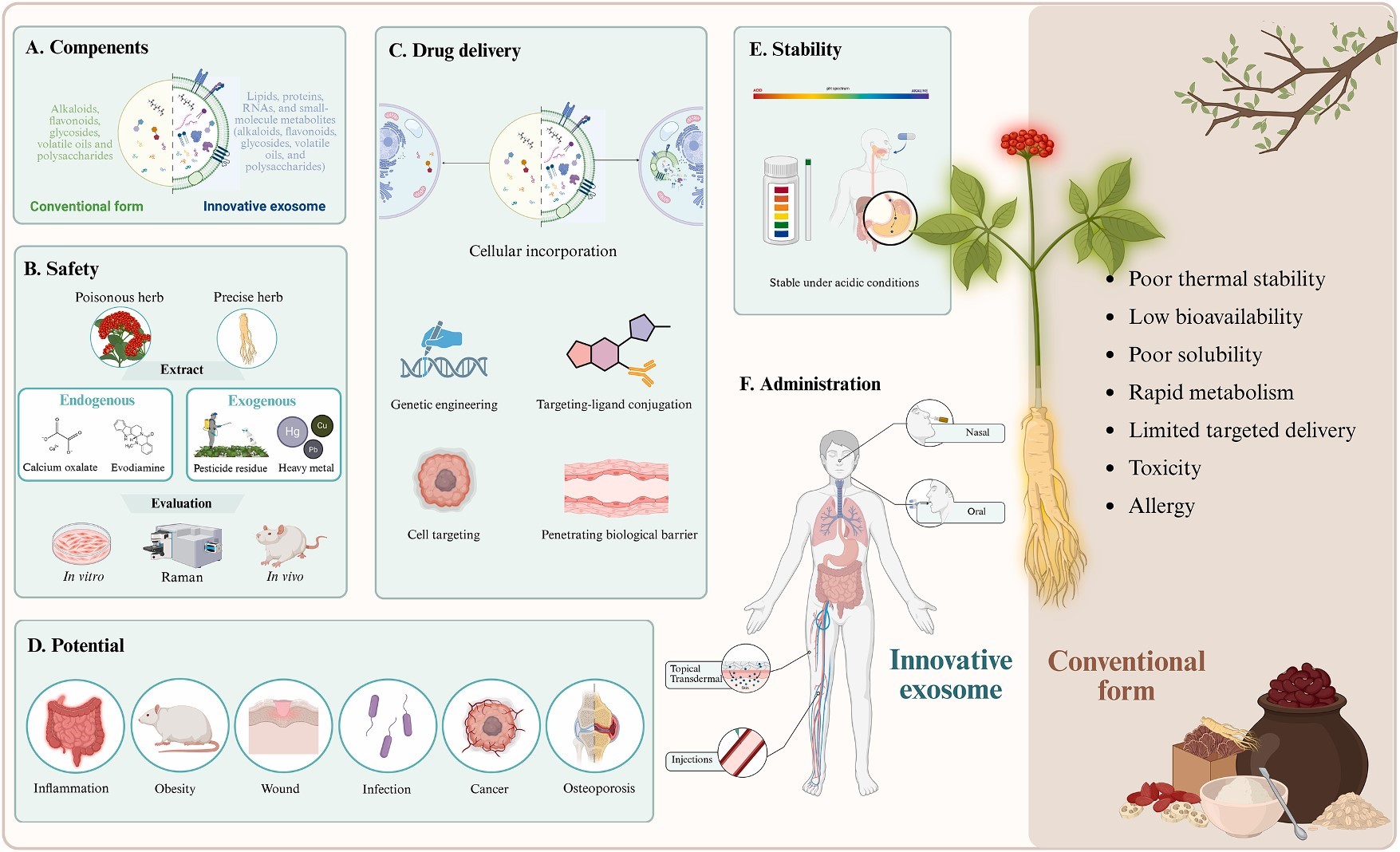
传统草药因“多组分协同治疗”特性在医学史上具有重要地位,但受限于原料粗糙、成分复杂、生物利用度低及有效物质与作用靶点不明确等问题,临床转化面临显著瓶颈。植物来源外泌体(Plant-derived exosomes, PDEs)作为草药的创新存在形式,凭借独特的磷脂双分子层结构(可包裹蛋白质、脂质、RNA 及代谢物等生物活性分子),为突破传统提取物局限性提供了新路径。

今天分享的是发表在【Phytomedicine】(IF:8.3)上题为“Plant-derived exosomes: Unveiling the similarities and disparities between conventional extract and innovative form”的研究,本研究通过系统综述 PubMed、Web of Science 等数据库中植物外泌体相关研究,聚焦人参、姜、葛根、姜黄、枸杞等高频药用植物,深入解析 PDEs 的成分组成、生物利用度、药物递送能力及稳定性,明确其与传统草药提取物的异同,旨在为PDEs 在慢性疾病管理中的转化应用奠定理论基础。
一、PDEs 的核心优势:与其他载体的差异化对比
PDEs 在纳米医学应用中展现出优于哺乳动物来源外泌体(MDEs)及合成纳米颗粒的独特优势。从成分来看,PDEs 包含蛋白质(如肌动蛋白、四跨膜蛋白)、脂质(如双半乳糖基二酰基甘油 DGDG)及 RNA(富含 miRNA),且具有植物特异性表面标志物(如四跨膜蛋白、凝集素);MDEs 以 ALIX、CD9 等细胞特异性标志物为特征,合成纳米颗粒则依赖人工聚合物或脂质。在安全性与可持续性上,PDEs 因缺乏哺乳动物抗原而免疫原性低,无 zoonotic 病原体传播风险,且来源广泛、生产成本低、环境友好,克服了 MDEs 产量有限、易携带病原体及合成纳米颗粒修饰复杂、毒性风险高的缺陷。
PDEs 的药理活性覆盖多个疾病领域,包括癌症、肺泡纤维化、病毒感染、伤口愈合、脱发及炎症性疾病等,其核心机制在于通过靶向递送生物活性物资调控细胞功能。
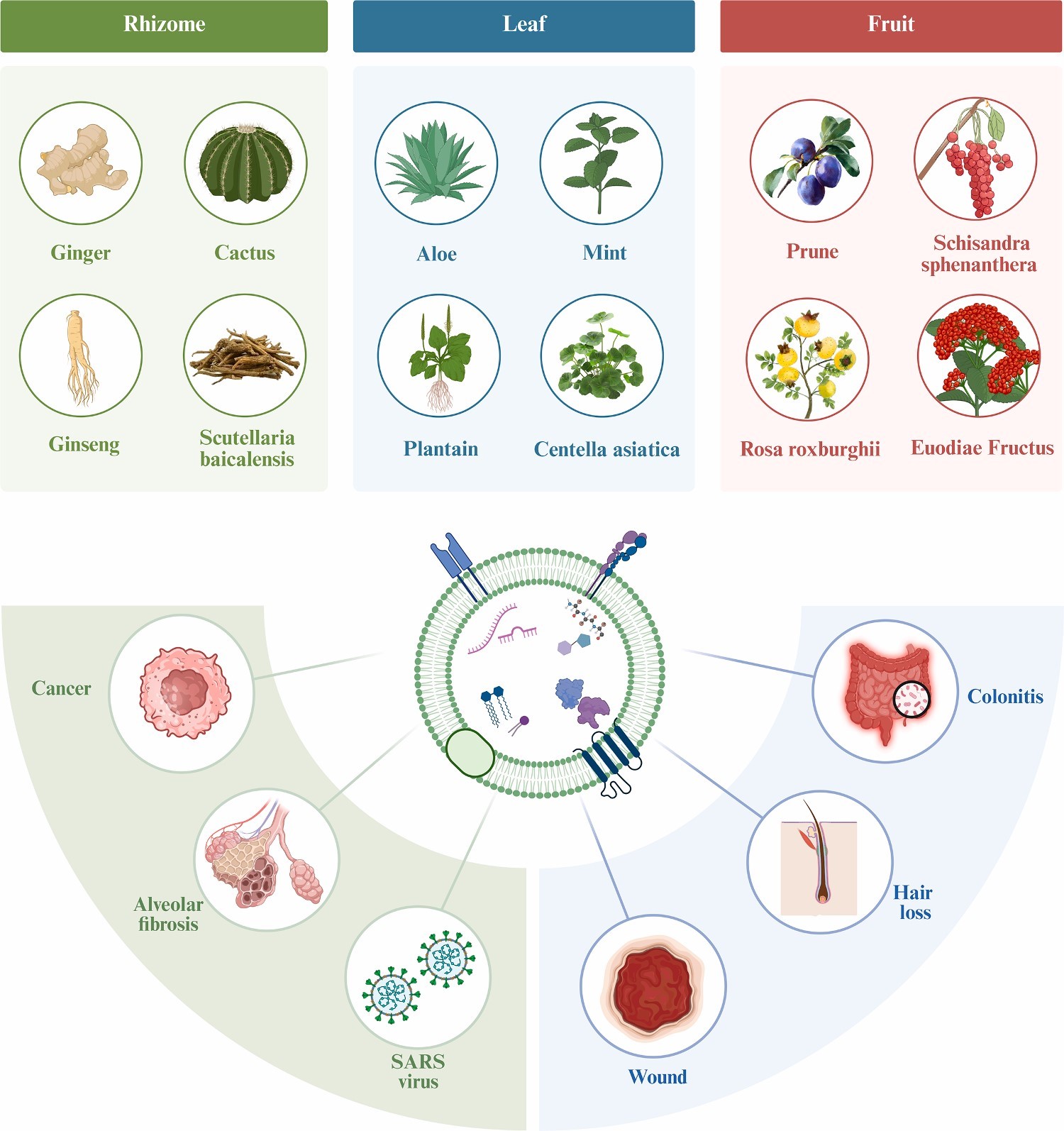
二、PDEs 的提取技术
1. 研究归纳了PDEs的6类核心提取技术,各类方法在纯度、效率及适用性上存在显著差异。
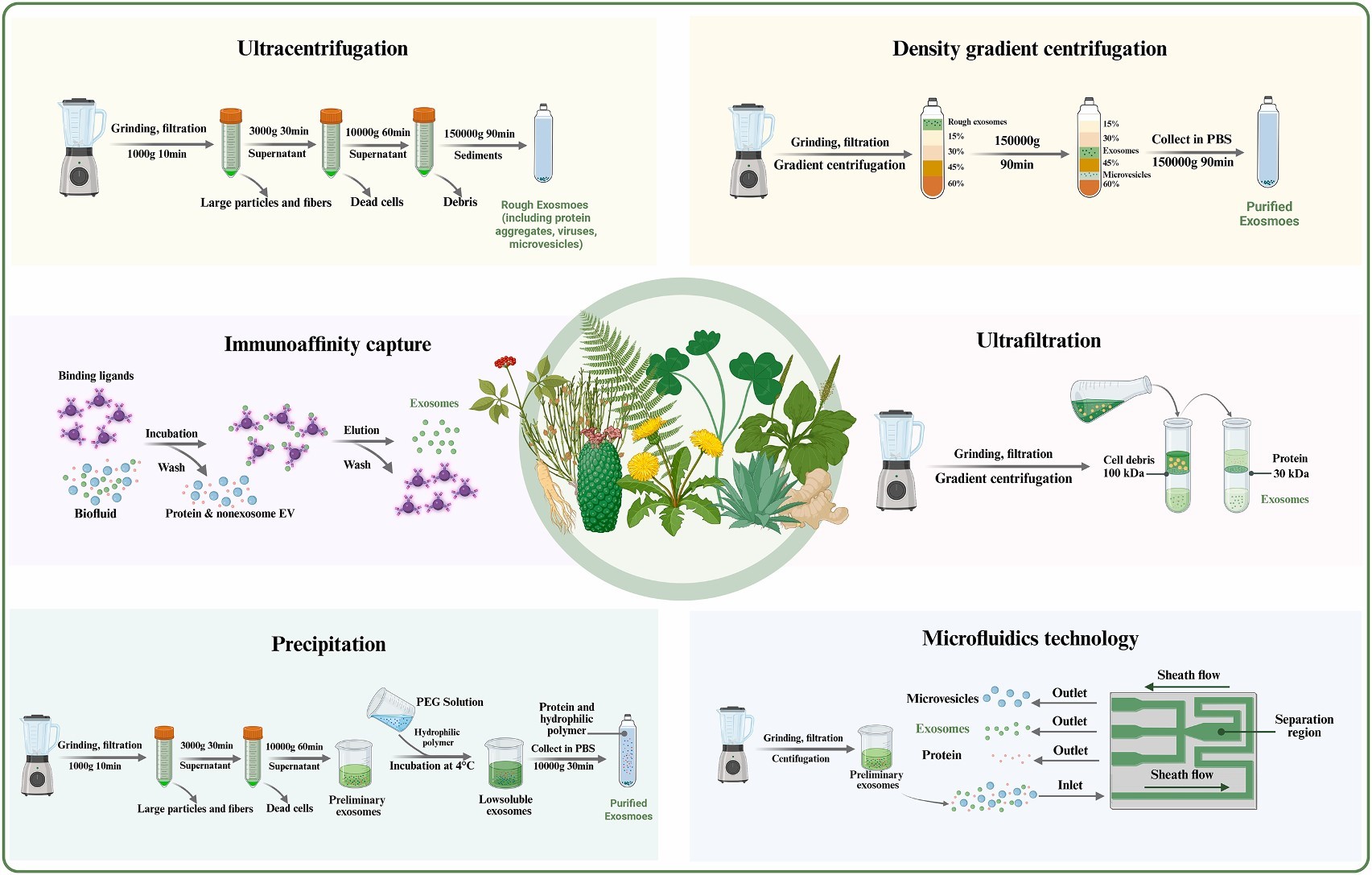
1.1差速超速离心:通过逐步提升离心力(如 1000×g→5000×g→10000×g→150000×g)分离不同大小颗粒,操作简便但纯度较低,常需结合密度梯度离心进一步纯化;
1.2密度梯度离心:基于浮力密度差异(如蔗糖)让 PDEs 在特定密度区域形成条带,实现高纯度分离,但介质残留可能影响后续分析;
1.3免疫亲和捕获:利用 PDEs 表面标志物(如四跨膜蛋白)与固定抗体的特异性结合,分离特定亚群 PDEs,纯度高但抗体成本高,限制规模化应用;
1.4超滤法:通过半透膜按分子量截留 PDEs,快速且可浓缩样本,效率与超速离心相当,但膜吸附易导致回收率下降;
1.5沉淀法:以聚乙二醇(PEG)改变 PDEs 溶解度,诱导其聚集沉淀,成本低、操作简单,但沉淀剂可能破坏 PDEs 结构完整性;
1.6微流控技术:依托芯片微结构按颗粒大小、电荷或表面标志物分离,无需超速离心,分离效率高,但设备门槛高、成本昂贵。
三、PDEs 的生物发生与组成特征
1. 生物发生机制
PDEs 的形成路径与 MDEs 类似,核心过程为:植物细胞膜内陷形成早期内体→内体通过膜内陷生成腔内囊泡,逐步成熟为多泡体(MVBs)→MVBs 与细胞膜融合,释放腔内囊泡即 PDEs。
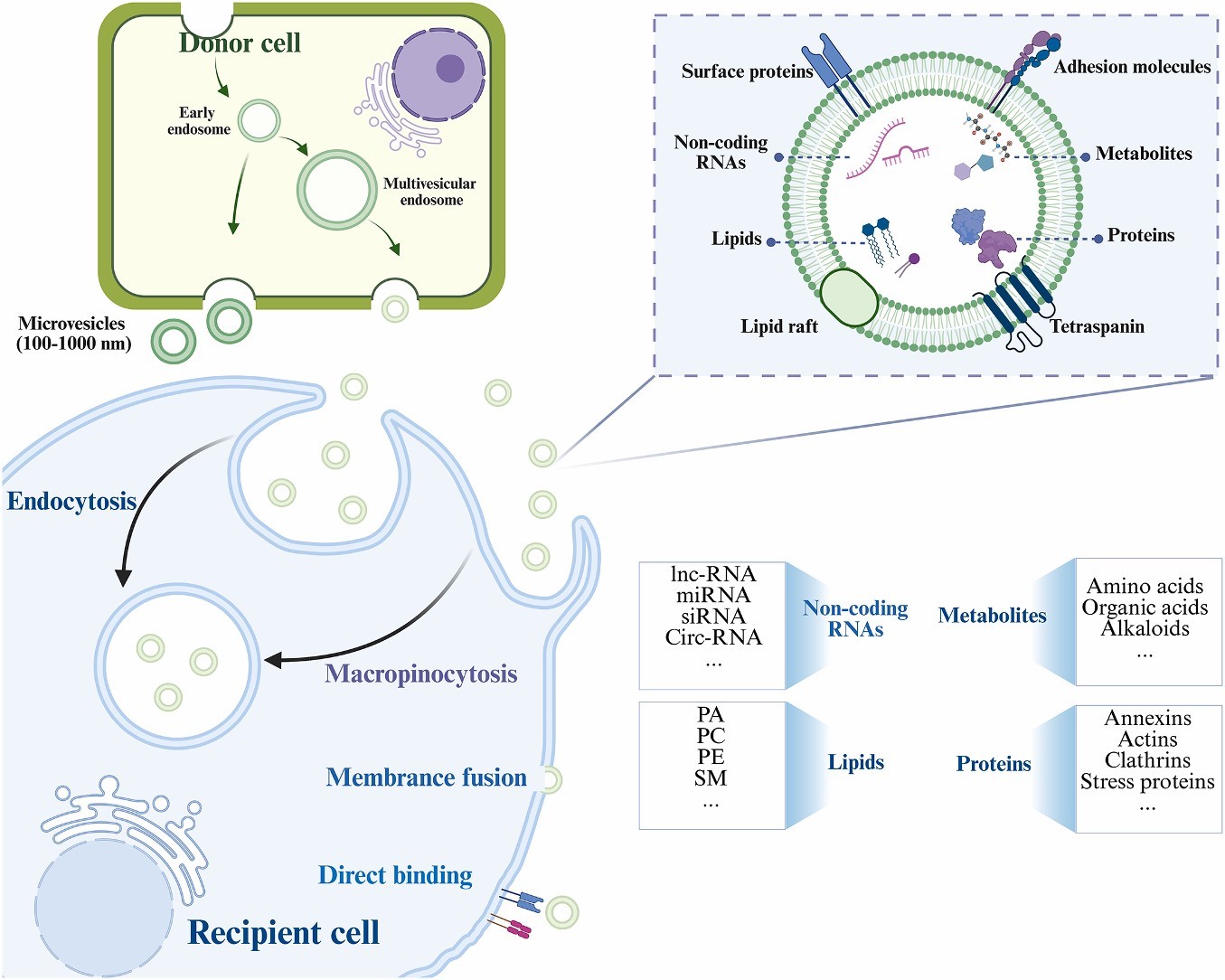
植物特有的代谢环境会使 PDEs 富集物种特异性成分,如人参 PDEs 富含人参皂苷,姜 PDEs 含有姜辣素,为其靶向治疗功能提供物质基础。
2. 核心组成及功能
PDEs 的组成具有 “多组分协同” 特征,不同成分赋予其独特生物学功能:
2.1 RNA:以 miRNA 为主,具有跨物种调控能力。例如苦瓜来源外泌体(Bit-DEs)的 miRNA 可抑制口腔鳞癌细胞(OSCC)中 NLRP3 炎症小体激活并诱导凋亡;姜来源外泌体(Ggr-DEs)的 miRNA 通过靶向乳酸菌 ycnE 基因,提升吲哚 - 3 - 甲醛水平与 IL-22 产量,助力结肠炎治疗;
2.2 蛋白质:涵盖跨膜蛋白(如水通道蛋白、四跨膜蛋白)、代谢酶(如 α- 淀粉酶)及 MVBs 相关蛋白(如 DnaJ 同源蛋白),其中水通道蛋白可维持膜稳定性,四跨膜蛋白参与细胞识别与摄取;
2.3 脂质:以甘油磷脂、糖脂及鞘脂为主,不仅是膜结构核心,还能增强 PDEs 的屏障穿透能力,如富含 MGDG/PC 的人参 PDEs 可耐受胃酸环境;
2.4 代谢物:包含黄酮类、皂苷、多糖等活性物质,且稳定性远优于游离形式。例如燕麦来源外泌体(Oat-DEs)的 β- 葡聚糖可被小胶质细胞剂量依赖性摄取;草莓来源外泌体的花青素可降低间充质干细胞(MSCs)氧化应激,且不影响细胞活性。
四、PDEs 的生物学功能与药物递送潜力
1. 跨物种细胞通讯功能
PDEs 可通过受体结合、膜融合或内吞作用被哺乳动物细胞摄取,实现跨 kingdom 调控:
1.1免疫调节:长春花来源外泌体(Cat-DEs)可激活巨噬细胞 NF-κB/PU.1 通路,增强吞噬能力与免疫细胞分化;拟南芥来源外泌体可向真菌病原体(如灰葡萄孢)递送 sRNA,沉默 BC1G_10728、BC1G_08464 等毒力基因,抑制感染;
1.2细胞增殖与分化调控:人参来源外泌体(Gin-DEs)的人参皂苷可促进皮肤 HaCaT 细胞、血管内皮 HUVEC 细胞增殖,加速细胞周期进程;其携带的 miRNA 可激活骨髓间充质干细胞(BMSCs)的 PI3K/Ras-ERK 通路,促进神经分化与神经再生;
1.3物种特异性差异:PDEs 的作用存在物种依赖,如 Ggr-DEs 的 osa-miR164d 在人巨噬细胞中沉默 TAB1 基因,在小鼠中则主要靶向 TNF 通路其他介质;叶酸修饰的 Ggr-DEs 对人结肠癌细胞(Colon-26)的摄取量是小鼠成纤维细胞的 2.8 倍,源于叶酸受体的物种表达差异。
2. 药物递送优势
PDEs 的磷脂双分子层结构使其成为理想药物载体,具备三大核心优势。
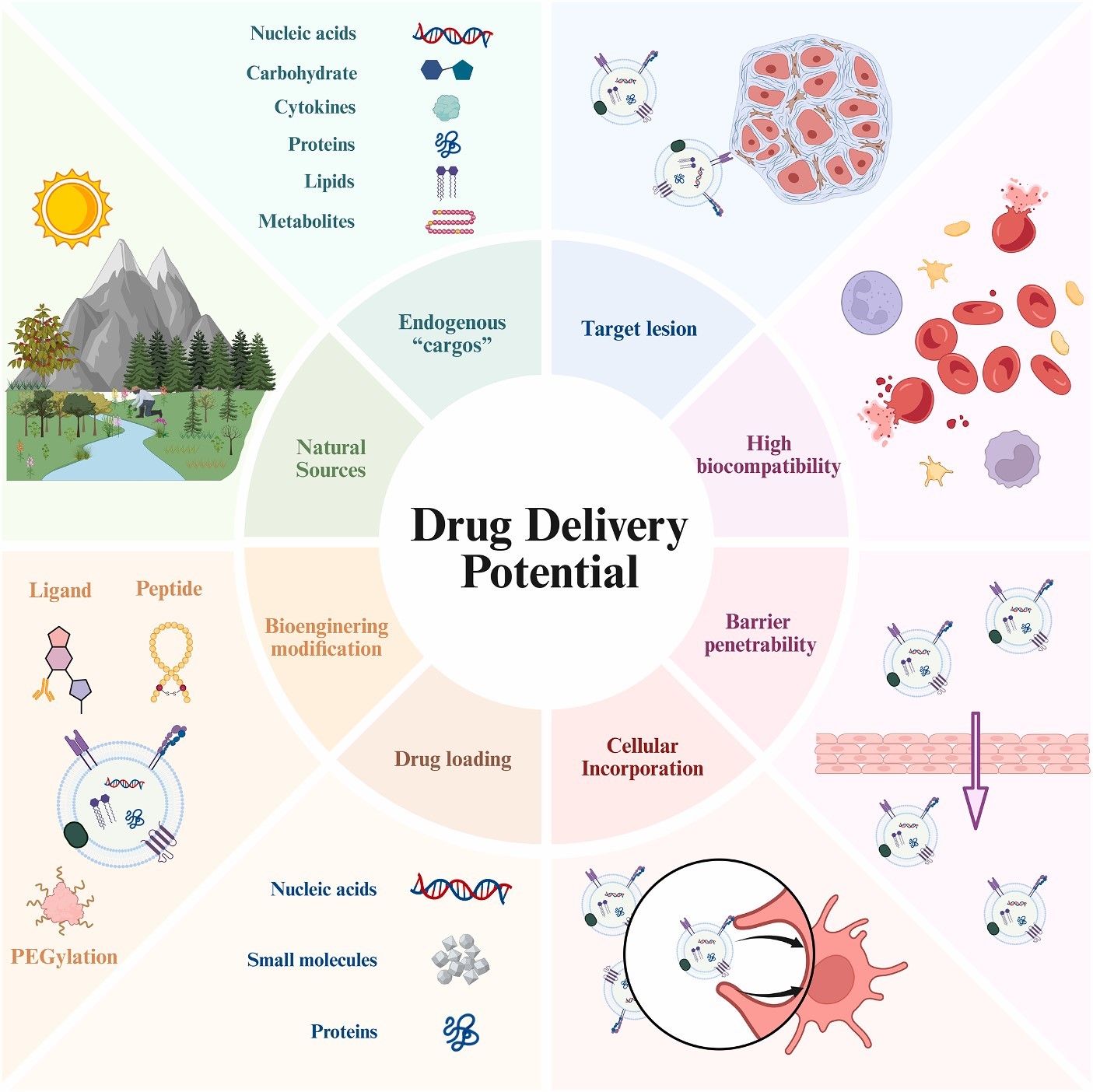
2.1高稳定性:可保护 cargo 免受酶解与 pH 波动影响,如金虎尾 PDEs 可保护 miRNA 耐受极端 pH 与 RNase;Gin-DEs 在 4℃下可稳定 25 天,在 pH 2 环境(模拟胃液)中 4 小时结构不变;
2.2强屏障穿透能力:纳米尺寸(30-150 nm)使其可穿透肠道黏液屏障、血脑屏障(BBB),如葡萄来源外泌体(Gra-DEs)可穿透肠道黏液到达干细胞;Gin-DEs 跨 BBB 效率是传统脂质体的 2.26 倍,1 小时内即可到达脑肿瘤部位,且在 3D 肿瘤球中的穿透深度显著优于对照组;
2.3可工程化改造:通过电穿孔、超声等技术加载外源药物,或修饰表面配体增强靶向性。例如将 dsRNA 载入柑橘 PDEs,可抑制霉菌毒素活性;肝素 - cRGD 修饰柠檬 PDEs,可靶向卵巢癌细胞的神经细胞黏附分子(NCAM),逆转 P - 糖蛋白介导的多药耐药。
五、PDEs 与传统草药提取物的差异化对比:以高频药用植物为例
研究选取人参、姜、葛根、姜黄、枸杞 5 类高频药用植物,从成分、药理效应、药物递送等维度,系统对比 PDEs 与传统提取物的差异:
1. 人参:Gin-DEs vs 传统提取物
Gin-DEs 通过差速离心与蔗糖梯度离心提取,含 miRNA、脂质、氨基酸及人参皂苷,保留完整活性成分,在抗结肠炎(调节肠道菌群、抑制促炎因子 TNF-α/IL-6)、抗胶质瘤(诱导凋亡、调控巨噬细胞极化)及促伤口愈合(激活 ERK/AKT/mTOR 通路)中展现优势,且可跨 BBB,加载顺铂后对 U-87MG 胶质瘤细胞毒性是游离药物的 12.66 倍;传统提取物多采用水提、醇沉或煎煮,以人参皂苷(Rb1、Rc、Rd、Re、Rg1)、多糖为主,高温与有机溶剂导致肽、RNA 降解,侧重心血管保护、神经保护(如抗阿尔茨海默病),需依赖脂质体 / PLGA 纳米颗粒包裹(如 Rg3 脂质体),靶向性差。
2. 姜:Ggr-DEs vs 传统提取物
Ggr-DEs 含高比例脂质(PA 约 40%、DGDG 约 30-40%)、136 种 miRNA(如 osa-miR164d)及姜辣素(6 - 姜辣素、8 - 姜辣素、10 - 姜辣素),其中姜辣素含量显著高于传统提取物,且 osa-miR164d 可沉默 TNF 通路 TAB1 基因,协同增强抗炎效果;药物递送中,阿霉素加载 Ggr-DEs(DOX@Ggr-DEs)对结肠癌的靶向效率达 95.9%,肿瘤细胞凋亡率(64.8%)是游离 DOX(23.3%)的 2.8 倍,且无明显心脏毒性;传统提取物以姜辣素(6 - 姜辣素为主)、挥发油、矿物质为主,通过抑制 MAPK 通路发挥抗炎、镇痛作用,靶向性差、易降解。
3. 葛根:Pue-DEs vs 传统提取物
Pue-DEs 通过差速离心与膜过滤提取,含 633 种蛋白质、92 种 miRNA、脂质(SM、TG、Cer)及葛根素、大豆苷等代谢物,可激活 PINK1-Parkin 介导的线粒体自噬,改善帕金森病病理,经鼻给药可跨 BBB 实现脑靶向递送;传统提取物以异黄酮(葛根素、大豆苷、大豆苷元)、三萜类为主,通过上调 SIRT1、抑制 NF-κB 通路发挥抗氧化、抗炎症作用,口服生物利用度低,需依赖注射给药。
4. 姜黄:Tur-DEs vs 传统提取物
Tur-DEs 含脂质(PE、TG、PI、DGDG)、CURS1/CURS2/CURS3 蛋白及姜黄素,加载黄芪成分(AC@Tur-DEs)后,阿魏酸的血药浓度(Cmax)提升 1.75 倍,体内暴露量(AUC0-t)提升 11.2 倍,且可通过抑制 NF-κB 通路治疗溃疡性结肠炎;传统提取物以姜黄素、挥发油、多糖为主,姜黄素水溶性差、易代谢,口服生物利用度低,需依赖纳米颗粒包裹(如 CUR@PLGA)。
5. 枸杞:Wol-DEs vs 传统提取物
Wol-DEs 含烯醇化酶、MGDG/PC 脂质、miRNA(aly-miR166a-3p)及枸杞多糖,可激活 AMPK/SIRT1/PGC1α 通路缓解肌肉萎缩,与 3D 打印 GelMA 水凝胶结合可促进脊髓损伤修复;传统提取物以多糖、氨基酸(牛磺酸)、维生素为主,通过调节肠道菌群发挥保肝、抗氧化作用,活性成分易降解。
六、结论
PDEs 作为传统草药与现代纳米医学融合的创新载体,在成分保留、生物相容性、靶向递送等方面展现出传统提取物无法比拟的优势,为慢性炎症、肿瘤、神经退行性疾病等领域的精准治疗提供了新策略。尽管当前面临标准化、稳定性及临床证据不足等挑战,但随着提取技术优化、机制研究深入及临床数据积累,PDEs 有望成为草药现代化与精准医疗领域的核心载体,推动传统植物疗法的革新与发展。






