研载生物科技(上海)有限公司
8 年
手机商铺
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
公司新闻/正文
外泌体科研方法论:外泌体分离、细胞摄取到动物实验的研究全流程!
150 人阅读发布时间:2025-11-07 15:07
类风湿性关节炎(RA)是一种慢性炎症性系统性自身免疫性疾病,常引起全身性多系统损伤。通过血液进行药物递送往往会导致目标病理部位的药物积累不足,通常需要频繁给药大剂量甚至联合给药才能达到预期的治疗效果,而这种大剂量治疗方案可引起严重的全身副作用,包括胃肠道紊乱、肝肾功能损害以及感染易感性增加。因此,迫切需要能够有效针对病变的疗法。

今天分享的是一篇发表在【Cell Commun Signal】(IF:8.9)上题为“Platelet-derived exosomes in situ reprogramming macrophages for rheumatoid arthritis treatment”的研究,该研究提出了一种新的类风湿性关节炎(RA)治疗策略,即使用血小板来源的外泌体(PLT-Exos)诱导M1巨噬细胞极化为抗炎M2表型。研究结果证实,PLT-Exos可通过静脉注射特异性富集于RA炎症关节部位,高效被M1型巨噬细胞摄取。PLT-Exos富含CD163等免疫调节蛋白,能在体外和体内诱导M1巨噬细胞向M2巨噬细胞极化,下调促炎因子分泌、上调抗炎因子表达,从而减轻关节滑膜炎症、抑制骨侵蚀和软骨损伤,改善CIA小鼠的运动功能;其治疗效果与临床药物MTX相当,但具有更优的生物相容性和更低的毒性,且能调节Th/Treg细胞平衡,参与免疫调控。因此,PLT-Exos为RA及其他炎症相关疾病提供了一种安全有效的新型治疗策略。
研究成果
1. PLT-Exos的表征
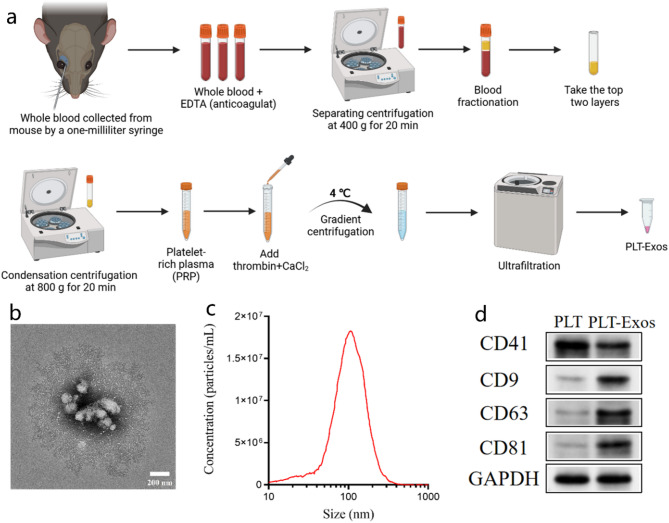
图1 PLT-Exos的提取与表征。
图1A:PLT-Exos的提取流程。
图1B:PLT-Exos的透射电子显微镜(TEM)图像。结果显示PLT-Exos为球形囊泡,直径约100 nm,符合外泌体典型形态。
图1C:纳米颗粒追踪分析(NTA)结果。结果显示PLT-Exos的粒径分布集中,与TEM观察到的直径范围一致,证实其尺寸均一性。
图1D:Western blot(WB)检测结果。结果显示PLT-Exos与血小板均表达血小板标志物CD41,且PLT-Exos阳性表达外泌体特征标志物CD9、CD63和CD81,验证了所提取囊泡的身份。
这些结果表明,通过梯度离心联合超滤法成功分离出高纯度的PLT-Exos,其形态、粒径和标志物表达均符合外泌体的核心特征。
2.体外细胞摄取PLT-Exos
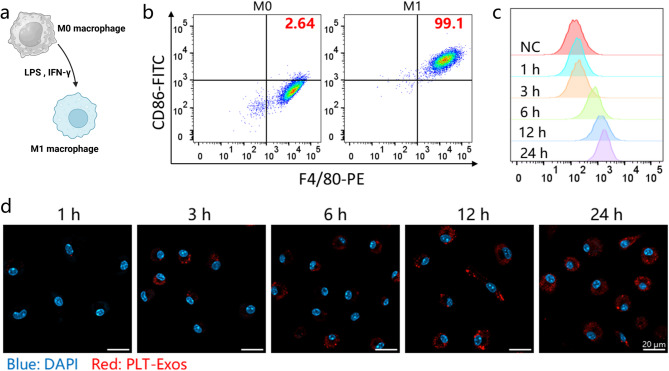
图2 M1巨噬细胞极化建立及PLT-Exos的体外摄取。
图2A:M0巨噬细胞向M1极化的示意图。
图2B:流式细胞术检测结果。结果显示经LPS和IFN-γ刺激后,99.1%的细胞表达M1巨噬细胞标志物CD86,证实M1巨噬细胞极化成功。
图2C:流式细胞术分析DiD标记的PLT-Exos被M1巨噬细胞摄取的效率。结果显示与PLT-Exos共孵育后,细胞内荧光强度随时间逐渐升高。
图2D:激光共聚焦显微镜图像。结果显示3小时时M1巨噬细胞内已出现明显红色荧光,12小时荧光强度达到峰值,与流式细胞术结果一致,证实M1巨噬细胞可高效摄取PLT-Exos。
这些结果表明,LPS和IFN-γ可成功诱导M0巨噬细胞极化为M1表型,且M1巨噬细胞能够时间依赖性地高效摄取PLT-Exos,为PLT-Exos调控巨噬细胞表型提供了前提条件。
3. PLT-Exos在体外诱导M1重编程为M2巨噬细胞
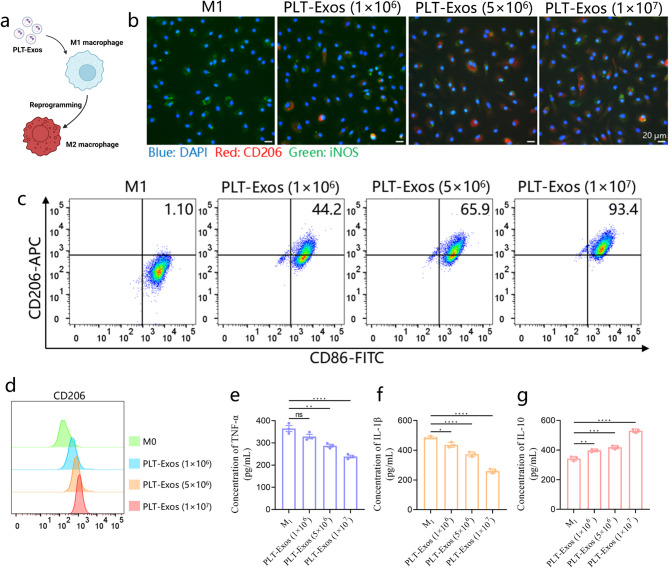
图3 PLT-Exos体外诱导M1巨噬细胞向M2表型重编程。
图3A:PLT-Exos诱导M1向M2巨噬细胞极化的示意图。
图3B:免疫荧光染色结果。结果显示随着PLT-Exos浓度升高,iNOS荧光信号逐渐减弱,CD206荧光信号逐渐增强,呈现浓度依赖性。
图3C:流式细胞术检测结果。结果显示M1巨噬细胞经不同浓度PLT-Exos处理后,M2标志物CD206的表达率随浓度升高而显著增加,进一步证实表型转化效果。
图3D:流式细胞术检测结果。结果显示M0巨噬细胞经PLT-Exos处理后,CD206表达率同样浓度依赖性升高,提示PLT-Exos对巨噬细胞表型具有正向调控作用。
图3E-G:ELISA检测结果。结果显示与未处理的M1巨噬细胞相比,PLT-Exos处理组的促炎因子TNF-α、IL-1β水平显著降低,抗炎因子IL-10水平显著升高,且呈浓度依赖性。
这些结果表明,PLT-Exos可在体外浓度依赖性地诱导M1巨噬细胞向M2表型极化,同时下调促炎因子分泌、上调抗炎因子表达,具备显著的抗炎调控能力。
4. PLT-Exos在CIA小鼠中的治疗效果
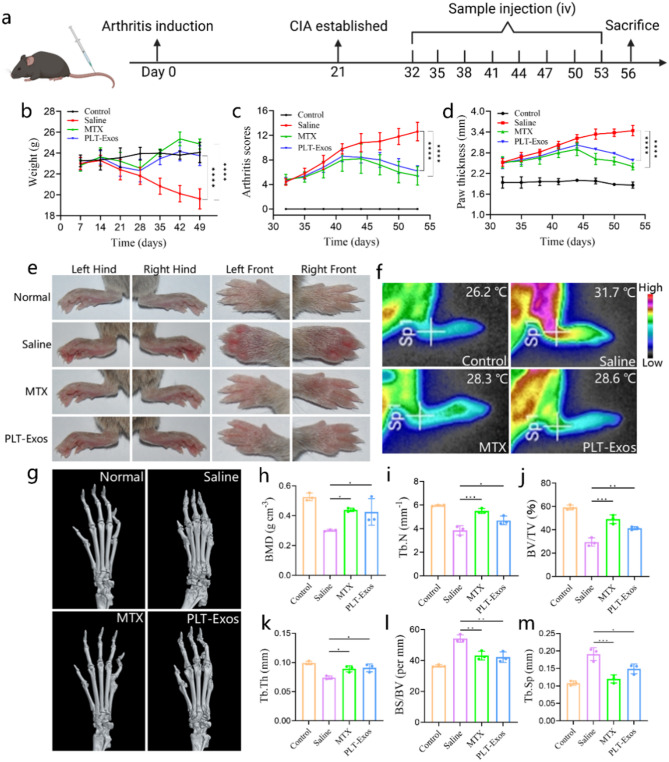
图4 PLT-Exos在CIA小鼠中的治疗效果。
图4A:RA模型建立及治疗方案示意图。
图4B:体重变化曲线。结果显示生理盐水组小鼠体重持续下降,而PLT-Exos组和MTX组体重逐渐升高,接近正常对照组水平。
图4C:关节炎评分曲线。结果显示生理盐水组评分持续升高,PLT-Exos组和MTX组评分显著降低,且两组疗效相当。
图4D:关节厚度变化曲线。结果显示生理盐水组关节厚度逐渐增加,PLT-Exos组和MTX组显著减轻,且维持在较低水平。
图4E:小鼠四肢外观图。图像显示生理盐水组四肢关节出现明显红斑和严重肿胀,PLT-Exos组和MTX组红斑、肿胀显著缓解。
图4F:红外热成像图。图像显示生理盐水组右后爪温度(31.7℃)显著高于正常组(26.2℃),PLT-Exos组(28.6℃)和MTX组(28.3℃)温度显著降低。
图4G:Micro-CT图像。图像显示生理盐水组小鼠后爪骨表面粗糙、骨侵蚀严重;PLT-Exos组和MTX组关节结构完整,骨表面相对光滑。
图4H-M:Micro-CT定量分析结果。结果显示生理盐水组骨矿物质密度(BMD)、骨小梁数量(Tb.N)、骨体积分数(BV/TV)、骨小梁厚度(Tb.Th)显著降低,骨表面积/体积比(BS/BV)、骨小梁间距(Tb.Sp)显著升高;PLT-Exos组和MTX组上述骨形态参数均接近正常水平。
这些结果表明,PLT-Exos对CIA小鼠的治疗效果与临床药物MTX相当,可显著减轻关节炎症(降低关节炎评分、关节厚度和局部温度)、保护骨和软骨结构、改善小鼠全身状态(增加体重),具备良好的体内治疗潜力。
5. PLT-Exos在CIA小鼠中的生物分布
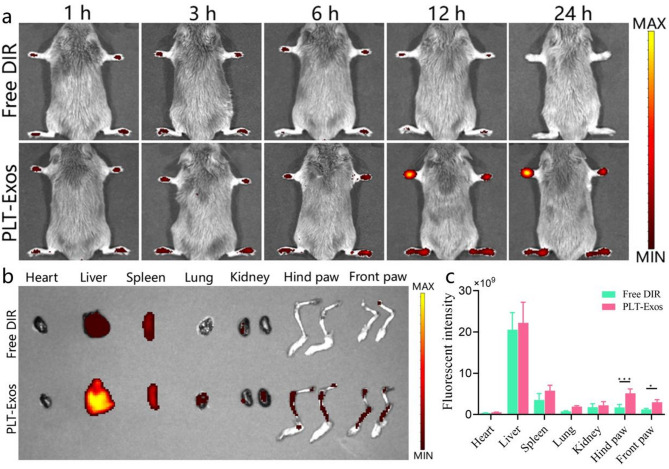
图5 PLT-Exos在CIA小鼠体内的生物分布。
图5A:体内荧光成像结果。结果显示PLT-Exos组关节荧光信号强且持续时间长,24小时仍可清晰检测到,尤其在病变严重的爪部富集明显。
图5B:24小时后主要器官及四肢的荧光分布图像。图像显示PLT-Exos组后爪和前爪荧光强度显著高于心脏、肺、肾脏,仅肝脏和脾脏(免疫代谢器官)荧光强度较高。
图5C:荧光定量分析结果。结果显示PLT-Exos组关节部位荧光强度显著高于游离DiR组,证实PLT-Exos可特异性富集于炎症关节。
这些结果表明,PLT-Exos具有良好的体内炎症部位靶向性,可在CIA小鼠炎症关节持续富集,为其局部调控巨噬细胞表型、发挥治疗作用提供了靶向基础。
6.组织学研究
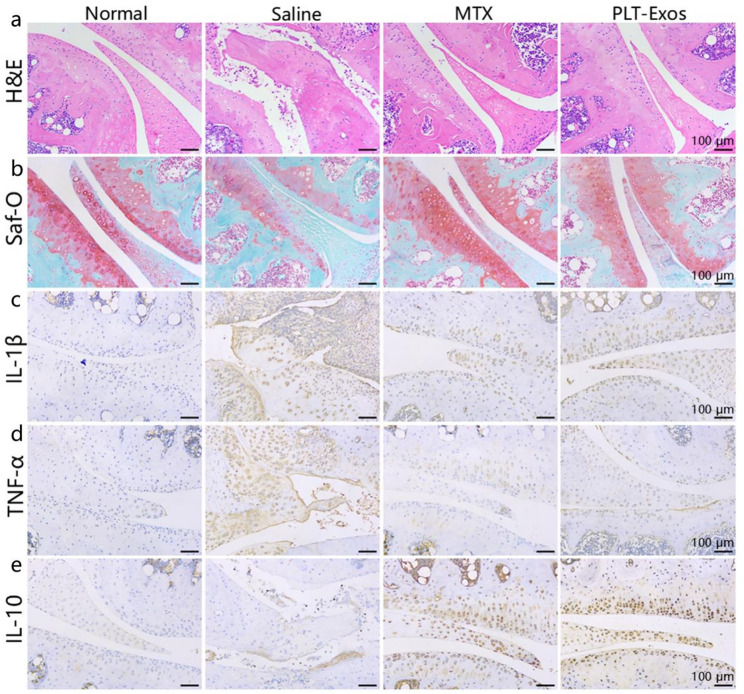
图6关节组织的组织学分析。
图6A:HE染色结果。结果显示正常组关节结构完整,无炎症浸润;生理盐水组关节滑膜增生严重、炎症细胞大量浸润、骨破坏明显;PLT-Exos组和MTX组滑膜增生减轻、炎症细胞浸润减少、骨破坏显著缓解。
图6B:番红O-固绿染色结果。结果显示生理盐水组关节软骨表面红色染色减弱,提示软骨大量丢失;PLT-Exos组和MTX组软骨表面红色染色明显,表明软骨得到有效保护。
图6C-E:免疫组织化学检测结果。结果显示生理盐水组关节组织中促炎因子IL-1β、TNF-α表达显著升高,抗炎因子IL-10表达显著降低;PLT-Exos组和MTX组IL-1β、TNF-α表达降低,IL-10表达升高,与正常组接近。
这些结果表明,PLT-Exos可通过抑制滑膜增生、减少炎症细胞浸润、下调促炎因子表达、上调抗炎因子表达,减轻关节组织炎症损伤,保护软骨和骨结构,与体内宏观治疗效果一致。
7. PLT-Exos诱导M1在体内有效重编程为M2巨噬细胞
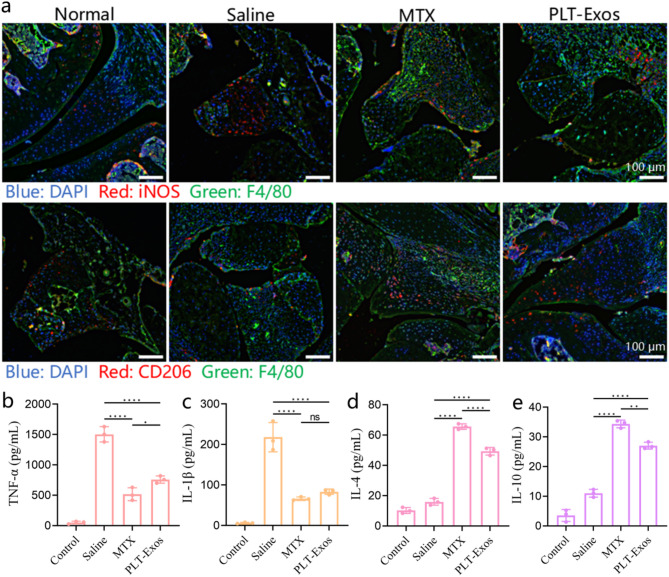
图7 PLT-Exos在体内诱导M1巨噬细胞向M2表型重编程。
图7A:免疫荧光染色结果。结果显示生理盐水组iNOS表达显著升高、CD206表达显著降低;PLT-Exos组iNOS表达降低、CD206表达升高,与MTX组效果相当。
图7B-E:关节组织ELISA检测结果。结果显示生理盐水组促炎因子TNF-α(图7B)、IL-1β(图7C)水平显著升高,抗炎因子IL-4(图7D)、IL-10(图7E)水平显著降低;PLT-Exos组上述因子水平均恢复至接近正常组水平,证实体内抗炎因子分泌增加、促炎因子分泌减少。
这些结果表明,PLT-Exos在CIA小鼠体内可有效诱导M1巨噬细胞向M2表型极化,重构关节局部炎症微环境,这是其发挥RA治疗作用的核心机制之一。
8. PLT-Exos的安全性
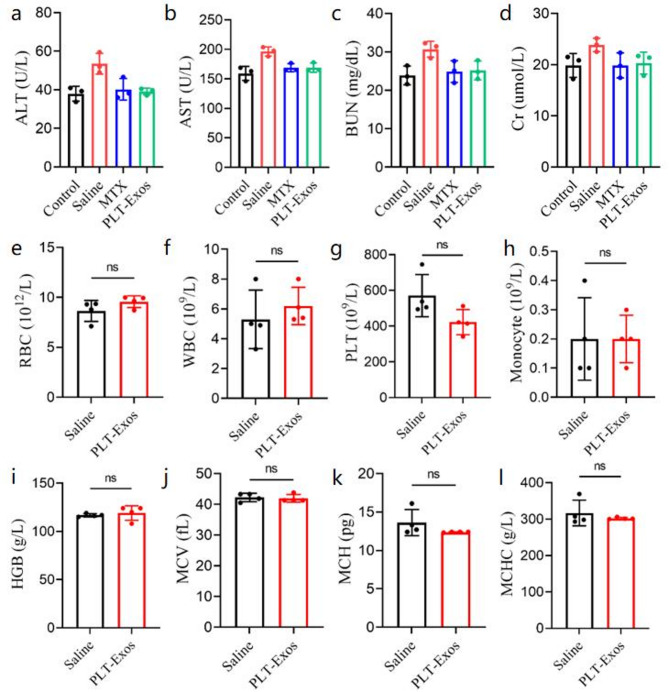
图8 PLT-Exos的安全性评估。
图8A-D:血清生化指标检测结果。结果显示PLT-Exos组小鼠血清中肝功能指标谷丙转氨酶(ALT,图8A)、谷草转氨酶(AST,图8B),肾功能指标血尿素氮(BUN,图8C)、肌酐(Cr,图8D)水平,与正常对照组无显著差异,提示PLT-Exos无明显肝肾功能毒性。
图8E-L:血常规检测结果。结果显示PLT-Exos组与生理盐水组相比,红细胞(RBC,图8E)、白细胞(WBC,图8F)、血小板(PLT,图8G)、单核细胞(Mon,图8H)比例,以及血红蛋白(HGB,图8I)、平均红细胞体积(MCV,图8J)、平均红细胞血红蛋白含量(MCH,图8K)、平均红细胞血红蛋白浓度(MCHC,图8L)均无显著差异,表明PLT-Exos不影响血液系统功能。
这些结果表明,PLT-Exos具有良好的生物相容性,静脉注射后对小鼠肝肾功能、血液系统无明显毒性,安全性优于可能引发副作用的临床药物MTX。
结论
该研究首次明确了PLT-Exos通过重编程巨噬细胞治疗RA的分子机制,为RA提供了一种靶向性强、疗效确切、安全性高的新型治疗策略。PLT-Exos作为天然来源的囊泡,无需复杂工程化改造,易于规模化制备,不仅为RA治疗提供了潜在候选药物,也为其他炎症相关自身免疫性疾病的治疗提供了新的思路和实验依据。






